Jonų mainai. Jonitai ir jų klasifikacija
Mainų talpa
Ionovio jonų mainų ir sorbcijos savybių kiekybinėms charakteristikoms naudojamos šios vertės: pilna, dinamiška ir dirbanti birža.
Pilnas mainų bakas(PO.) Nustatoma pagal funkcinių grupių skaičių, galinčių jonų mainų, oro sauso arba patinusių jonų masės ir yra išreikštas MM-EQ / G arba ME-EQ / L. Tai pastovi vertė, nurodyta jonato pase, ir nepriklauso nuo keitimosi jonų koncentracijos ar pobūdžio. Tai gali skirtis (sumažėjimas) dėl šilumos, cheminės ar radiacijos poveikio. Tikromis sąlygomis, jis sumažėja su laiku dėl jonato matricos senėjimo, negrįžtamas nuodų jonų absorbcija (organinė, geležis ir kt.), Kuri blokuoja funkcines grupes.
Equilibrium (statinis) mainų talpa priklauso nuo jonų koncentracijos vandenyje, pH ir jonato kiekio ir tirpalo santykiu matavimais. Reikia atlikti technologinių procesų skaičiavimus.
Dinaminis mainų tankas(Kasdien) - svarbiausias vandens valymo procesų rodiklis. Tikromis sąlygomis, daugialypis jonet vartojimas sorbcijos regeneracijos cikle, biržos pajėgumas nėra visiškai panaudotas, bet tik iš dalies.
Naudojimo laipsnį lemia regeneracinio agento regeneravimo ir srauto greitis, jonato kontakto laikas su vandeniu ir regeneruojančiu agentu, naudojamo prietaiso druskų, pH, dizaino ir hidrodinamikos koncentracija. Šis skaičius rodo, kad vandens valymo procesas sustabdomas tam tikra koncentracija ribojančia jonų, kaip taisyklė, ilgai iki visiško prisotinimo jonet. Šioje byloje absorbuotų jonų skaičius, atitinkantis stačiakampio a, priskirto jonet tūrį plotą ir bus kasdien.
Absorbuotų jonų skaičius, atitinkantis visišką prisotinimą, kai "Spock" yra 1, atitinkantis sumos ir tamsesnio figūros ploto sumą virš S-Pabaigos kreivės, vadinama bendra dinamiška mainų talpa (PD) . Tipo tipo vandens valymo procesuose paprastai jis neviršija 0,4-0,7.
Fig. vienas
Eksperimentinė dalis
Reagentai ir sprendimai:mgcl2 * 6H2O druskos distiliuotame vandenyje matavimo kolboje su 250 cm galia
Kalcio nitrato tirpalas (0,02 m) buvo parengtas ištirpinant mėginį (1,18 g) Salia Ca (NO3) 2 · 4N20. Ištirpinus mėginį, tirpalas praskiedžiamas distiliuotu vandeniu matavimo kolboje, kurių talpa yra 250 cm.
2 tirpalas Kalcio nitratas (O.1m) buvo parengtas ištirpinant mėginį (5,09 g.) CA (NO3) 2 · 4N20 druskų. Ištirpinus mėginį, tirpalas praskiedžiamas distiliuotu vandeniu matavimo kolboje, kurių talpa yra 250 cm.
Originalus sudėtingo sprendimas III.paruoštas iš fixanal. Standartizacija buvo atlikta pagal magnio sulfatą.
Buferiniai tirpalai, paruošti iš NH4CL "CHD.A." ir nh4oh.
Likusios MG 2+ jonų koncentraciją lėmė kompleksoNometriškai su erioichroma indikatoriumi T.
Likusios CA 2+ jonų koncentraciją lėmė kompleksoNometriškai su "Murcxide" indikatoriumi.
Sorbed koncentracija buvo nustatyta pagal pradinį ir likutinį.
Kaip sorbentas buvo naudojamas Zeolitai, turintys veislės artyhevsky pasireiškimo.
Sorbento virimas.
CSP Atheshevsky pasireiškimas trupinimo, sijojančių, surinktos granulių surinkimo su 1 - 2 - 3 mm dydžiu ir džiovinami džiovinimo spintelėje.
Jonų mainų konteineris statiniu režimu. 20 cm su tirpalu, kuriame yra CA 2+ jonų, kitais atvejais, MG 2+, su žinoma koncentracija ir
tam tikra PH vertė buvo pridėta 5,0 g sorbento, sukrėtė tam tikrą laiką ir atskirti kietą fazę filtruojant. Į
Chelamometrinio titravimo selektyvumas kalcio atžvilgiu gali būti pagerintas nustatant ryžtą stipriai alkoholio terpėje (magnio filtratas buvo nustatytas pagal CA 2+ jonų likutinę koncentraciją, kitais atvejais, mg 2+. Nustatyta paviršiaus koncentracija Kalbant apie šaltinį ir likučius.
Metalo chrominis indikatorius - MURIESID.
EDTA, 0,05 m tirpalas; Amonio buferio mišinys PH \u003d 9; NaOH, 2M tirpalas; Rodikliai - "Eryoichrom" juoda T ir MURIESID - kieta (mišinys su NaCl pagal 1: 100).
Metodologijos apibrėžimas
1. Analizuojamo tirpalo mėginys buvo perkeltas į titravimo kolbą, 10 cm3 amonio buferinio mišinio (pH 9), 25 cm3 distiliuoto vandens buvo pridėta, ant Spatula 30 - 40 mg Eriohrom iš juodos t ir nusveria sistemą, kad visiškai ištirptų rodiklį. Tirpalas įgytas vynas raudonas. EDTA tirpalo titravimas buvo atliktas iš buretės su nuolat maišant į spalvą aiškiai mėlyna spalva.
2. Analizuojamo tirpalo mėginys buvo perkeltas į titravimo kolbą, įpilama 5 cm3 2 m NaOH tirpalo, 30 cm3 distiliuoto vandens ir 30 MGxide mentelės galo. Tirpalas įgijo raudonos spalvos. Titravimą atliko EDTA tirpalas prieš purpurinio spalvos perėjimą.
Statistinių sąlygų apskaičiavimas pagal kalcio ir magnio jonus.
Magnio mainų pajėgumų nustatymas
20 cm3 Magnio chlorido tirpalas su ekvivalento koncentracija 0,02 mol / l pridėta ir 5,0 s sorbento išdžiovinta 105 0 s 1 valandą ir pakratykite tam tikrą laiką (0,5 val.). Kitais atvejais, 1 valanda ir pan. Pasibaigus laikui, tirpalas filtruojamas. Jis buvo imtasi siekiant analizuoti 5 cm 3 filtrato ir likutinė koncentracija mg 2+ jonų buvo nustatomas pagal kompleksikonometrinį metodą.
2. iki 20 cm3 kalcio chlorido tirpalo su moline koncentracija lygiavertį 0, l mole / l pridėta 5,0 g sorbento išdžiovinti 1050c už 1 valandą ir purtyti tam tikrą laiką (0,5 valandos). Kitais atvejais, 1 valanda ir pan. Pasibaigus laikui, tirpalas filtruojamas. Jis buvo imtasi siekiant analizuoti 5 cm3 filtrato ir likusią CA2 jonų koncentraciją buvo nustatyta pagal kompleksikonometrinį metodą.
CSP kontaktinio laiko ir Sprendimo Cacl2 * 4N2O įtaka CSP valiutos talpykloje statinėmis sąlygomis.
(C (Ca2 +) ex \u003d 0,1 mol / l; MCSP \u003d 5.0)
Didėjant etapų kontaktiniam gyvenimui, pastebimas pusiausvyros koncentracijos padidėjimas. Po 3 valandų įdiegta dinamiška valcavimo pusiausvyra.
6. Protokolo dėl standartizacijos, metrologijos ir sertifikavimo (IUS 11-12-94) nutraukimo 3-94 protokolo apribojimas (IUS 11-12-94)
7. Edition (2002 m. Sausio mėn.) Su pakeitimu (IUS 3-91)
Šis standartas taikomas joniečiams ir nustato dinamiško mainų bako nustatymo metodus su visa jonine regeneracija ir su tam tikru regeneravimo agento vartojimu.
Metodai susideda nustatant jonų skaičių absorbuojamas iš darbo tirpalo patinęs jonito tūris su nuolatiniu tirpalo srautu per jonito sluoksnį.
1. Mėginių ėmimo metodas
1. Mėginių ėmimo metodas
1.1. Mėginių ėmimo metodas rodo konkrečių produktų reguliavimo ir techninius dokumentus.
1.2. Jonitai, kuriuose drėgmės masė yra mažesnė nei 30%, mėginys imamas (100 ± 10). Patinimui, mėginys dedamas į stiklą, kurio talpa yra 600 cm ir pilama su sočiu tirpalu. Natrio chloridas, kuris turėtų būti padengtas pertekliumi, kad padengtų jonito sluoksnį su jo patinimu. Po 5 val. Ionio plaunamas distiliuotu vandeniu.
1.3. Jonitai su masės dalimi drėgmės, daugiau nei 30% imamas mėginio (150 ± 10) g į stiklinę 600 cm su talpa ir 200 cm distiliuoto vandens yra laikomasi.
2. Reagentai, tirpalai, indai, prietaisai
Vanduo, distiliuotas pagal "GOST 6709" arba "Demineralized", atitinka "GOST 6709" reikalavimus.
Bario chloridas pagal GOST 742, H.CH. tirpalą, kurio masės dalis yra 10%.
Kalcio 2-vandens chloridas, h.ch., koncentracijos tirpalai (SASL \u003d 0,01 mol / dm (0,01 n.) Ir (SASL) \u003d 0,0035 mol / dm (0,0035 n.).
Salono rūgštis pagal GOST 3118, H.Ch., tirpalai, kurių masės frakcija yra 5% ir koncentracija (HCl) \u003d 0,5 mol / dm (0,5 n.), (HCl) \u003d 0,1 mol / dm (0, 1 n. ) Ir (NSL) \u003d 0,0035 mol / dm (0,0035 n.).
Sieros rūgštis pagal GOST 4204, H.Ch., tirpalai, kurių masės frakcija yra 1%, koncentracija (HSO) \u003d 0,5 mol / dm (0,5 n.).
Natrio hidroksidas pagal GOST 4328, H.Ch., tirpalais, kurių masės frakcija yra 2, 4, 5%, koncentracija (NAOH) \u003d 0,5 mol / dm (0,5 n.), (NaOH) \u003d 0,1 mol / dm (0,1) n.), (NaOH) \u003d 0,0035 mol / dm (0,0035 n.).
Natrio chloridas pagal GOST 4233, H.C., prisotintą tirpalą ir koncentracijos tirpalą (Naci) \u003d 0,01 mol / dm (0,01 n.).
Mišrus indikatorius, sudarytas iš metilo raudonos ir metileno mėlynos arba metilo raudonos ir bromono žalios žalios, paruoštas pagal GOST 4919.1.
Metilo oranžinė arba metilo raudona indikatorius, tirpalas su 0,1% masės frakcija yra parengta pagal GOST 4919.1.
Fenolftaleino indikatorius, alkoholio tirpalas su 1% masės dalimi, paruošti pagal GOST 4919.1.
Amortizatorius cheminės kalkių CPI-1 pagal GOST 6755 arba kalkių yra NaRON.
Vamzdis (hlorkalcium) pagal GOST 25336.
Menzur 1000 pagal GOST 1770.
Cilindrai pagal GOST 1770 spektaklius 1-4, kurių talpa yra 100 ir 250 cm ir spektakliai 1, 2, kurių talpa yra 500 ir 1000 cm.
Akiniai į arba N pagal GOST 25336 bet kokiu našumu, kurio talpa yra 600 ir 1000 cm.
KLASKS KN-1-250 pagal GOST 25336.
Pipetės 2-2-100, 2-2-25, 2-2-20 ir 2-2-10 per NTD.
Buretės 1, 2, 2, spektakliai 1-5, 1, 2 tikslumo klases, kurių talpa yra 25 arba 50 cm, kurių padalijimo kaina yra ne didesnė kaip 0,1 cm, o 1, 2 tipų biurai, vykdymas 6, tikslumas 1, 2 klasių, kurių talpa yra 2 arba 5 cm, su padalijimo kaina ne didesnė kaip 0,02 cm.
1, 2 matavimo kolbos pagal GOST 1770, 1, 2 tikslumo klasė, kurių talpa yra 10, 25 ir 100 cm.
Sieta su valdymo tinklu 0315K pagal GOST 6613 su apvalkalu su 200 mm skersmens.
CCC-5000 puodelis pagal GOST 25336 arba iš polimerizacijos medžiagos pakanka įdėti sietą į jį.
Montavimo laboratorija (žr brėžinį) susideda iš buteliuko 1 ir stiklo kolonėlės su 6 vidiniu skersmeniu (25,0 ± 1,0) mm ir ne mažiau kaip 600 mm aukščio, kad būtų galima nustatyti dinaminį mainų pajėgumą visiško joninio regeneracijos ir vidinio skersmens sąlygomis (16,0 ± 0,5) mm ir mažiausiai 850 mm aukščio, kad būtų galima nustatyti nustatyto regeneruojančio agento srauto sąlygas. Apatinėje VPIAN filtro 7 stulpelio dalyje Por 250 Por 250 XC pagal GOST 25336 arba kitą filtravimo įtaisą, atsparus rūgštims ir šarmams, neperduodant jonų grūdų daugiau kaip 0,25 mm ir turintys mažą filtravimo varžą . Stulpelis yra prijungtas prie butelio su stiklo vamzdeliu 3 ir guminio žarna 4 su varžtu. HPP-1 absorberis.
Laboratorinis diegimas
Leidžiama naudoti kitas matavimo priemones su metrologinėmis savybėmis, kurios nėra blogesnės nei minėtos, taip pat kokybės reagentai ne mažesni už nurodytą.
3. Metodas nustatant dinaminį mainų pajėgumus su visu joniniu regeneracija
3.1. Pasirengimas bandymui
3.1.1. Pasirengimas bandymams atliekamas pagal GOST 10896 ir po treniruotės jonų laikoma uždaroje kolboje po distiliuoto vandens sluoksniu.
Kaotionitas KU-2-8 AG Prekinis ženklas ir prekės ženklo AB-17-8C į bandymą anijonas pagal GOST 10896 nėra paruošti.
3.1.2. Ioninis mėginys iš kolbos vandeninės pakabos pavidalu perkeliamas į cilindrą su 100 cm talpos ir užplombuokite jonato sluoksnį, paspaudus ant kieto cilindro dugno paviršiaus iki susitraukimo nutraukimo. Jonų tūris yra reguliuojamas iki 100 cm ir su distiliuotu vandeniu toleruoti jonus į stulpelį, po oro burbuliukų tarp jonijos granulių. Vandens perteklius iš stulpelio yra nusausintas, paliekant 1-2 cm sluoksnį per jonito lygį.
3.1.3. Stulpelyje jonai plaunami distiliuotu vandeniu, perduodant jį nuo viršaus iki apačios iki 1,0 dm / h greičio. Tuo pačiu metu anionitas plaunamas iš šarmų (pagal fenolftaleną) ir rūgšties katijonas (pagal metil oranžinį).
3.1.4. Labai privalomi anons hidroksilo formoje greitai įkraunamos ir plaunamos vandeniu, kuriame nėra anglies dioksido.
3.2. Bandymas.
3.2.1. Dinamiško jonų mainų pajėgumo nustatymas susideda iš kelių ciklų, kurių kiekvienas apima tris nuosekliąsias operacijas - sodrumą, regeneraciją, plovimą, kurių sąlygos pateiktos 1 lentelėje.
1 lentelė
Sąlygos nustatant dinamišką mainų pajėgumus su visais jonų regeneracija
Rodiklis. \\ T | Jonito klasė | Ionitų prisotinimo sprendimas | Saturacijos kontrolė | Regeneracija | |||
patenkinti | skalbiniai | regeneracija |
|||||
Dinaminis mainų gebėjimas slippath () | Stiprus | Kalcio chloridas (CaCl) \u003d 0,01 mol / dm (0,01 n.) | Prieš kalcio jonų koncentraciją filtrate (CA) \u003d 0,05 mmol / dm (0,05 mg · EQ / DM) nustato GOST 4151 | Druskos rūgštis, tirpalas su masės dalimi 5% | |||
Stiprus | Natrio chloridas (NaCl) \u003d 0,01 mol / dm (0,01 n.) | Prieš mažėjant šarmiškai 0,5 mmol / dm koncentracijos (0,5 mg · EQ / DM), palyginti su didžiausia stabilia vertė filtrate [mišri indikatorius, pavadinimas tirpalo, koncentracijos druskos rūgšties (HCl) \u003d 0,01 mol / dm (0,01 n.)] Ir prieš didinant chloro jonų turinį, palyginti su tvaraus filtrato turiniu (apibrėžta pagal GOST 15615) | Natrio hidroksidas, tirpalas su masės dalimi 5% | ||||
Silpnai | Prieš rūgščių filtratą (metil oranžine) | ||||||
Užbaigti dinamišką mainų pajėgumą () | Silpnai | Salono rūgštis (HCl) \u003d 0,1 mol / dm (0,1 n.) | Prieš išlyginant filtrato koncentraciją su darbo tirpalo koncentracija | Natrio hidroksidas, tirpalas su 2% masės dalimi | |||
Pastabos:
1. Nustatant CA jonų koncentraciją pagal GOST 4151
2. Specifinė apkrova yra tirpalo tūris per 1 valandą. Pavyzdžiui, 5 DM / DM · H atitinka filtravimo greitį, kuriame jis yra 100 cm tirpalo (8,3 cm / min.) Po 100 cm ionito.
3. Filtravimo greitis nustatomas matavimo cilindre, gaunamas tam tikru laiko intervalu.
Sprendimai ir vanduo šeriami iš viršaus į apačią. Naudojant AN-1 ANONITA ženklus ir AN-2FN tirpalai yra sumažinami iš apačios.
3.2.2 Prieš atliekant sodrumą, regeneraciją ir skalbimo operacijas, kolonėlė yra užpildyta atitinkamu tirpalu. Sprendimo sluoksnis virš jono turi būti (15 ± 3) cm.
3.2.3. Po sodrumo, regeneracijos ir plovimo stulpelyje per joną, palikite skysčio sluoksnį 1-2 cm aukščiu.
3.2.4. Joninis stulpelis užpildytas darbo tirpalu specifinei jonito klasei (žr. 1 lentelę), kad tirpalo sluoksnis virš jonų yra (15 ± 3) cm ir pasirinkite atitinkamą filtravimo greitį.
Kai 0,1 mol / dm koncentracija yra perduodama per stulpelį su jonu (0,1 n.), Filtratas surenkamas cilindruose, kurių talpa yra 250 cm, esant 0,01 mol / dm koncentracijai (0,01 n.) Cilindrai, kurių talpa yra 1000 cm. Antra ir vėlesniuose prisotinimo cikluose prieš išvaizdą filtrate išvaizda (nustatyta po pirmojo ciklo), filtratas surenkamas 100 ir 250 cm dalyse pagal koncentraciją Darbo sprendimas.
3.2.5. Iš kiekvienos filtrato dalies mėginys priimamas ir kontroliuoja prisotinimą pagal 1 lentelę.
3.2.6. Pasirodžius filtrato dalyje, darbinio tirpalo jonai apskaičiuoja bendrą filtrato kiekį.
3.2.7. Norėdami nustatyti visišką dinaminį mainų talpą, tirpalas ir toliau derinamas filtrato koncentracija su darbinio tirpalo koncentracija. Šio atvejo prisotinimo kontrolė atlieka mėginio titravimą su rūgšties tirpalu (natrio hidroksidu) su mišriu indikatoriumi prieš keičiant spalvą.
3.2.8. Prieš atliekant regeneraciją, jonitai stulpelyje sprogus distiliuoto vandens srovės iš apačios į viršų, kad visi jontos grūdai būtų judėti. KU-1 prekės ženklo kationijos sprogimas ir AN-1 ir AN-2FN ženklų anijonai atliekami prieš sodrumo veikimą.
3.2.9. Joninis regeneravimas atliekamas su rūgšties tirpalu (natrio hidroksidu) 1 lentelėje nurodytu greičiu. Filtratas nuolat montuojamas cilindru su cilindru, kurio tūris yra 250-1000 cm, pridedant 3-4 lašų indikatorių. Kai pasirodo rūgštis (natrio hidroksidas), jo koncentracija nustatoma filtrate vėlesnėse dalyse. Norėdami kontroliuoti filtratą, mėginys yra paimtas su pipete arba išmatuojama kolba ir titruoja rūgšties tirpalu (natrio hidroksido) koncentracija (HSL, HSO) \u003d 0,5 mol / dm (0,5 n.), (NaOH) \u003d 0,5 mol / DM (0, 5 n.) Esant indikatoriui
3.2.10. Rūgšties tirpalas (natrio hidroksidas) perduodamas filtrato koncentracijai suvienodinant regeneruojančio tirpalo koncentraciją.
3.2.11. Ionis po regeneracijos plaunamas distiliuotu vandeniu iki neutralios reakcijos pagal metil oranžinį (fenolftaleną) 1 lentelėje nurodytu greičiu. Tada jonas laikomas distiliuotame vandenyje 1 valandą ir filtrato patikrinkite dar kartą. Jei filtratas neturi neutralios reakcijos, jonas vėl plaunamas.
3.2.12. Dinamiško mainų pajėgumo apibrėžimas yra baigtas, jei paskutiniai gautos ciklai gautos rezultatai, tarp kurių neatitikimas neviršija 5% vidutinio rezultato.
3.2.13. Dinamiškam AB-17-8CC anijono keitimosi pajėgumui nustatomas dviem lygiagrečiais mėginiais pirmuoju sodrumo ciklu, prieš išvaizdą filtrate. Filtratas surenkamas 250 cm porcijomis. Dėl rezultatų vidutiniai aritmetiniai dviejų apibrėžimų rezultatai, leistinas neatitikimas tarp kurių neviršija 5% vidutinio rezultato.
(Pakeitimas, IUS 3-91).
4. Dinaminio mainų konteinerių nustatymo metodas su tam tikru regeneravimo suvartojimu
4.1. Pasirengimas bandymui
4.1.1. IONIS, parinktas pagal 1.2 ir 1.3 punktus, yra atskirtas nuo mažų frakcijų drėgnos pakartotinio pagal GOST 10900 metodą, naudojant sietą su tinkleliu N 0315K.
4.1.2. Atskiras anionitas yra įdėtas į stiklą, maišomas ir maišomas 500 cm natrio hidroksido tirpalo su 4% masės dalimi. Po 4 val, hidroksido tirpalas nusausinamas, o anijonas plaunamas vandeniu iki šiek tiek šarminės reakcijos pagal fenolftaleną ir perkeliamas į stulpelį, kaip nurodyta 3.1.2 punkte.
4.1.3. Atskira katijonas plaunamas iš suspensijos ir nutolusi su distiliuotu vandeniu su dekantavimu prieš šviesos plovimo vandenį ir perkeliamas į stulpelį pagal 3.1.2 punktą.
4.2. Bandymas.
4.2.1. Dinaminio mainų rezervuaras jonitų prieš pradedant nuo darbo tirpalo jonų išvaizda filtrate () susideda iš kelių ciklų, kurių kiekvienas apima tris nuoseklius operacijas - sodrumas, regeneravimas, plovimas, kurio sąlygos pateiktos 2 lentelėje. Sprendimai ir vanduo šeriami iš viršaus į apačią. Skysto sluoksnio aukštis virš jonet lygio yra nustatytas kaip nurodyta PP.3.2.2 ir 3.2.3.
2 lentelė
Sąlygos nustatant dinamišką mainų pajėgumus jonų tam tikrame regeneruojančiam vartojimui
Jonito klasė | Regeneracija | Konkretus vertės tarifas Regeneruotas | Nuplaukite kontrolę | Jonito sodrumo sprendimas | Saturacijos kontrolė | Filtravimo greitis |
||
nASA. | sušikti | registrai |
||||||
Stiprus | Iki liekamojo rūgšties koncentracijos filtrate ne daugiau | Kalcio chloridas (SASL \u003d 0,0035 mol / dm (0,0035 n.) | Prieš kalcio jonų koncentraciją filtrate daugiau (ca) \u003d 0,05 mmol / dm | |||||
Silpnai | Sieros rūgštis, tirpalas su 1% masės dalimi | Iki sieros filtrato nebuvimo (mėginys su Bacll į HCl) | Natrio hidroksidas (NaOH) \u003d 0,0035 mol / dm (0,0035 n.) | Iki koncentracijos natrio hidroksido filtrate (NAOH) \u003d 0,1 mmol / dm | ||||
Stiprus | Natrio hidroksidas su masės dalimi 4% | Iki natrio hidroksido koncentracijos filtrato ne daugiau (NaOH) \u003d 0,2 mmol / dm | Natrio chloridas (Naci) \u003d 0,01 mol / dm (0,01 n.) | Prieš mažėjant šarminiu koncentracija (NAOH) \u003d 0,7 mmol / dm | ||||
Silpnai | Natrio hidroksidas, tirpalas su masės dalimi 4% | Likusios natrio hidroksido koncentracijos filtrate ne daugiau (NAOH) \u003d 0,2 mmol / dm (0,2 mg · EQ / DM) per fenolftaleną | Druskos (sieros) rūgštis (HSL, HSO) \u003d 0,0035 mol / dm (0,0035 n.) | Iki likutinės rūgšties koncentracijos filtrate yra ne daugiau (h) \u003d 0,1 mmol / dm (0,1 mg · EQ / DM), indikatorius yra sumaišytas, pavadinimas tirpalas - natrio hidroksido koncentracija (NAOH) \u003d 0,01 mol / dm (0, 01 n.) | ||||
Pastabos:
1. Išreikšti konkrečios srauto greičio norma regeneruojančio agento () gramais ant molio pagal žodį "Mole" reiškia molines masė jonų ekvivalento (NA, K, Ca, mg, Cl, Ne, Nso, HSO, CO, taip
Ir kt.).
2. Tikrasis regeneruojančio agento srautas neturėtų skirtis nuo nurodytos normos daugiau nei 5%.
3. Nustatant SA jonų koncentraciją pagal GOST 4151, naudokite 2-3 lašų chrom-tamsiai mėlynos spalvos ir titravimo trilono-B koncentracijos (NAHCON · 2HO) \u003d 0,01 mol / dm (0,01
4. Specifinė apkrova yra tirpalo tūris, perduodamas per IONIS per 1 valandą. Pavyzdžiui, 5 dm / dm · h atitinka filtravimo greitį, kuriame jis yra 100 cm tirpalo (8.3 cm / min) po 100 cm ionito.
5. Filtravimo greitis nustatomas matavimo cilindre, gaunamas per tam tikrą laiko intervalą.
Siekiant išvengti katijonizito žalos, rūgšties regeneravimas ir plovimas iš regeneravimo produktų atliekamas be sustojimo, neleidžiant atotrūkiui tarp operacijų.
Prieš atliekant kiekvieną vėlesnį ciklą, jonas yra shinding vandens srautas iš apačios į viršų, kad visi Ionship grūdai juda.
4.2.2. Per jonus stulpelyje perduodamas regeneruojantis tirpalas, kurio tūris () kubinių centimetrų apskaičiuojamas pagal formulę
kur yra tam tikros regeneruojančio agento srauto greičio vertė, g / m · EQ);
- dinaminis mainų bakas; Pasirinkti pagal reguliavimo ir techninius dokumentus konkrečioje Ionyje, mol / m (r · Eq / m); Dėl jonitų, AB-17-8, AN-31 ir EDE-10P klases leidžiama pirmosios regeneracijos padidėjusi dinamiško mainų pajėgumų vertė 3;
- Ionitos mėginiai, cm;
- Regeneruojančio skiedinio, G / DM koncentracija.
Regeneruojančio tirpalo kiekis matuojamas stulpelio išėjime su cilindru arba benzuru. Tada stulpelis atjungtas, stulpelyje esančio tirpalo lygis yra sumažintas iki 1-2 cm ir uždarytas mažesnis už
4.2.3. Ionitai po regeneracijos plaunami distiliuotu vandeniu nuo rūgšties (natrio hidroksido) perteklių 2 lentelėje nurodytu greičiu.
Periodiškai pasirinkite filtrato mėginį ir titratų natrio hidroksido tirpalus (rūgšties) koncentraciją (NaOH, HCl, HSO) \u003d 0,1 mol / dm (0,1 n.) Esant metilo oranžinei (fenolftalenui).
Nuplaukite 2 lentelėje.
4.2.4. Po plovimo stulpelis pripildytas darbaratį ir nustatykite prisotinimo greitį nuo 2 lentelės.
Dirbdami su koncentracijų darbo tirpalais 0,01 mol / dm (0,01 n.) Filtratas yra surinktas į cilindrą, kurio talpa yra 250 cm, esant 0,0035 mol / dm koncentracijai (0,0035 n.) Naudokite cilindrą su a 1000 cm talpa. Antra ir vėlesni prisotinimo ciklai prieš išvaizdą filtrate išvaizda (nustatoma po pirmojo ciklo), filtratas surinkamas 100 ir 250 cm, atitinkamai darbo tirpalo koncentracija.
4.2.5. Norėdami kontroliuoti prisotinimą nuo filtrato dalies, mėginys imamas ir analizuojamas pagal 2 lentelę. Jei analizės rezultatas rodo, kad prisotinimo lygis nepasiekė 2 lentelėje nurodytų verčių, visi ankstesni filtrato mėginiai negali būti analizuojami.
4.2.6. Pasirodydamas darbo tirpalo jonų filtrato dalį 2 lentelėje nurodytos sumos, prisotinimas baigtas ir apskaičiuojamas bendras filtrato () ir dinaminis mainų konteineris.
4.2.7. Jon yra taikoma antrajam regeneracijai ir plovijami pagal.2.2 ir 4.2.3 punktus.
Apskaičiuojant regeneravimo agentą, reikalingą antrajam ciklui, dinamiško mainų konteinerio vertė, gauta pirmuoju ciklu pagal 4.2.6 punktą, naudojama pagal 4.2.6 punktą.
Prieš atliekant vėlesnius prisotinimo ciklus, regeneravimo suvartojimas apskaičiuojamas pagal dinamišką mainų pajėgumą, gautą ankstesniame cikle.
4.2.8. Apibrėžimas baigiasi, jei paskutiniai ciklai gaunami rezultatai, kuriuos leidžiami neatitikimai, kurių neviršija 5% vidutinio rezultato, su faktiniu konkrečiu regeneruojančio agento srautu, skiriasi nuo nurodytos normos ne daugiau kaip 5%.
5. Apdorojimo rezultatai
5.1. Dinaminis mainų talpa () kubiniame metrui (r · EQ / m), kol filtrate atsiranda veikimo tirpalo jonai, apskaičiuojami pagal formulę
kur - bendras filtrato kiekis, perduotas per jonus, prieš išvaizdą išjungiant darbo tirpalo jonus, žr.;
- jonet apimtis
5.2. Tikrasis regeneruojančio agento srauto greitis () gramais per MOL (G / G EQ) absorbuotų jonų apskaičiuojamas pagal formulę
kur yra regeneravimo skiedinio tūris;
- regeneravimo tirpalo koncentracija, g / dm;
- bendras filtrato kiekis, perduotas per jonus, kol pasirodo darbo tirpalo jonai;
- Darbo tirpalo koncentracija, MOL / DM (n.
5.3. Visiškas dinaminis mainų pajėgumas () moliuose per kubinį metrą (R · EQ / M) apskaičiuojami pagal formulę
kur - bendra filtrato suma, perduodama filtrato koncentracijos ir darbinio tirpalo koncentracijai, cm;
- darbo tirpalo koncentracija, mol / dm (n.);
- filtrato dalies tūris po darbo tirpalo jonų (praleidimas), cm;
- tirpalo koncentracija filtrato porcijomis po darbo tirpalo jonų (praleidimas), mol / dm (n.);
- jonet tūris,
5.4. Dėl apibrėžimo rezultatas, vidutiniai aritmetiniai rezultatai dviejų pastarųjų ciklų yra imami, neatitikimai tarp kurių neviršija ± 5%, su patikimu tikimybe \u003d 0,95.
Pastaba. Išreiškiant dinamišką jonų mainų talpą kubiniame metrui pagal žodį "mole", yra molinė masė jonų ekvivalentas (Na, K, Ca, mg, Cl, ne, NSO, HSO, CO, taip ir tt ).
Dokumento tekstas yra išspręstas:
oficialus leidimas
Jonitai. Nustatymo metodai
valiutos talpa: Sat. Gostovas. -
M.: IPK leidybos standartai, 2002 m
Bendrosios sąvokos
Apskritai žodžiai, pagal jonų mainų dervą, jis suprantamas kaip jonų skaičius, kurį galima absorbuoti tam tikru dervos kiekiu. Be to, dervos talpyklos matavimo vienetas gali būti kitoks. Pavyzdžiui, mm-eq / ml (meq / ml), p. (EQ / L) arba kilogranas ant kubinės pėdos (KGR / FT3). Žinant lygiavertę masę, galite apskaičiuoti dervo rezervuarą. Lygiavertė medžiagos masė apibrėžiama kaip medžiagos molinės masės santykis su savo valencija (griežtai kalbant į medžiagos lygiavertiškumo skaičių). Pavyzdžiui, kalcio molinis svoris yra 40 g. / Mol, o valencija 2, tada lygiavertė masė yra lygi 20 g. / Mol (40/2 \u003d 20). ION mainų dervos su 1,95 g - EQ / l keitimo talpa gali pašalinti 1,95 h 20 \u003d 39 gramus iš tirpalo 1 litro dervos.
Praktiškai dervos biržos pajėgumas nustatomas titravimo laboratorijose. Per stulpelį, kuriame soda yra įdėta į vandenilio pavidalą (H formos), yra perduodamas natrio hidroksido tirpalas (NAOH). NA + jonų dalis keičiama vandenilio jonais. Natrio hidroksidas, kuris nebuvo patekęs į reakciją su joninės dervos grupe, yra valomas rūgštimi. Suteikite iš pradinės natrio hidroksido koncentracijos, likusi koncentracija gali būti nustatoma pagal katijono konteinerį. Kitas būdas nustatyti jonų mainų pajėgumus yra perduodamas per kalcio chlorido tirpalo dervos sluoksnį. Panašiai nustatoma anijoninio biržos dervos (OH forma) rezervuaras, per kurį perduodamas rūgšties tirpalas.
Dervos talpumas gali būti matuojamas MM-EQ / ML (tūrį) arba mg-EQ / g (svoris). Jei yra apibrėžtas indas, išreikštas mm-Eq / g / g) (ir sausos jonų masė yra skirta), žinant dervos drėgmę, lengva eiti į mm-Eq / ml.
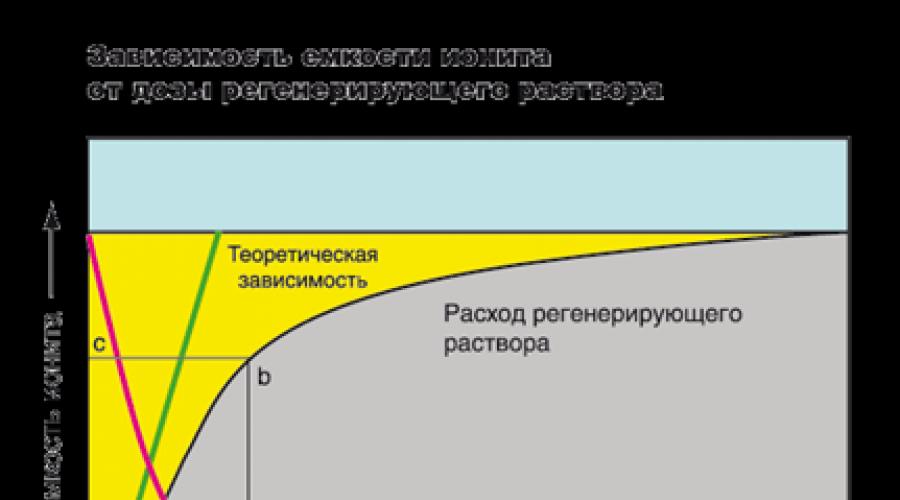
Paveiksle dervos keitimo talpa grafiškai pavaizduota geltona spalva, esanti tarp vertikalios tiesios ir Cl. Pilka, esanti žemiau kreivės, plotas yra jonų koncentracija išgryninto vandenyje. Dviračio pradžioje filtrato jonų koncentracija yra labai maža ir išlieka pastovi visoje filtravimociklyje, tuo metu, kai filtravimo priekis pasiekia IONE sluoksnio pabaigą, jonai atsiranda į filtratą ( Paveikslas - P punktas P). Tai signalas atgaivinti regeneraciją. Paprastai filtro regeneravimas atliekamas su slydimu. Pavyzdžiui, pramonėje, standumo jonų koncentracija, kurioje filtras yra gaunamas regeneracijai, gali pasiekti mažiau kaip 0,05 03 vertę, o vidaus minkštinimo sistemose - mažiau nei 0,5 0. X - Y segmento ilgis atitinka išgryninto vandens tūrį litrais ar galonais. ANLB figūrų plotas yra visiškai absorbcija dervos, o ANMB figūra plotas yra absorbuotų jonų skaičius iki slippath atsiradimo.
Kalbėdamas apie bakas, mes dažnai reiškia veikti tiksliai, o ne visiškai mainų konteinerį. Darbo pajėgumai nėra nuolatinė vertė, tai priklauso nuo veiksnių rinkinio: jonito prekės ženklo, absorbuotų jonų koncentracijos ir tipo, tirpalo pH, išvalyto vandens reikalavimų, srauto greičio, aukščio Jonito sluoksnio ir kitų reikalavimų.

Didelio masto jonų ekstrahavimo pasiekimas iš vandeninio tirpalo reikia padidinti regeneruojančio tirpalo dozę (raudona linija). Tačiau didinant regeneruojančio tirpalo koncentraciją yra be galo neįmanoma (žalioji linija yra teorinė priklausomybė nuo dervos talpos sumažinimo laipsnio ir regeneravimo tirpalo srauto greitis). Praktiškai, norint pasiekti didelį pajėgumą, būtina padidinti dervų skaičių. Su pirmuoju filtrui, sumažinti jonų mainų savybių laipsnį gali siekti 100%, tačiau laikui bėgant ši vertė sumažės. Pavyzdžiui. Dauguma vandens minkštinimo sistemų gamintojų rekomenduojama naudoti NaCl tirpalą su 100-125 g. / L koncentracija, kad būtų atkurta iki 50 - 55% visos keitimo konteinerio.
Nustatant konteinerį, būtina žinoti dervos jonų formą (druska, rūgštis, pagrindinė). Su regeneracija arba veikimo procese, pumpuojamų dervų pokyčių tūris, procesas vadinamas derva vadinamas "kvėpavimas". Lentelėje matyti, kaip dervos elgiasi įvairiuose procesuose.
Atskirti katijoną ir anijoniką. Reakcijos, kuriose jonai dalyvauja lentelėje.
jonų mainų dervos reakcijos titravimas

Be to, anglų kalbos literatūroje SAC simbolis rodo stipriai rūgštinį katijoną, SBA yra labai naudinga anijonas, WAC yra silpnai rūgštinis katijonas, o WBA yra silpnai palanki anijonija. Gebėjimas jonų mainams nustatomas pagal funkcinės grupės buvimą, stipriai rūgštus katijonus yra sulfo grupė - SO3H, ir silpnai rūgšties rūgšties katijonas karboksilo grupės - Cooh. Labai rūgščiai keičiasi katijonais bet kokios pH vertės, tai yra, jie elgiasi kaip stiprios rūgštys tirpalu. Silpniai rūgšties rūgšties katijonas yra panašus į silpnas rūgštis ir reaguoja jonų mainai tik pH vertės virš 7. Anijonika yra funkcinių grupių penkių tipų: (-NH2, NH \u003d, N?, - N (CH3) 3OH, - N (CH3) 2OH4OH). Pirmosios trys grupės suteikia prastai palankių savybių anijoną ir grupes - N (CH3) 3OH, - N (CH3) 2C2H4OH - stipriai kasyba. Silpnai draugiški anadai reaguoja su stiprių rūgščių anijomis (taip, Cl-, ne) ir labai privalomi su stipriais ir silpnais (HCO, HSI) anijomis nuo 1 iki 14. Kalbant apie labai privalomų rezervuarą Anionas, turėtumėte atkreipti dėmesį į tai, kad dervos yra funkcinių grupių būdingos ir prastai palankios anijonikos. Senėjant labai privalomą anijoną arba esant aukštai temperatūrai, yra pradinio ir dalinio funkcinių grupių sunaikinimo sumažėjimas.
Apsvarstykite daugiau reakcijų nutekėjimo su jonų mainų dervų dalyvavimu. Reakcija 1 - Vandens minkštinimas ant stipriai rūgštiniu druskos (NA) formų katijonu, 2 - Nitratų jonų pašalinimas labai privalomas anijonas CL-forma. Paraiška, kaip regeneruojantis natrio chlorido ir kalio chlorido sprendimas prisideda prie plačiai naudoti šio tipo derva kasdieniame gyvenime, pramonėje ir nuotekų valyme. Cationijas taip pat galima atkurti rūgšties tirpalais (pavyzdžiui, druskos rūgštimi) ir anijonais - kaustinės sodos tirpalu (NaOH). Ionitai H ir OH forma yra naudojami schemose, skirtų schemose, kai preparatas (3 ir 4 reakcija). Silpnai rūgštus katijonas nurodomas ION mainų savybėmis didelėmis pH vertėmis (5 reakcija) ir silpnai ašies anionite - esant mažoms pH reikšmėms (reakcija 6). Reakcija 5 yra vienu metu minkštėja ir sumažėjo vandens šarmiškai. Pažymėtina, kad WBA derva dėl regeneracijos su šarminiu tirpalu nėra perduodamas OH formoje, tačiau vadinamoji FB forma (laisva bazė).
Silpnai rūgštus kationis, palyginti su stipriomis rūgštimis, turi didesnį keitimosi pajėgumus, jiems būdingas dideli vandenilio jonų afinitetas, todėl regeneravimas palengvina ir greičiau. Svarbu, kad už WAC regeneraciją, taip pat WBA, natrio chlorido ar kalio tirpalai nenaudojami. Vieno ar kito jonų mainų dervos pasirinkimas priklauso nuo daugelio sąlygų. Pavyzdžiui, išskiriami dviejų tipų labai kasybos anijonika: I tipo (funkcinė grupė - N (CH3) 3OH) ir II tipo (-N (CH3) 2C2H4OH). I tipo anijoms geriau sugeria HSIO jonus, priešingai nei II tipo anijonikai, tačiau pastarosios pasižymi didesniu mainų pajėgumu ir geriau regeneruojami.
Apibendrinant, mes dėmesį, kad literatūroje, taip pat pase ant produktų, bendras svorio ir mainų rezervuaras dervos yra nurodyta, kuri yra apibrėžta laboratorijoje. Dervos darbinis pajėgumas yra mažesnis už gamintoją deklaruojant ir priklauso nuo daugelio veiksnių, kurių negalima atsižvelgti į laboratorines sąlygas (dervų sluoksnio geometrines charakteristikas, konkrečios proceso sąlygos: transliacijos greitis, ištirpusių medžiagų koncentracija, regeneravimo laipsnis ir tt).
VION medžiagos naudojamos ventiliacijos išmetamųjų dujų išvalymui iš tirpių komponentų, rūgščių ir sunkiųjų metalų druskų aerozolių, kur jie naudojami daugiausia neaustinės adatos laipiojimo drobičių pavidalu.
Progresas:
Pasveriama 2 gr. Katitatita Vion KN-1 (sausas). Supilkite į bures. Perkelkite originalų CUCL 2 (3,6 mmol / l) per stulpelį, užpildytą katijonu. Toliau šliaužiame mėginį 50 ml titravimo. Remiantis metodika (3.1 punktas), mes nustatome mėginio optinį tankį ir suraskite vario koncentraciją. Rezultatai pateikiami 3.5 lentelėje.
3.5 lentelė
|
C, mmol / l |
||||
Jie pastatė vario koncentracijos priklausomybę filtrate nuo tirpalo tūrio per jonet.
Fig. 3.4.
Sorbcijos procesas yra visiškai sugerti pirmąsias katijonų dalis, o absorbcijos sritis palaipsniui juda išilgai stulpelio į išvestį. Po to momentas įvyksta, kai dėl katijono konteinerio išsekimo, katijonai pradeda išeiti iš stulpelio. Iš grafiko matyti, kad vario koncentracija stulpelio išleidimo metu palaipsniui didėja ir turi S formos kreivės formą, pradedant nuo nulinės koncentracijos iki maksimalios. Ši kreivė yra ištempta su mažomis druskų koncentracijomis.
Apskaičiuota vario kiekį, kuris absorbuojamas stulpelį iki bendros prisotinimo katijonui, kaip figūros plotas, ribotos S formos kreivės ir tiesioginės didžiausios koncentracijos:
h \u003d? VI * (Cmax - CI) (3)
kur vi \u003d 50 ml,
Cmax \u003d 3,6mmmol.
h1 \u003d 2.20 mmol.
Apskaičiuota tūrinė talpykla:
z1 \u003d H1 / m k \u003d 2.20 / 2 \u003d 1,10 mmol / gr. Kationata.
Rezultatų diskusija
Eksperimentinio darbo metu buvo nustatytas trijų skirtingų katijonų mainų pajėgumas (KU-2-8, KU-1, VION KN-1). Rezultatai pateikiami 3.5 pav.

Bendras katijono mainų bakas yra proporcingas figūros plotai, ribotos S formos kreivės ir tiesioginės maksimalios koncentracijos. Kaip matyti iš 3.5 pav. Įvairių jonų talpyklos yra skirtingos ir mažesnės už visišką paso nurodyto paso katijonų katijonų pajėgumą. Taigi visiškas KU-2-8 katijono keitimo pajėgumas yra eksperimentiškai mažesnis už paso vertę 28%, visiškas KU-1 mainų pajėgumas yra mažesnis už paso vertę 57%, o vion kN-1 katijonas yra 39%. Apskaičiuojant ir projektuojant jonų mainų aparatus ir filtrus reikia atsižvelgti į šiuos duomenis.
Jonų mainų pajamos tose adsorbenduose, kurie yra polielektros (jonų biržos, jonų mainų dervos).
Jonų mainailygiavertis jonizacijos mainų procesas jonų šilumokaičiu vadinamas kitais to paties ženklo jonais sprendime. Jonų mainų procesas yra grįžtamas.
Ionitai yra suskirstyti į katijonus, anijonus ir amfoterines jonitų.
Katijai- medžiagos, turinčios fiksuotas neigiamai apmokestintas grupes jų struktūroje (fiksuoti jonai), kurie juda judančiais katijomis (kovos su jomis), kurios gali keistis su katijais tirpalu (81 pav.).
Fig. 81. Polielectrolytės matricos (katijono) modelis su fiksuotomis anijomis ir judančiomis kovomis, jei - fiksuoti jonai;
- conses, - tarybos
Natūralūs katijonai: zeolitai, permutiitas, silicio gelis, celiuliozė, taip pat dirbtinis: aukštos molekulinės masės kietos netirpios joninės polimerai, kuriuose yra dažniausiai sulfo grupių, karboksilo, fosfinų rūgšties, arseno rūgšties ar seleno grupių. Sintetiniai neorganiniai katijonai, kurie dažniausiai naudojami aliuminiolicates.
Remiantis joninių grupių jonizacijos laipsniu, katijonai yra suskirstyti į sunkų rūgštį ir silpnumą. Labai rūgščiai katijonai gali keistis savo mobiliuosius katijonus išorinių katijonų šarminėje, neutralioje ir rūgštinėje aplinkoje. Silpnai rūgščių keitimo mainai keičiasi kitais katijais tik šarminės aplinkoje. Labai rūgštus yra cationis su stipriomis disocicijomis rūgšties grupėmis - sulfonrūgštis. Silpnai rūgštis apima kationį, kuriuose yra silpnai rūgštinių rūgščių grupių - fosforo rūgšties, karboksilo, oksidhenilo.
Anionitai- jonų keitikliai, kuriuose yra teigiamai apmokestintos joninės grupės jų struktūroje (fiksuoti jonai), kurie yra judantys anijoniai (kovos su sandoriai), kurie gali keistis su anijomis, kurios yra tirpale (82 pav.). Atskirti natūralią ir sintetinę anijoniką.

Fig. 82. Polielectrolyte matricos (anijono) modelis su fiksuotomis katijomis ir judančiomis kovomis, kur + yra fiksuotos jonai;
- conses, - tarybos
Sintetinėje anijonijoje yra teigiamai įkrautos joninės grupės makromolekulės. Silpnai-jauki anijonika yra jų sudėties pirminės, antrinės ir tretinių amino grupėse, labai privalomi anijonuose yra ketvirtinių svogūnų druskų ir bazių grupių (amonio, piridiniumo, sulfonio, fosfonio). Labai privalomi anons keistis judančiais anijomis rūgštinėje, neutralioje ir šarminėje žiniasklaidoje, silpnai ašyje - tik rūgštinėje aplinkoje.
Amfoteriniai jonitaijame yra ir katijoninės, ir anijoninės joninės grupės. Šios jonai gali sorbitų ir katijonų ir anijonų.
ION kiekybinė savybė yra pilnas mainų bakas(PO). Nustatymą galima atlikti statiniu arba dinamišku metodu, pagrįstu reakcijomis, tekančiomis IONBIT - sprendimų sistemoje:
RSO 3 - H + + NaOH → RSO 3 - NA + + H 2 O
RNH 3 + OH - + HCl → RNH 3 + CL - + H 2 O
Talpa nustatoma pagal jonų grupių skaičių jonate ir todėl teoriškai turi būti pastovi vertė. Tačiau tai praktiškai priklauso nuo tam tikrų sąlygų. Yra statinio mainų tankai (SEO) ir dinaminis mainų pajėgumas (DEE). Statinis mainų pajėgumas yra pilnas konteineris, kuris apibūdina bendrą jonų grupių (Milecquvivvalents) už vieneto masės oro sausos jonų arba Na vieneto patinęs Ionio sumos. Natūralūs jonitai turi nedidelį statinį metabolinį pajėgumą, ne didesnį kaip 0,2-0,3 mekv / g. Sintetiniams jonų mainų dervoms jis yra 3-5 mekv / g, o kartais pasiekia 10,0 meko / g.
Dinaminis, ar darbas, valiutų gebėjimai taikoma tik IONGepps, kuri dalyvauja jonų mainų, kurie vyksta technologinėse sąlygose, pavyzdžiui, jonų mainų stulpelyje tam tikru santykiniu jonito ir sprendimo greičiu. Dinaminis talpa priklauso nuo judėjimo greičio, stulpelio dydį ir kitus veiksnius ir visada yra mažesnis už statinį metabolinį gebėjimus.
Norėdami nustatyti statinio mainų talpyklą jonitų, naudojami įvairūs metodai. Visi šie metodai yra sumažinti iki jonų prisotinimo bet jone, tada išstumti jį su kita jonų ir pirmojo tirpalo analizė. Pavyzdžiui, katijonas yra patogiai išverstas į H + -Form (liejimo vandenilio jonai), tada nuplaukite natrio chlorido tirpalu, o gautas rūgštus tirpalas pašalinamas su šarminiu tirpalu. Talpa yra lygi rūgšties kiekiui, kuris praėjo į rūgšties tirpalą į IONON nuotaiką.
Su statiniu metodu, rūgštimi arba šarmais yra titruojamas, kuris dėl jonų mainų adsorbcijos atsiranda tirpale.
Dinamišku metodu tai nustatoma chromatografiniais stulpeliais. Per stulpelį, pripildytą jonų mainų dervos, elektrolito tirpalas perduodamas ir absorbuotos jonų koncentracijos pasenusiame tirpale (eliuatas) yra įrašomas nuo praeities tirpalo tūrio (išėjimo kreivės). Apskaičiuojamas pagal formulę
 , ,
| (337) |
kur V. Iš viso - bendras tūris, apimantis iš derva tiekiamos rūgšties; nuo. - rūgšties koncentracija šiame tirpale; m. - ION mainų dervos masė stulpelyje.
Equilibrium Exchange konstanta gali būti nustatoma iš duomenų apie pusiausvyros pasiskirstymą jonų statinėmis sąlygomis (pusiausvyros būklė jonų mainai aprašyti pagal masės įstatymą), taip pat dinamiško metodo judant zonoje Medžiaga palei dervos sluoksnį (eliuento chromatografiją).
Už jonų mainų reakciją
![]()
equilibrium pastovus yra lygus
 , ,
| (338) |
kur, - jonų koncentracija jonet; - jonų koncentracija tirpale.
Taikant joniją, galite sušvelninti vandenį arba nudeginti druskos vandenį ir gauti tinkamą farmacijos tikslais. Kitas jonų mainų adsorbcijos vartojimas vaistinėje yra naudoti jį analitiniais tikslais kaip analizuojamos vienos ar kitos sudedamosios dalies mišinių ekstrahavimo metodas.
Pavyzdžiai sprendžiant problemas
1. 60 ml tirpalo su tam tikros medžiagos koncentracija, 0,440 mol / l dedamas įjungtas anglies sveriantis 3 g. Sprendimas su adsorbentu buvo sukrėtė, kad sukurtų adsorbcijos pusiausvyrą, dėl kurių medžiagos koncentracija sumažėjo iki 0,350 Mol / l. Apskaičiuokite adsorbcijos reikšmę ir adsorbcijos laipsnį.
Sprendimas:
Adsorbcija apskaičiuojama pagal formulę (325):

Pagal formulę (326), nustato adsorbcijos laipsnį
2. Pagal pateiktus duomenis, už dimedrolio adsorbcija ant anglies paviršiaus, apskaičiuoti grafiškai konstantos Langmur lygtį:
Apskaičiuokite dimedrolio adsorbciją į 3,8 mol / l koncentraciją.
Sprendimas:
Grafiškai nustatyti Langmuiro lygties konstantą, naudojame linijinę šios lygties formą (327):
Apskaičiuokite 1 / bet ir 1 / nuo.:
Sukurkite koordinates tvarkaraštį 1 / bet – 1/nuo.(83 pav.).
Fig. 83. Langmuro \u200b\u200blygties konstantų grafinis apibrėžimas
Tuo atveju, kai taškas h.\u003d 0 yra už brėžinio, naudokite antrasis kelias y \u003d ax + b. Pirma, pasirinkite du bet kokius taškus, esančius tiesiai (83 pav.) Ir nustatykite jų koordinates:
(·) 1 (0,15; 1,11); (·) 2 (0,30; 1,25).

b \u003d Y 1 - AX 1 \u003d0,11 - 0,93 · 0,15 \u003d 0,029.
Mes tai gauname b. = 1/bet ¥ \u003d 0,029 μmol / m 2, todėl bet ¥ \u003d 34,48 μmol / m 2.
Nuolatinis adsorbcijos pusiausvyros K.nustatoma taip:
Apskaičiuokite difrololio adsorbciją į 3,8 mol / l koncentraciją pagal Langmuiro lygtį (327):
3. Studijuojant benzenkarboks adsorbciją ant kieto adsorbento, šie gautos duomenys:
Sprendimas:
Apskaičiuoti Freundlicho lygties konstantą, būtina naudoti linijinę lygties (332) linijinę formą LG koordinatėse ( x / T.) – lg. nuo. Izoterminis yra tiesioginis.
Rasti LG reikšmes c. ir LG. x / M.įtraukta į linijinį freundlich lygtį.

| Lg. c. | –2,22 | –1,6 | –1,275 | –0,928 |
| Lg. x / M. | –0,356 | –0,11 | 0,017 | 0,158 |
Sukurkite tvarkaraštį LG koordinatėse ( x / T.) – lg. nuo.(84 pav.) .
Fig. 84. Freundlich lygties konstantų grafinis apibrėžimas
Nuo taško h.\u003d 0 Įsikūręs už nuotraukos (84), mes naudojame antrasis kelias Tiesioginio koeficientų apibrėžimas y \u003d ax + b(Žr. "Įvadinis blokas. Eksperimentinių duomenų matematinio apdorojimo pagrindai"). Pirma, pasirinkite du bet kokius taškus, esančius tiesioje linijoje (pvz., 1 ir 2 punktuose) ir nustatykite jų koordinates:
(·) 1 (-2,0; -0,28); (· -1,0; 0,14).
Tada apskaičiuojame kampinį koeficientą pagal formulę:

b \u003d Y. 1 - AX. 1 = -0,28 - 0,42 · (-2,0) \u003d 0,56.
Freundlich lygties konstantos yra lygios:
lg. K \u003d b \u003d0,56; K.= 10 0,56 = 3,63;
1/n \u003d a \u003d0,42.
Apskaičiuokite benzenkinio rūgšties adsorbciją 0,028 mol / l koncentracijoje, naudojant Freundlich lygtį (330):
4. Naudojant statymo lygtį, apskaičiuokite konkretų adsorbento paviršių pagal dujinio azoto adsorbcijos duomenis:
Azoto molekulė užima tankų monolayer yra 0,08 nm 2, azoto tankis yra 1,25 kg / m 3.
Sprendimas:
Lyginamos linijinės formos polimolekulinio adsorbcijos lygtis turi formą (333)
Norėdami sukurti grafiką, nustatykite vertes:
Sukurti koordinates tvarkaraštį - P / P s (85 pav.).
Naudojant. \\ T pirmasis metodas (Žr. "Įvadinis blokas. Eksperimentinių duomenų matematinio apdorojimo pagrindai") Tiesioginių koeficientų apibrėžimas y \u003d ax + b. Mes apibrėžiame koeficiento vertę b.kaip taško ordinatas, esantis tiesiai, kuris yra abscisa, lygus 0 ( h.= 0): b. \u003d 5. Pasirinkite tašką tiesiai ir nustatykite jo koordinates:
(·) 1 (0,2; 309).
Tada apskaičiuojame kampinį koeficientą:


Fig. 85. Statymo izotermos polimolekulinio adsorbcijos konstantų grafinis apibrėžimas
Konstantos izoterminės polimolekulinio adsorbcijos statymo lygtis yra lygūs:
 ; .
; .
Sprendžiant lygčių sistemą, gauti bet ∞ \u003d 6,6 · 10 -8 m 3 / kg.
Apskaičiuoti adsorbcijos ribinę vertę, mes imsimės bet ∞ iki 1 mol:
 .
.
Konkrečios adsorbento paviršiaus vertė nustatoma pagal formulę (329):
5. Polistireno sulfocationitis N + -Form svorio 1 g buvo įvesta į KCL tirpalą su pradine koncentracija nuo. 0 \u003d 100 EQ / m 3 tūris V.\u003d 50 ml ir mišinys buvo laikomas pusiausvyros būsenai. Apskaičiuokite kalio pusiausvyros koncentraciją jonate, jei jonų mainų pusiausvyros konstanta yra konstanta, o bendras katijono mainų bakas yra PO \u003d 5 MOL EQ / kg.
Sprendimas:
Norėdami nustatyti jonų mainų pastovumą, naudokite lygtį (338). Dervos, H + jonų keitimasis lygiaverčiu jonų skaičiumi K.
Sulfocationito masė H + -forma nustatoma pagal formulę (337):


Bendras anijono skaičius yra lygus:
Anijono masė jame taip pat nustatoma pagal formulę (337):
