Ionska razmjena. I njihova klasifikacija
Razmjena kapaciteta
Za kvantitativne karakteristike ionske razmjene i sorpcijskih svojstava IONOVIS-a koriste se sljedeće vrijednosti: puni, dinamički i radni tenk.
Puni tenk(Podijeliti) Određeno brojem funkcionalnih skupina sposobnih za razmjenu iona, u jedinici mase zraka suhe ili natečene ionske i izražena je u mm-ekv / g ili me-ekv / l. To je konstantna vrijednost naznačena u ionatnoj putovnici i ne ovisi o koncentraciji ili prirodi razmjene iona. To se može varirati (smanjiti) zbog toplinskog, kemijskog ili zračenja. U stvarnim uvjetima, s vremenom se smanjuje zbog starenja ionatne matrice, nepovratne apsorpcije pozonskih iona (organskih, željeza, itd.), Koji blokiraju funkcionalne skupine.
Ekspitarni kapacitet ravnoteže (statički) ovisi o koncentraciji iona u vodi, pH i omjeru ionatnih volumena i otopine na mjerenjima. Potrebno provesti izračune tehnoloških procesa.
Dinamički spremnik za razmjenu(Dnevno) - najvažniji pokazatelj procesa obrade vode. U stvarnim uvjetima, višestruko korištenje ionet u ciklusu sorpcije regeneracije, kapacitet razmjene se ne koristi, već samo djelomično.
Stupanj upotrebe određuje se regeneracijom i brzinom protoka regeneracijskog agensa, vrijeme kontakta ionata s vodom i s regenerirajućim sredstvom, koncentracijom soli, dizajna i hidrodinamike korištenog uređaja. Slika pokazuje da je proces pročišćavanja vode zaustavljen u određenoj koncentraciji ograničavajućeg iona, u pravilu, dugo prije punog zasićenja ionet. Broj iona u ovom slučaju apsorbira, što odgovara području pravokutnika A, dodijeljen volumen ionet, i bit će svakodnevno.
Broj apsorbiranih iona koji odgovara potpunoj zasićenju, kada spock je 1, koji odgovara količini iznosa i površine zasjenjene figure iznad S-slične krivulje, naziva se ukupni dinamički kapacitet za razmjenu (PD) , U procesima pročišćavanja vode tipa, obično ne prelazi 0,4-0,7 u.
Sl. jedan
eksperimentalni dio
Reagensi i rješenja:mgCl2 * 6H2O soli u destiliranoj vodi u mjernoj tikvici s kapacitetom od 250 cm
Otopina kalcijevog nitrata (0,02 m) pripravljena je otapanjem uzorka (1,18 g) sali CA (NO3) 2 · 4N20. Nakon otapanja uzorka otopina se razrijedi u destiliranoj vodi u mjernoj tikvici s kapacitetom od 250 cm.
Rješenje 2 kalcijev nitrat (O.1M) je pripravljen otapanjem uzorka (5.09 g.) Soli Ca (NO3) 2 · 4N20. Nakon otapanja uzorka otopina se razrijedi u destiliranoj vodi u mjernoj tikvici s kapacitetom od 250 cm.
Originalna otopina kompleksa Iiipripremljeni od fiksanala. Standardizacija je provedena u skladu s magnezijevim sulfatom.
Pufer rješenja pripremljena iz NH4C1 "Ch.d.a." i NH4OH.
Rezidualna koncentracija Mg2 + iona određena je složenometrijskim s indikatorom erouichroma T.
Rezidualna koncentracija Ca2 + iona određena je kompenmenometrijskim s indikatorom urceksida.
Sorbed koncentracija pronađena je u smislu početnog i rezidualnog.
Kao sorbent koristio je pasmina manifestacije Artyhevskog koji je sadržavao Zeoliti.
Kuhanje sorbent.
CSP Atheshevsky manifestacija drobljenja, prosijan, prikupljenih frakcija granula s veličinom od 1 - 2 - 3 mm i sušena u ormariću za sušenje.
Spremnik za ionsku izmjenu u statičkom načinu rada. Za 20 cm s otopinom koja sadrži Ca2 + iona, u drugom slučaju, mg 2+, s poznatom koncentracijom i
određena pH vrijednost je dodana 5,0 g sorbenta, mućkana tijekom određenog vremena i odvojila je čvrstu fazu filtracijom. U
Selektivnost kelametametrijskog titracije s obzirom na kalcij može se poboljšati određivanjem određivanja u jako alkoholnom mediju (magnezijev filtrat je određen rezidualnom koncentracijom CA2 + iona, u drugom slučaju, Mg2+. Pronađena je koncentracija površine u smislu izvora i preostalog.
Metalni kromistički indikator - mumiesid.
EDTA, 0,05M otopina; Smjesa amonijevog pufera pH \u003d 9; NaOH, 2M otopina; Pokazatelji - EReoichrom Black T i Muriesid - krutina (smjesa s NaCl u smislu 1: 100).
Definicija metodologije
1. Uzorak analizirane otopine prenesena je u titracijsku tikvicu, dodano je 10 cm3 amonijev pufer (pH 9), 25 cm3 destilirane vode, na vrhu lopatice 30 - 40 mg eriohrom crne t i nadmašuje sustav kako bi se potpuno otopio indikator. Rješenje je steklo vino-crveno. Titracija EDTA otopine je izvedena kap po kap iz birete s kontinuiranim miješanjem u boju boje u jasno plavoj boji.
2. Uzorak analizirane otopine prenesen je u titla za titraciju, doda se 5 cm3 2 M otopina NaOH, 30 cm3 destilirane vode i na vrhu lopatice od 30 mgeksida. Otopina je dobila crvenu boju. Titracija je izvedena otopinom EDTA prije prijelaza boje u ljubičastoj boji.
Izračun statističkih uvjeta u odnosu na kalcijeve i magnezijeve ione.
Određivanje kapaciteta za razmjenu magnezija
Za 20 cm3 otopinu magnezijevog klorida s molarnoj koncentraciji ekvivalentnog 0.02 mol / l dodanog i 5,0 s sorbent unaprijed osušena na 105 0 s tijekom 1 sata i trese za određeno vrijeme (0,5 sata). U drugom slučaju, 1 sat i tako dalje. Nakon isteka vremena, otopina je filtrirana. Odveden je za analizu 5 cm3 filtrata, a preostala koncentracija Mg2 + iona određena je sredstvomneonometrijskom metodom.
2. za 20 cm3 otopine kalcijevog klorida s molarnoj koncentraciji ekvivalenta 0, l mol / l dodano 5,0 g sorbent unaprijed osušene na 1050 ° C tijekom 1 sata i trese za određeno vrijeme (0,5 sata). U drugom slučaju, 1 sat i tako dalje. Nakon isteka vremena, otopina je filtrirana. Odveden je za analizu 5 cm3 filtrata, a preostala koncentracija CA2 iona određena je asolesonometrijskom metodom.
Utjecaj vremena kontakta CSP-a i otopine CaCl2 * 4N2O na mjenjačnice CSP u statičkim uvjetima.
(C (ca2 +) ex \u003d 0,1 mol / l; mcsp \u003d 5.0)
Uz povećanje vremena kontakta faza, opaženo je povećanje koncentracije ravnoteže. Nakon 3 sata instalirana je dinamična kotrljačka ravnoteža.
6. Ograničenje valjanosti prekinutog protokola br. 5-94 Međudržavnog vijeća o standardizaciji, mjeriteljstvu i certifikaciji (IUS 11-12-94)
7. izdanje (siječanj 2002.) s izmjenom (ius 3-91)
Ovaj se standard primjenjuje i na ionice i uspostavlja metode za određivanje dinamičkog spremnika s punom ionskom regeneracijom i s danom konzumiranjem agensa za regeneriranje.
Metode se sastoje u određivanju broja iona apsorbiraju se iz radne otopine pomoću jedinice volumena otečenog ionita s kontinuiranim protokom otopine kroz ionitni sloj.
1. Metoda uzorkovanja
1. Metoda uzorkovanja
1.1. Metoda uzorkovanja ukazuje na regulatornu i tehničku dokumentaciju za određene proizvode.
1.2. Za ionite, u kojima je maseni frakcija vlage manji od 30%, uzorak se uzima (100 ± 10). Za oticanje, uzorak se stavlja u čašu s kapacitetom od 600 cm i izlije sa zasićenom otopinom Natrijev klorid, koji treba obložiti viškom da pokrije ionitni sloj s oticanjem. Nakon 5 sati ionisa se ispere destiliranom vodom.
1.3. Za ionite s masovnim frakcijama vlage, više od 30% uzima se uzorak (150 ± 10) g u čašu od 600 cm s kapacitetom i 200 cm destilirane vode se pridržava.
2. Reagensi, otopine, posuđe, uređaji
Voda destilirana prema GOST 6709 ili demineralizira, zadovoljava zahtjeve iz GOST-a 6709.
Barium klorid prema GOST 742, H.CH., otopina s masenim frakcijom od 10%.
Kalcijev 2-voda klorid, H.CH., koncentracijske otopine (SASL \u003d 0,01 mol / DM (0,01 n) i (SASL) \u003d 0.0035 mol / DM (0.0035 n.).
Salonska kiselina prema GOST 3118, H.CH., otopine s masenim frakcijom od 5% i koncentracije (HCl) \u003d 0,5 mol / DM (0,5 n), (HCl) \u003d 0,1 mol / DM (0, 1 N. ) I (NSL) \u003d 0,0035 mol / dm (0.0035 n.).
Sumporna kiselina prema GOST 4204, H.CH., otopine s masenim frakcijom od 1%, koncentracije (HSO) \u003d 0,5 mol / DM (0,5 n).
Natrijev hidroksid prema GOST 4328, H.CH., otopine s masenim frakcijom od 2, 4, 5%, koncentracije (NaOH) \u003d 0,5 mol / DM (0,5 n), (NaOH) \u003d 0,1 mol / DM (0.1 n.), (NaOH) \u003d 0.0035 mol / DM (0.0035 n.).
Natrijev klorid prema GOST 4233, H.C., zasićenoj otopini i otopinu koncentracije (NaCl) \u003d 0,01 mol / DM (0,01 n).
Mješoviti indikator koji se sastoji od metil crvene i metilen plave ili metil crvene i bromon-zelene zelene, pripravljen je prema GOST 4919.1.
Metil narančasta ili metil crvena indikator, otopina s masenim frakcijom od 0,1% se pripravlja prema GOST 4919.1.
Fenolftalein indikator, alkoholna otopina s masenim frakcijom od 1%, priprema prema GOST 4919.1.
Apsorbera kemijska limeta CPI-1 prema GOST 6755 ili vapno je natron.
Cijev (hlorkalcium) prema GOST 25336.
Menzur 1000 prema GOST 1770.
Cilindri prema gosti 1770 nastupi 1-4 s kapacitetom od 100 i 250 cm i performansi 1, 2 s kapacitetom od 500 i 1000 cm.
Naočale u ili n prema GOST 25336 u bilo kojoj izvedbi s kapacitetom od 600 i 1000 cm.
Bočice kn-1-250 prema GOST 25336.
Pipete 2-2-100, 2-2-25, 2-2-20 i 2-2-10 preko NTD.
Burete na NTD vrstama 1, 2, nastupi 1-5, klase točnosti 1, 2, s kapacitetom od 25 ili 50 cm, s cijenom podjele ne više od 0,1 cm i mirise tipova 1, 2, izvršenje 6, točnost Nastava 1, 2, s kapacitetom od 2 ili 5 cm, s cijenom podjele ne više od 0,02 cm.
Mjerni tikvice 1, 2 prema GOST 1770, klase točnosti 1, 2, s kapacitetom od 10, 25 i 100 cm.
Sito s kontrolnom mrežom 0315k prema GOST 6613 sa školjkom s promjerom od 200 mm.
CCC-5000 kup prema GOST 25336 ili iz polimerizacijskog materijala dovoljan za stavljanje sita u nju.
Laboratorij za instalaciju (pogledajte crtež) sastoji se od boce 1 i staklenog stupca s 6 unutarnjeg promjera (25,0 ± 1,0) mm i visine od najmanje 600 mm kako bi se odredio dinamički kapacitet razmjene u uvjetima pune ionske regeneracije i unutarnjeg promjera (16,0 ± 0,5) mm i visina od najmanje 850 mm za određivanje u uvjetima određenog protoka regenerirajućeg sredstva. U donjem dijelu stupca WPIAN filtera 7 od Pora 250 por 250 XC prema GOST 25336 ili drugom uređaju za filtriranje, otporan na kiseline i alkaliju, ne prenosi ionske žitarice od više od 0,25 mm i imaju malu otpornost na filtriranje , Kolona je spojena na bocu sa staklenom cijev 3 i gumenom crijevom 4 s vijčem 5. Da bi se spriječio ugljični dioksid iz zraka iz zraka u otopinu natrijevog hidroksida u cijev za bocu, ugrađen je klorikacijski cijev 2 s HE-1 apsorber.
Laboratorijska instalacija
Dopušteno je koristiti druge mjerne instrumente s mjeriteljskim karakteristikama koje nisu lošije od onih spomenutih, kao i kvalitetnih reagensa koji nisu niži od navedenog.
3. Postupak za određivanje dinamičke razmjene kapaciteta s punom ionskom regeneracijom
3.1. Priprema za test
3.1.1. Priprema za ispitivanje provodi se prema GOST 10896 i nakon treninga ion se pohranjuje u zatvorenoj tikvici ispod sloja destilirane vode.
Katoinitis KU-2-8 HP brand i anion brand ab-17-8Cs na test prema GOST 10896 nisu pripravljeni.
3.1.2. Ionski uzorak iz tikvice u obliku vodene suspenzije se prenosi u cilindar s kapacitetom od 100 cm i brtve sloj ionata dodirom oko krute površine dna cilindra za prestanak skupljanja. Volumen iona je podešen na 100 cm i uz pomoć destilirane vode toleriraju ions u stupac, slijedeći mjehuriće zraka između ionskih granula. Višak vode iz stupca je isušen, ostavljajući 1-2 cm sloj preko ionitne razine.
3.1.3. Ioni u koloni se isperu destiliranom vodom, prolazeći ga od vrha do dna pri brzini od 1,0 dm / h. U isto vrijeme, anilitis se ispere iz alkalija (prema fenolftalenu) i kiselinski kation (prema metil narančastoj).
3.1.4. Vrlo vezivni anioni u hidroksilnom obliku se brzo napućuju i isperu s vodom koja ne sadrži ugljični dioksid.
3.2. Testiranje
3.2.1. Određivanje dinamičkog razmjene kapaciteta ionesa sastoji se od nekoliko ciklusa, od kojih svaki uključuje tri uzastopna operacija - zasićenost, regeneracija, pranje, čiji su uvjeti prikazani u tablici 1.
stol 1
Uvjeti za određivanje dinamičke razmjene kapaciteta s punom ionskom regeneracijom
Indikator | Ionit klasa | Rješenje za zasićenje ionita | Kontrola zasićenja | Regeneracija | |||
zadovoljavajući | praonica | regeneracija |
|||||
Dinamička kapaciteta razmjene za Slippath () | Snažan | Kalcijev klorid (CaCl) \u003d 0,01 mol / dm (0,01 n) | Prije koncentracije kalcijanih iona u filtratu (CA) \u003d 0,05 mmol / DM (0,05 mg · eq / DM) određuje se na GOST 4151 | Klorovodična kiselina, otopina s masenim frakcijom od 5% | |||
Snažan | Natrijev klorid (NaCl) \u003d 0,01 mol / dm (0,01 n) | Prije smanjenja koncentracije alkalija 0,5 mmol / DM (0,5 mg · ekv / dm) u usporedbi s maksimalnom stabilnom vrijednošću u filtratu [mješoviti indikator, naslovna otopina, koncentracijska klorovodična kiselina (HCl) \u003d 0,01 mol / dm (0.01 n.)] I prije povećanja sadržaja klora iona u usporedbi s njezinim održivim sadržajem u filtratu (definiran prema GOST 15615) | Natrijev hidroksid, otopina s masenom frakcijom od 5% | ||||
Slabo | Prije pojavljivanja u filtratu kiselina (metil narančastom) | ||||||
Kompletan dinamički kapacitet razmjene () | Slabo | Salonska kiselina (HCl) \u003d 0,1 mol / dm (0,1 n) | Prije izjednačavanja koncentracije filtrata s koncentracijom radne otopine | Natrijev hidroksid, otopina s masenim frakcijom od 2% | |||
Bilješke:
1. Prilikom određivanja koncentracije CA iona prema GOST 4151
2. Specifično opterećenje je volumen otopine prolazi kroz ionet volumen na 1 sat. Na primjer, 5 DM / DM · h odgovara brzini filtracije na kojoj je 100 cm otopine (8,3 cm / min) nakon 100 cm ionita.
3. Brzina filtriranja je podešena za mjerenje u mjernom cilindru volumena filtrata dobivenog tijekom određenog vremenskog intervala.
Rješenja i voda se hrane od vrha do dna. Kada uživate u anonita brandovima AN-1 i AN-2FN rješenja se smanjuju odozdo.
3.2.2 Prije provođenja zasićenosti, regeneracije i operacija pranja, kolona je ispunjena odgovarajućom otopinom. Otopinski sloj preko iona treba biti (15 ± 3) cm.
3.2.3. Nakon zasićenja, regeneracije i pranja u koloni iznad iona, ostavite sloj tekućine s visinom od 1-2 cm.
3.2.4. Ionski stupac je ispunjen radnom otopinom za određenu klasu jonita (vidi tablicu 1) tako da je sloj otopine preko iona (15 ± 3) cm i odaberite odgovarajuću brzinu filtracije.
Kada se koncentracija 0,1 mol / DM propušta kroz kolonu s ionom (0,1 n), filtrat se sakupi u cilindrima kapaciteta od 250 cm, pri koncentraciji od 0,01 mol / DM (0,01 n) - u cilindri s kapacitetom 1000 cm. U drugom i naknadnom ciklusima zasićenja prije pojave radne otopine iona u filtratu (određeno nakon prvog ciklusa), filtrat se sakupi porcijama od 100 i 250 cm u skladu s koncentracijama radno rješenje.
3.2.5. Iz svakog dijela filtrata, uzorak se uzima i kontrolira zasićenost u skladu sa tablicom 1.
3.2.6. Nakon pojavljivanja u dijelu filtrata, ioni radnog rješenja izračunavaju ukupni volumen filtrata.
3.2.7. Da bi se utvrdilo potpuni dinamički kapacitet razmjene, otopina se nastavlja poravnati koncentraciju filtrata s koncentracijom radne otopine. Kontrola zasićenja u ovom slučaju provodi se titracijom uzorka s otopinom kiseline (natrijev hidroksid) s mješovitim indikatorom prije promjene boje.
3.2.8. Prije izvođenja regeneracije, ionite u koloni eksplodiraju struju destilirane vode iz dna prema gore tako da su sve ionske žitarice u pokretu. Eksplozija KU-1 marke Catiaia i aniona brandova AN-1 i AN-2FN provode se prije operacije zasićenja.
3.2.9. Ionska regeneracija se provodi s otopinom kiseline (natrijev hidroksid) po brzini navedenoj u tablici 1. Filtrat se kontinuirano sastavlja cilindrom s cilindrom s volumenom od 250-1000 cm, dodajući 3-4 kapi indikatora. Kada se pojavi kiselina (natrijev hidroksid), njegova koncentracija se određuje u filtratu u slijedećim obrocima. Za kontrolu filtrata, uzorak se uzima s pipetom ili mjerljivim tikvicom i titrira s otopinom koncentracije kiseline (natrijevog hidroksida) (HSl, HSO) \u003d 0,5 mol / DM (0,5 N.), (NaOH) \u003d 0,5 mol / DM (0, 5 n.) U prisutnosti indikatora
3.2.10. Otopina kiseline (natrijev hidroksid) je došlo do izjednačavanja koncentracije filtrata s koncentracijom otopine za regeneraciju.
3.2.11. Ionis nakon regeneracije se ispere destiliranom vodom u neutralnu reakciju prema metil narančastoj (fenolftalen) pri brzini navedenoj u tablici 1. Zatim se ion drži u destiliranoj vodi 1 sat i ponovno se provjerava filtrat. Ako filtrat nema neutralnu reakciju, ion se ponovno ispere.
3.2.12. Definicija dinamičkog razmjene je potpuna ako su posljednji ciklusi dobiveni rezultati, odstupanje između kojih ne prelazi 5% prosječnog rezultata.
3.2.13. Dinamička razmjena kapaciteta aniona AB-17-8CC određuje se s dva paralelna uzorka na prvom ciklusu zasićenja, prije pojave iona radne otopine u filtratu. Filtrat se prikuplja dijelovima od 250 cm. Za rezultat, prosječni aritmetički rezultati dvije definicije, dopuštena odstupanja između koja ne prelazi 5% prosječnog rezultata.
(Amandman, IUS 3-91).
4. Postupak za određivanje dinamičkih kontejnera za izmjenu s danom konzumiranjem potrošnje
4.1. Priprema za test
4.1.1. Ionis, odabran u skladu s patentnim zahtjevima 12 i 1.3, odvoji se od malih frakcija metodom mokre rezolucije prema GOST 10900, koristeći sito s grid n 0315k.
4.1.2. Odvojeni anionit se stavlja u staklo, 500 cm otopine natrijevog hidroksida s masenom frakcijom od 4% se miješa i miješa. Nakon 4 h, otopina hidroksida je isušena, a anion se ispere s vodom u lagano alkalnu reakciju prema fenolftalenu i prenese se u kolonu, kao što je naznačeno u klauzuli 3.1.2.
4.1.3. Odvojeni kation se ispere iz suspenzije i razbode s destiliranom vodom s dekantiranjem prije pojave lagane vode i prenese se u kolonu u skladu s odredbom 3.1.2.
4.2. Testiranje
4.2.1. Određivanje dinamičke izmjene ionita prije pojave radne otopine iona u filtratu () sastoji se od nekoliko ciklusa, od kojih svaki uključuje tri uzastopna operacija - zasićenost, regeneracija, pranje, čiji su uvjeti prikazani u tablici 2. Rješenja i voda se hrane od vrha do dna. Visina tekućeg sloja iznad ionetske razine postavljen je kako je navedeno u PP.3.2.2 i 3.2.3.
tablica 2
Uvjeti za određivanje dinamičkog kapaciteta iona u određenoj potrošnji regeneracije
Ionit klasa | Regeneracija | Specifična vrijednost stopa regenerirana | Kontrola pranja | IONITE otopina zasićenja | Kontrola zasićenja | Brzina filtracije |
||
nASA | jebeni | registrira |
||||||
Snažan | Na preostalu koncentraciju kiseline u filtratu više | Kalcij klorid (SASL \u003d 0.0035 mol / DM (0.0035 n.) | Prije koncentracije kalcijevih iona u filtratu više (CA) \u003d 0,05 mmol / DM | |||||
Slabo | Sumporna kiselina, otopina s masenim frakcijom od 1% | Do odsutnosti u sulfacijskom filtratu (uzorak s bacll u prisutnosti HCl) | Natrijev hidroksid (NaOH) \u003d 0.0035 mol / DM (0.0035 n.) | Do koncentracije u filtratu natrijevog hidroksida (NaOH) \u003d 0,1 mmol / DM | ||||
Snažan | Natrijev hidroksid s masenim frakcijom od 4% | Na preostalu koncentraciju natrijevog hidroksida u filtratu br. (NaOH) \u003d 0,2 mmol / DM | Natrijev klorid (NaCl) \u003d 0,01 mol / DM (0,01 n) | Prije smanjenja koncentracije alkalija na (NaOH) \u003d 0,7 mmol / DM | ||||
Slabo | Natrijev hidroksid, otopina s masenom frakcijom od 4% | Na preostalu koncentraciju natrijevog hidroksida u filtratu ne više (NaOH) \u003d 0,2 mmol / DM (0,2 mg · eq / DM) preko fenolftalena | Sol (sumporna) kiselina (HSl, HSO) \u003d 0.0035 mol / DM (0.0035 n.) | Do preostale koncentracije kiseline u filtratu nije više (H) \u003d 0.1 mmol / DM (0,1 mg · ekv / DM), indikator se miješa, naslovna otopina - koncentracija natrijevog hidroksida (NaOH) \u003d 0,01 mol / dm (0, 01 n.) | ||||
Bilješke:
1. Pri izrazivanju norme specifične brzine protoka regenerirajućeg sredstva () u gramima na krticu ispod riječi "mol" znači molarna masa ekvivalenta iona (Na, K, CA, mg, Cl, NSO, NSO, NSO, NSO, NSO, NSO, NSO, NSO, HSO, CO, tako
Itd.).
2. Stvarna brzina protoka regeneracijskog agensa ne bi se trebala razlikovati od navedene norme za više od 5%.
3. Prilikom određivanja koncentracije ione prema GOST 4151, upotreba 2-3 kapi indikatora kroma-tamno plave i titracije koncentracije trilone-B (NaHCon · 2HO) \u003d 0.01 mol / DM (0.01
4. Specifično opterećenje je volumen otopine prolazi kroz volumen ionisa na 1 sat. Na primjer, 5 DM / DM · h odgovara brzini filtracije na kojoj je 100 cm otopine (8,3 cm / min) nakon 100 cm ionita.
5. Brzina filtracija postavljena je za mjerenje u mjernom cilindru filtrata dobivenog tijekom određenog vremenskog intervala.
Kako bi se izbjeglo oštećenje katicitisa, regeneracija kiseline i pranje iz regeneracijskih proizvoda provodi se bez zaustavljanja, ne dopuštajući jaz između operacija.
Prije obavljanja svakog sljedećeg ciklusa, ion se shyling protok vode iz donjeg prema gore, tako da su sve ionske žitarice u pokretu.
4.2.2. Kroz ions u stupcu, prolazi se regenerirajuća otopina, čiji je volumen () u kubičnim centimetrama izračunat formulom
gdje je određena vrijednost specifične brzine protoka regenerirajućeg sredstva, g / mol (g / g · eq);
- dinamički tenk; Odaberite prema regulatornoj i tehničkoj dokumentaciji o specifičnom ionima, mol / m (r · eq / m); Za iionice, AB-17-8, AN-31 i EDE-10P razreda su dopušteni za prvu regeneraciju povećanu vrijednost dinamičke razmjene na 3;
- Uzorci ionita, cm;
- koncentracija regenerirajućeg morta, g / dm.
Količina otopine regeneracije mjeri se na izlazu kolone s cilindrom ili benzurom. Zatim je stupac prekinut, razina otopine preko iona u koloni se spušta na 1-2 cm i zatvorena niža za
4.2.3. Ioni su nakon regeneracije isprane destiliranom vodom iz viška kiseline (natrijev hidroksid) brzinom navedenom u tablici 2.
Povremeno odaberite uzorak filtrata i titrira koncentraciju natrijevog hidroksida (kiselina) (NaOH, HCl, HSO) \u003d 0,1 mol / DM (0,1 n) u prisutnosti metilne narančine (fenolftalena).
Pranje se kontrolira tablicom 2.
4.2.4. Nakon pranja, kolona je ispunjena rotorom i postavite brzinu zasićenja iz tablice 2.
Prilikom rada u stupcu radnih otopina koncentracija 0,01 mol / DM (0,01 n), filtrat se sakupi u cilindar s kapacitetom od 250 cm, u koncentraciji od 0,0035 mol / DM (0.0035 n.) Koristite cilindar s a Kapacitet od 1000 cm. Drugi i naknadni ciklusi zasićenja prije pojave radnog mort iona u filtratu (određeni nakon prvog ciklusa), filtrat se sakupi za 100 i 250 cm, odnosno koncentracije radne otopine.
4.2.5. Za kontrolu zasićenosti iz dijela filtrata, uzorak se uzima i analizira u skladu sa tablicom 2. Ako rezultat analize pokazuje da razina zasićenja nije dosegla vrijednosti navedene u tablici 2, svi prethodni uzorci filtrata ne mogu se analizirati.
4.2.6. Nakon pojavljivanja u dijelu filtrata radne otopine iona u količinama navedenim u tablici 2, zasićenost je potpuna i izračunata ukupni filtrat () i kontejner dinamičke izmjene.
4.2.7. Ion je podvrgnut drugoj regeneraciji i oprao u skladu sa stavkom 4.2.2 i 4.2.3.
Prilikom izračunavanja sredstva za regeneraciju potreban za drugi ciklus, vrijednost dinamičkog kontejnera za razmjenu dobivenih u prvom ciklusu u skladu s odredbom 4.2.6 se koristi u skladu s odredbom 4.2.6.
Prije obavljanja naknadnih ciklusa zasićenja, konzumiranje potrošnje potrošnje izračunava se veličinom dinamičkog razvodnog kapaciteta dobivenog u prethodnom ciklusu.
4.2.8. Kraj definicija ako su posljednji ciklusi dobiveni rezultati dopušteni odstupanjima između kojih ne prelaze 5% prosječnog rezultata, uz stvarni specifičnu brzinu protoka regenerirajućeg sredstva, razlikuju se od navedene norme ne više od 5%.
5. Rezultati obrade
5.1. Dinamička razmjena kapaciteta () u kubičnom metru (r · eq / m) dok se ionska otopina ne pojave u filtratu izračunavaju se formulom
gdje - ukupni volumen filtrata prolazi kroz ions prije pojave iona radnog rješenja, vidi;
- Volumen ionet, vidi
5.2. Stvarna brzina protoka regenerirajućeg sredstva () u gramima po molu (g / g eq) apsorbiranih iona izračunava se pomoću formule
gdje je volumen regenerirajućeg morta, vidi;
- koncentracija otopine regeneracije, g / dm;
- ukupna količina filtrata prolazi kroz ions dok se ne pojavi ione radnog rješenja, vidi;
- Koncentracija radnog otopina, MOL / DM (n.
5.3. Kompletna dinamička kapaciteta razmjene () u molovima po kubičnom metru (r · ekv / m) izračunavaju se formulom
gdje - ukupna količina filtrata prolazi kroz ions za izjednačavanje koncentracija filtrata i radne otopine, cm;
- koncentracija radnog otopina, MOL / DM (n.);
- volumen dijela filtrata nakon pojave iona radnog rješenja (Skip), cm;
- koncentracija otopine u dijelovima filtrata nakon pojave iona radne otopine (SKIP), MOL / DM (n);
- ionet volumen,
5.4. Rezultat definicije, prosječni aritmetički rezultati dvaju ciklusa se uzimaju, odstupanja između koje ne prelaze ± 5%, s pouzdanom vjerojatnošću \u003d 0,95.
Bilješka. Kada izražavate dinamičke razmjene kapaciteta ionija u kubičnom metru ispod riječi "mol", postoji molarna masa ekvivalenta iona (Na, K, CA, mg, Cl, ne, NSO, HSO, CO, tako itd. ).
Tekst dokumenta je izbušen po:
službeno izdanje
Ionite. Metode određivanja
exchange Kapacitet: Sat. Gostov. -
M.: IPK izdavaštvo standarda, 2002
Opći pojmovi
Općim riječima, pod kapacitetom smole ionske izmjene, shvaća se kao broj iona, koji se mogu apsorbirati određenom količinom smole. Štoviše, jedinica mjerenja kapacitivnosti smola može biti različita. Na primjer, mm-ekv / ml (meq / ml), g. (EQ / L) ili kilogravan na kubičnom stopalu (Kgr / FT3). Znajući ekvivalentnu masu materije, možete izračunati spremnik smole. Ekvivalentna masa tvari definirana je kao omjer molarne mase tvari u njegovoj valenciji (strogo govoreći, na broj ekvivalentnosti tvari). Na primjer, masa kalcijevog molara je 40 g. / Mol, i valent 2, zatim ekvivalentna masa je jednaka 20 g. / Mol (40/2 \u003d 20). Smola ionske izmjene s kapacitetom razmjene od 1,95 g - eq / l je u stanju ukloniti 1,95 h 20 \u003d 39 grama iz otopine na 1 litru smole.
U praksi, kapacitet razmjene smole određuje se u titracijskim laboratorijima. Kroz kolonu u kojem se nalazi soda u obliku vodika (H-form), se nalazi, otopina natrijevog hidroksida (NaOH). Dio na + iona se mijenja za vodikove ione. Natrijev hidroksid, koji nije ulazio u reakciju s ionskom skupinom smole, čisti se s kiselinom. Od početne koncentracije natrijevog hidroksida, preostalu koncentraciju može se odrediti kationskim spremnikom. Drugi način određivanja razmjene kapaciteta iona prolazi kroz sloj smole otopine kalcijevog klorida. Slično tome, određuje se spremnik anionske izmjene smole (u obliku OH), kroz koji se prolazi kiselina otopina.
Kapacitet smole može se mjeriti u mm-ekv / ml (volumenu) ili mg-eq / g (težina). Ako je kontejner eksprimiran u mm-ekv / g definiran (i masa suhog iona je namijenjena), onda, znajući vlažnost smole, lako je otići u mm-ekv / ml.
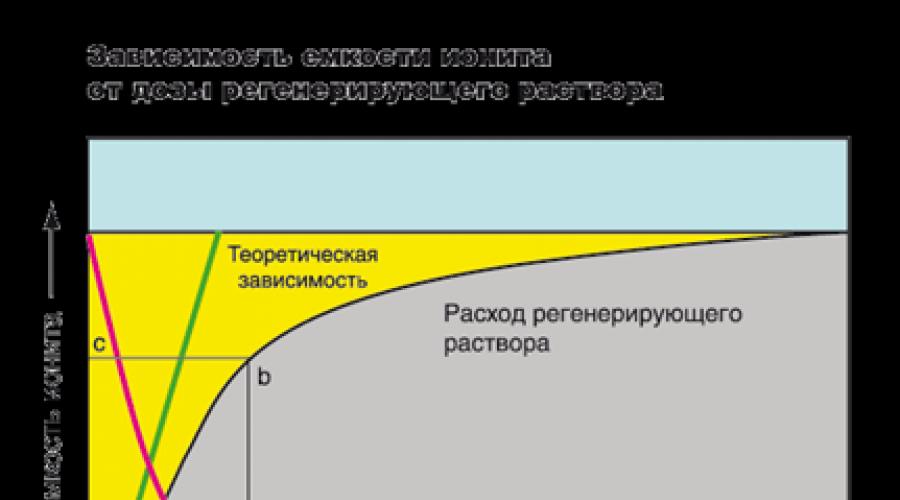
Na slici, kapacitet razmjene smole grafički je prikazan s područjem žute boje između okomitog ravnog i Cl. Područje sive, smješteno ispod krivulje, je koncentracija iona u pročišćenoj vodi. Na početku ciklusa, koncentracija iona u filtratu je vrlo mala i ostaje konstantna u cijelom filteru, u trenutku kada front filtriranje dosegne kraj iona sloja, ioni se javljaju na filtrat (u Slika - točka p). Ovo je signal regeneracije smola. Obično se regeneracija filtra provodi na slippath. Na primjer, u industriji, koncentracija rigističkih iona u kojima je filtar izveden za regeneraciju može doseći vrijednost manju od 0,05 03, au kućnim sustavima za omekšavanje - manje od 0,5 0. X - duljina segmenta odgovara volumenu pročišćene vode u litarima ili galonima. ANLB Slika je potpuna apsorpcija iona smole, a područje ANMB lik je broj apsorbiranih iona do pojave priboda.
Govoreći o spremniku, često mislimo radi upravo upravo radi, a ne potpuni kontejner za razmjenu. Radni kapacitet nije trajna vrijednost, ovisi o skupu čimbenika: brand ionita, koncentracije i vrste apsorbiranih iona, pH otopine, na zahtjeve pročišćene vode, brzine protoka, visine ionitnog sloja i drugih zahtjeva.

Postizanje visokog stupnja ekstrakcije iona iz vodene otopine zahtijeva povećanje doze regenerirajuće otopine (crvene linije). Međutim, povećanje koncentracije otopine regeneracije je beskrajno nemoguće (zelena linija je teoretska ovisnost između stupnja smanjenja kapacitivnosti smole i brzine protoka otopine regeneracije). U praksi, kako bi se postigao veliki kapacitet, potrebno je povećati broj smola. S prvom filtrociklom, stupanj smanjenja ionskih razmjenskih svojstava može doseći 100%, ali s vremenom će se ta vrijednost smanjiti. Na primjer. Većina proizvođača sustava za omekšavanje vode preporučuje se upotreba otopine NaCl s koncentracijom od 100-125 g. / L za vraćanje kapaciteta kationa do 50 - 55% ukupnog kontejnera za izmjenu vode.
Prilikom određivanja spremnika potrebno je znati ionski oblik smole (sol, kiselina, glavna). S regeneracijom ili u procesu rada, volumen se mijenja pumpe, proces koji se naziva "disanje". Tablica pokazuje kako se smole ponašaju u različitim procesima.
Razlikovati kation i anionske. Reakcije u kojima su ioni uključeni u stol.
ionska reakcijska reakcija reakcije

Štoviše, u literaturi na engleskom jeziku, sac simbol ukazuje na snažno kisele kation, SBA je vrlo koristan anion, WAC je slabo kiseli kation, a WBA je slabo prijateljski anion. Sposobnost ionske razmjene određena je prisutnošću funkcionalne skupine, snažno kisele kacijete sadrže sulfo skupinu - SO3H, i slabo kiselina kiselina kationa karboksilne skupine - COOH. Snažno kisele kacijete zamijenjene su kationima u bilo kojoj pH vrijednosti, tj. Ponašaju se kao jake kiseline u otopini. Slabo kiselina kiselina je slična slabim kiselinama i reakciju ionske izmjene samo na pH vrijednosti iznad 7. Anionske sadrže funkcionalne skupine od pet vrsta: (-NH2, NH \u003d, N (CH3) 3OH, - N (CH3) 3OH, - N (CH3) 3OH, - N (CH3) 2OH4OH). Prve tri skupine daju anion slabo prijateljskih svojstava, a skupine - N (CH3) 3OH, -N (CH3) 2C2H4OH - snažno rudarstvo. Slabo-prijateljski anioni reagiraju s anionima jakih kiselina (tako, CL-, ne) i visoko vezanja s anioni jake i slabe (HCO, HSIO) u pH raspon od 1 do 14. Govoreći o spremniku visoko veznog Anion, trebali biste obratiti pozornost na to u smolju postoje funkcionalne skupine svojstvene i loše prijateljske anionske. Kada starenje visoko vezanja aniona ili pod djelovanjem visokih temperatura, postoji smanjenje osnovnog i djelomičnog uništenja funkcionalnih skupina.
Razmotrite više reakcija koje curi uz sudjelovanje ionske izmjene smole. Reakcija 1 - Omekšavanje vode na snažno kiselom kation soli (Na) obliku, 2 - uklanjanje nitratnih iona na visoko vezujući anion u Cl-formu. Aplikacija kao regenerirajuća otopina natrijevog klorida i kalijevog klorida doprinosi široko rasprostranjenoj upotrebi ove vrste smole u svakodnevnom životu, industriji i obradi otpadnih voda. Kations se također može obnoviti kiselim otopinama (na primjer, klorovodična kiselina) i anioni - otopina kaustične sode (NaOH). Ionite u H i OH-obliku koriste se u shemama za pripravu desalidne vode (reakcija 3 i 4). Slabo kisela kationa označena je svojstvima ionske izmjene pri visokim pH vrijednostima (reakcija 5) i slabo-osi anilij - pri niskim pH vrijednostima (reakcija 6). Reakcija 5 je istovremena omekšavanje i smanjena alkalnošću vode. Treba napomenuti da je WBA smola kao posljedica regeneracije s alkalnom otopinom ne prenosi u OH obliku, već takozvani FB forme (slobodna baza).
Slabo kisele kation u usporedbi s jakim kiselinama imaju veći kapacitet razmjene, oni karakterizira veliki afinitet za vodikove ione, tako da regeneracijski prihodi lakše i brže. Važno je da se za regeneraciju WAC-a, kao i WBA ne koriste otopine natrijevog klorida ili kalija. Izbor jedne ili druge marke smole ionske izmjene ovisi o mnogim uvjetima. Na primjer, razlikuju se dvije vrste visoko rudarskih anionskih anionskih: tip I (funkcionalna skupina - N (CH3) 3OH) i tip II (-N (CH3) 2C2H4H). Anioni tipa i bolja apsorbiraju HSIO ione, za razliku od anionskih tipa II, ali potonji se karakterizira većim razmjenom i bolje regenerira.
U zaključku, napominjemo da je u literaturi, kao iu putovnici na proizvodima, naznačena je ukupna težina i mjenjačni spremnik smole, koji su definirani u laboratoriju. Radni kapacitet smole je niža od proglašenja proizvođača i ovisi o mnogim čimbenicima koji se ne mogu uzeti u obzir u laboratorijskim uvjetima (geometrijske karakteristike sloja smole, specifične procesne uvjete: brzine streaming, koncentracija otopljenih tvari, stupanj regeneracije, stupanj regeneracije, stupanj regeneracije , itd.).
Materijali vion koriste se za čišćenje emisija ventilacijskih otpadnih plinova iz topljivih komponenti, aerosola kiselina i soli teških metala, gdje se koriste uglavnom u obliku netkanih penjačkih platna igle.
Napredak:
Težio je 2 gr. Kation Vion Kn-1 (suho). Ulijte u štednju. Premjestite originalni CUCl 2 (3.6 mmol / L) kroz kolonu napunjenu katitom. Zatim, mirimo uzorak za 50 ml titracije. Na temelju metodologije (stavak 3.1) određujemo optičku gustoću uzorka i pronađite koncentraciju bakra. Rezultati su prikazani u tablici 3.5.
Tablica 3.5
|
C, mmol / l |
||||
Oni su izgradili grafikon ovisnosti koncentracije bakra u filtratu iz volumena otopine prolazi kroz ionet.
Sl. 3.4.
Proces sorpcije je u potpunosti apsorbirati prve postrojenje kationa, a apsorpcijsko područje postupno se kreće duž stupca do izlaza. Nakon toga, trenutak se događa kada, zbog iscrpljenosti spremnika za kation, kationi počinju izaći iz kolone. Iz grafikona se može vidjeti da se koncentracija bakra na izlazu kolone postupno povećava i ima oblik krivulje u obliku oblika, u rasponu od nulte koncentracije do maksimuma. Ova krivulja rasteže se malim koncentracijama soli.
Izračunava količina bakra, koja je apsorbiranu kolonu u ukupnu zasićenost kationa, kao područje slike, ograničena krivulja u obliku oblika i izravna maksimalna koncentracija:
h \u003d? VI * (cmax - CI) (3)
gdje VI \u003d 50 ml,
Cmax \u003d 3,6mmmol
h1 \u003d 2,20 mmol.
Izračunati volumetrijski spremnik kationa:
z1 \u003d H1 / M k \u003d 2,20 / 2 \u003d 1.10 mmol / gr. Kationta.
Rasprava o rezultatima
Tijekom eksperimentalnog rada utvrđena je ukupna razmjena od tri različita kation (KU-2-8, KU-1, VION KN-1). Rezultati su prikazani na slici 3.5.

Ukupni tenk kationa je proporcionalan na području slici, ograničenom oblikovanom krivuljom i izravnom maksimalnom koncentracijom. Kao što se može vidjeti sa slike 3.5. Spremnici različitih i igalisa su različiti i manji od potpunog kapaciteta razmjene kationa navedenih u putovnici. Dakle, potpuni kapacitet za razmjenu KU-2-8 kationa se nalazi eksperimentalno ispod vrijednosti putovnice za 28%, potpuni kapacitet razmjene KU-1 manji je od vrijednosti putovnice za 57% i kation VION KN-1 je 39%. Ti se podaci moraju uzeti u obzir pri izračunavanju i projektiranju aparata i filtera za ionsku razmjenu.
Ionska razmjena odvija se o tim adsorbensima koji su polielektroliti (ionski izmjenjivači, ioni, ionske izmjenjivačke smole).
Ionska razmjenaekvivalentan proces razmjene ionizacije u ionskom izmjenjivaču naziva se ions istog znaka u otopini. Proces ionske razmjene je reverzibilan.
Ioni su podijeljeni u kation, aniona i amfoterične ionite.
Katici- tvari koje sadrže fiksne negativno napunjene skupine u njihovoj strukturi (fiksni ioni), koje se kreću kretanje (protuioni), koje se mogu razmjenjivati \u200b\u200bs kationi u otopini (sl. 81).
Sl. 81. Model polielektrolijskog matrice (kationa) s fiksnim aniona i pomicanja, gdje - fiksni ioni;
- Kooines, - savjetovanja
Prirodne kation: Zeolitis, persolitis, silika gel, celuloza, kao i umjetna: visoke molekularne težine kruti netopljivi ionski polimeri koji sadrže najčešće sulf skupine, karboksilu, fosfin-kiselinu, arsenske kiseline ili selenijskih skupina. Sintetički anorganski kationi koji se najčešće koriste aluminozitici.
Prema stupnju ionizacije ionskih skupina, kationi su podijeljeni u tešku kiselinu i slabost. Snažno kisele kacijete su sposobne za razmjenu svojih mobilnih kationa na vanjskim kationama u alkalnim, neutralnim i kiselim okruženjima. Slabo kiselinski kation razmjenjuje protuobićima na drugim kationima samo u alkalnom okruženju. Snažno kiseli su kation s jako disociranim kiselim skupinama - sulfonska kiselina. Slabo kiselina uključuje kation koji sadrži slabo kisele kiseline skupine - fosfornu kiselinu, karboksil, oksifenil.
Aniooni- Ionski izmjenjivači koji sadrže pozitivno nabijene ionske skupine u njihovoj strukturi (fiksni ioni), koji se krećuju anioni (protuioni), koji mogu razmjenjivati \u200b\u200bs anionima koji su u otopini (sl. 82). Razlikovati prirodne i sintetičke anionske.

Sl. 82. Model polielectrolyte matrice (anion) s fiksnim kationima i pomicanja, gdje + su fiksirani ioni;
- Kooines, - savjetovanja
Sintetski anionis sadrže pozitivno nabijene ionske skupine u makromolekulama. Slaboze - domaće anionske su u njihovom sastavu osnovne, sekundarne i tercijarne amino skupine, visoko vezani anioni sadrže skupine kvarternih soli i baza (amonij, piridinij, sulfonij, fosfonij). Visoko obvezujući anioni razmjenjuju se u kiselim, neutralnim i alkalnim medijima, slabo-os - samo u kiselom okruženju.
Amfoterijske ionitesadrže i kationske i anionske ionske skupine. Ovi ioni mogu sorbiti i kationi i anioni.
Kvantitativna karakteristika iona je puni tenk(Po). Određivanje se može provesti statičkom ili dinamičkom metodom na temelju reakcija koje teče u sustavu ionbitskog sustava:
RSO 3 - H + + NaOH → RSO 3 - Na + + H20
RNH3 + OH - + HCl → RNH3 + Cl - + H20
Kapacitet se određuje brojem ionskih skupina u ionatu i stoga teoretski mora postojati konstantna vrijednost. Međutim, to praktično ovisi o nizu uvjeta. Postoje statični spremnici za razmjenu (SEO) i dinamički kapacitet razmjene (Dee). Statični kapacitet razmjene je kompletan kontejner koji karakterizira ukupan broj ionskih skupina (u Milciecquentivalenti) po jedinici mase zraka suhog iona ili NA jedinice količine otečenog ionisa. Prirodni ionite imaju mali statički metabolički kapacitet, a ne prelazi 0,2-0,3 mEKV / g. Za sintetičke ionske izmjene smole, ona je unutar 3-5 mVv / g, a ponekad i doseže 10,0 meq / g.
Dinamički ili radni, razmjeni kapacitet primjenjuje se samo na dio Iongepps, koji su uključeni u ionsku razmjenu koja se javlja u tehnološkim uvjetima, na primjer, u stupcu za ionsku izmjenu na određenoj relativnoj brzini ionita i otopine. Dinamički kapacitet ovisi o brzini kretanja, veličini stupca i drugim čimbenicima i uvijek je manji od statičkog metaboličkog kapaciteta.
Da biste odredili statični spremnik ioni, koriste se različiti postupci. Sve ove metode su svedene na zasićenost ionet bilo kojim ionom, a zatim ga prevrtanjem s drugim ionom i analizom prve otopine. Na primjer, katij se prikladno prevede u H +-oblik (protuioni su vodikov ione), zatim isperite otopinom natrijevog klorida i rezultirajuća kisela otopina se ukloni s alkalijskim otopinom. Kapacitet je jednak omjeru količine kiseline koja je prošla u otopinu kiseline do raspoloženja ionskog.
S statičkom metodom, kiselina ili alkalija se titrira, koja kao posljedica adsorpcije ionske izmjene pojavljuje se u otopini.
U dinamičkoj metodi, to se određuje kromatografskim stupovima. Kroz kolonu napunjenu s ionskom izmjenom sela, otopina elektrolita prolazi i ovisnost koncentracije apsorbiranog iona u zastarjeli otopini (eluau) se bilježi od volumena prošle otopine (izlazna krivulja). Poze izračunate formulom
 , ,
| (337) |
gdje Vlan Ukupno - ukupni volumen koji sadrži kiselinu koja se isporučuje od smole; iz - koncentraciju kiseline u ovoj otopini; m. - masa smole ionske izmjene u stupcu.
Konstanta za razmjenu ravnoteže može se odrediti iz podataka o ravnotežnoj raspodjeli iona u statičkim uvjetima (ravnotežno stanje ionske izmjene opisan je zakonom mase), kao i dinamička metoda za brzinu premještanja zone supstanca duž sloja smole (eluensna kromatografija).
Za reakciju ionske izmjene
![]()
konstanta ravnoteže je jednaka
 , ,
| (338) |
gdje, - koncentracija iona u ionetu; - koncentracija iona u otopini.
Primjena ionike, možete omekšati vodu ili desalinirati slanu vodu i dobiti prikladne za farmaceutske svrhe. Još jedna upotreba adsorpcije ionskog razmjene u farmaciji je da ga koristi u analitičke svrhe kao metoda za ekstrakciju iz smjese jedne ili druge komponente koja se analizira.
Primjeri rješavanja problema
1. U 60 ml otopine s koncentracijom neke tvari, 0,440 mol / l postavljenog aktiviranog ugljika težine 3 g. Otopina s adsorbentom je mućka da se uspostavi adsorpcijska ravnoteža, kao rezultat kojih se koncentracija tvari smanjila na 0,350 mol / l. Izračunajte adsorpcijsku vrijednost i stupanj adsorpcije.
Odluka:
Adsorpcija se izračunava formulom (325):

Po formuli (326) odredite stupanj adsorpcije
2. Prema danim podacima, za adsorpciju dimendrola na površini ugljena izračunajte grafički konstante langlemurne jednadžbe:
Izračunajte adsorpciju dimedola u koncentraciji od 3,8 mol / l.
Odluka:
Grafički odrediti konstante langmuir jednadžbe, koristimo linearni oblik ove jednadžbe (327):
Izračunati 1 / ali i 1 / iz:
Izgraditi raspored u koordinatama 1 / ali – 1/iz(Sl. 83).
Sl. 83. Grafička definicija konstanti langlemurske jednadžbe
U slučaju kada je točka h.\u003d 0 se nalazi izvan crteža, koristite drugi način y \u003d ax + b, Prvo, odaberite dvije osobe koje leže na ravnom (sl. 83) i odredite njihove koordinate:
(·) 1 (0.15; 1,11); (·) 2 (0.30; 1.25).

b \u003d y 1 - sjekira 1 \u003d0.11 - 0.93 · 0.15 \u003d 0.029.
Dobivamo to b. = 1/ali ¥ \u003d 0,029 μmol / m2, stoga ali ¥ \u003d 34,48 μmol / m 2.
Stalna ravnoteža adsorpcije K.određuje se kako slijedi:
Izračunajte adsorpciju diprolola u koncentraciji od 3,8 mol / l pomoću langmuir jednadžbe (327):
3. Prilikom studiranja adsorpcije benzojeve kiseline na krutom adsorbentu, dobiveni sljedeći podaci:
Odluka:
Da bi se izračunali konstante Freundlich jednadžbe, potrebno je koristiti linearni oblik jednadžbe (332), u koordinatama LG ( x / t.) – lG. iz Izotermarni ima vrstu izravnog.
Pronađite vrijednosti LG c. i lg. x / M.uključena u jednadžbu linearizirane Freundlich.

| LG. c. | –2,22 | –1,6 | –1,275 | –0,928 |
| LG. x / M. | –0,356 | –0,11 | 0,017 | 0,158 |
Izgraditi raspored u koordinatama LG ( x / t.) – lG. iz(Sl. 84) .
Sl. 84. Grafička definicija konstanti Freundlich jednadžbe
Od točke h.\u003d 0 nalazi se izvan slike (84), koristimo drugi način Definicija koeficijenata izravno y \u003d ax + b(Vidi "Uvodni blok. Osnove matematičke obrade eksperimentalnih podataka"). Prvo, odaberite dvije točke koje leže na ravnoj liniji (na primjer, točke 1 i 2) i odredite njihove koordinate:
(·) 1 (-2.0; -0.28); (·) 2 (-1.0; 0.14).
Tada ćemo izračunati kutni koeficijent formulom:

b \u003d y. 1 - sjekira. 1 = -0,28 - 0,42 · (-2.0) \u003d 0,56.
Konstante Freundlich jednadžbe su jednaki:
lG. K \u003d b \u003d0,56; K.= 10 0,56 = 3,63;
1/n \u003d a \u003d0,42.
Izračunajte adsorpciju benzojeve kiseline u koncentraciji od 0,028 mol / l koristeći Freundlich jednadžbu (330):
4. Koristeći jednadžbu oklade, izračunajte specifičnu površinu adsorbenta u skladu s podacima o adsorpciji plinovitih dušika:
Područje koje zauzima molekula dušika u gustom monosloj je 0,08 nm2, gustoća dušika je 1,25 kg / m3.
Odluka:
Jednadžba polimolekularnog adsorpcije oklade u linearnom obliku ima oblik (333)
Za izradu grafikona odredite vrijednosti:
Izgraditi raspored koordinata - p / p s (Sl. 85).
Upotreba prva metoda (Vidi "uvodni blok. Osnove matematičke obrade eksperimentalnih podataka") Definicija izravnih koeficijenata y \u003d ax + b. Definiramo vrijednost koeficijenta b.Kao što je ordinatna točka koja leži na izravnoj, koja je apscisa jednaka 0 ( h.= 0): b. \u003d 5. Odaberite točku na ravnom i odredite njegove koordinate:
(·) 1 (0.2; 309).
Tada ćemo izračunati kutni koeficijent:


Sl. 85. Grafička definicija konstanti polimolekularnog adsorpcije oklade izoterme
Konstante jednadžba izoterme polimolekularnog adsorpcijskog oklada su jednaki:
 ; .
; .
Rješavanje sustava jednadžbi, dobiti ali ∞ \u003d 6,6 · 10 -8 m 3 / kg.
Da bismo izračunali graničnu vrijednost adsorpcije, uzet ćemo ali ∞ do 1 mol:
 .
.
Vrijednost specifične površine adsorbenta nalazi se formulom (329):
5. Polistiren sulfokathionitis u n +-inform težini 1 g uvedeno je u otopinu KCL s početnom koncentracijom iz 0 \u003d 100 EQ / M 3 Volume Vlan\u003d 50 ml i smjesu se drži u ravnotežnom stanju. Izračunajte ekviristiju koncentraciju kalija u ionatu, ako je konstanta ionske izmjene ravnoteže \u003d 2.5, a ukupni tenk kationa je PO \u003d 5 mol-ekv / kg.
Odluka:
Da biste odredili konstantu ionske izmjene, koristite jednadžbu (338). U smolu, H + ioni razmjenjuju na ekvivalentnom broju iona K.
MASE sulfokathionitisa u H + u obliku se određuje formulom (337):


Ukupan broj aniona u njoj je jednak:
Masa aniona u njoj je također određena formulom (337):
