संबद्ध गैस का ऊष्मीय मान। प्राकृतिक गैस और घरेलू उपयोग के लिए इसका ऊष्मीय मान
ईंधन की एक इकाई मात्रा के पूर्ण दहन के दौरान निकलने वाली ऊष्मा की मात्रा को कैलोरी मान (Q) या, जैसा कि कभी-कभी कहा जाता है, ऊष्मीय मान या कैलोरी मान कहा जाता है, जो ईंधन की मुख्य विशेषताओं में से एक है।
गैसों के ऊष्मीय मान को सामान्यतः 1 . कहा जाता है एम 3,सामान्य परिस्थितियों में लिया गया।
तकनीकी गणनाओं में, सामान्य परिस्थितियों को 0 डिग्री सेल्सियस के बराबर तापमान पर और 760 के दबाव पर गैस की स्थिति के रूप में समझा जाता है। एमएमएचजी कला।इन शर्तों के तहत गैस का आयतन निरूपित किया जाता है एनएम 3(सामान्य घन मीटर)।
GOST 2923-45 के अनुसार औद्योगिक गैस माप के लिए, 20 ° C का तापमान और 760 का दबाव सामान्य परिस्थितियों के रूप में लिया जाता है एमएमएचजी कला।गैस की मात्रा इन स्थितियों को संदर्भित करती है, इसके विपरीत एनएम 3हम फोन करेंगे एम 3 (घन मीटर)।
गैसों का ऊष्मीय मान (क्यू))में व्यक्त किया किलो कैलोरी/एनएम ईया में किलो कैलोरी / एम 3।
तरलीकृत गैसों के लिए, ऊष्मीय मान को 1 . कहा जाता है किलोग्राम।
उच्च (क्यू इंच) और निम्न (क्यू एन) कैलोरी मान हैं। सकल ऊष्मीय मान ईंधन के दहन के दौरान बनने वाले जलवाष्प के संघनन की ऊष्मा को ध्यान में रखता है। शुद्ध कैलोरी मान दहन उत्पादों के जल वाष्प में निहित गर्मी को ध्यान में नहीं रखता है, क्योंकि जल वाष्प संघनित नहीं होता है, लेकिन दहन उत्पादों के साथ दूर ले जाया जाता है।
अवधारणाएं क्यू इन और क्यू एन केवल उन गैसों पर लागू होती हैं, जिनके दहन के दौरान जल वाष्प निकलता है (ये अवधारणाएं कार्बन मोनोऑक्साइड पर लागू नहीं होती हैं, जो दहन के दौरान जल वाष्प नहीं देती हैं)।
जब जल वाष्प संघनित होता है, तो ऊष्मा 539 . के बराबर निकलती है किलो कैलोरी / किग्रा।इसके अलावा, जब कंडेनसेट को 0 डिग्री सेल्सियस (या 20 डिग्री सेल्सियस) तक ठंडा किया जाता है, तो क्रमशः 100 या 80 की मात्रा में गर्मी निकलती है। किलो कैलोरी / किग्रा।
कुल मिलाकर, जल वाष्प के संघनन के कारण, गर्मी 600 . से अधिक निकलती है किलो कैलोरी / किग्रा,जो गैस के सकल और शुद्ध ऊष्मीय मान के बीच का अंतर है। शहरी गैस आपूर्ति में उपयोग होने वाली अधिकांश गैसों के लिए यह अंतर 8-10% है।
कुछ गैसों के ऊष्मीय मान का मान तालिका में दिया गया है। 3.
शहरी गैस आपूर्ति के लिए, वर्तमान में गैसों का उपयोग किया जाता है, जो एक नियम के रूप में, कम से कम 3500 का कैलोरी मान होता है। किलो कैलोरी / एनएम 3.यह इस तथ्य से समझाया गया है कि शहरों में गैस की आपूर्ति पाइप के माध्यम से काफी दूरी पर की जाती है। कम ऊष्मीय मान के साथ, बड़ी मात्रा में आपूर्ति करना आवश्यक है। यह अनिवार्य रूप से गैस पाइपलाइनों के व्यास में वृद्धि की ओर जाता है और, परिणामस्वरूप, धातु निवेश में वृद्धि और गैस नेटवर्क के निर्माण के लिए धन, और बाद में, परिचालन लागत में वृद्धि के लिए। कम-कैलोरी गैसों का एक महत्वपूर्ण नुकसान यह है कि ज्यादातर मामलों में उनमें कार्बन मोनोऑक्साइड की एक महत्वपूर्ण मात्रा होती है, जो गैस का उपयोग करते समय और साथ ही नेटवर्क और प्रतिष्ठानों की सर्विसिंग के दौरान खतरे को बढ़ाती है।
3500 . से कम कैलोरी मान वाली गैस किलो कैलोरी/एनएम 3सबसे अधिक बार उद्योग में उपयोग किया जाता है, जहां इसे लंबी दूरी तक ले जाने की आवश्यकता नहीं होती है और भस्म को व्यवस्थित करना आसान होता है। शहरी गैस आपूर्ति के लिए, गैस का एक स्थिर ऊष्मीय मान होना वांछनीय है। उतार-चढ़ाव, जैसा कि हम पहले ही स्थापित कर चुके हैं, 10% से अधिक की अनुमति नहीं है। गैस के ऊष्मीय मान में अधिक परिवर्तन के लिए एक नए समायोजन की आवश्यकता होती है, और कभी-कभी घरेलू उपकरणों के लिए बड़ी संख्या में एकीकृत बर्नर में बदलाव की आवश्यकता होती है, जो महत्वपूर्ण कठिनाइयों से जुड़ा होता है।
दहनशील गैसों का वर्गीकरण
शहरों और औद्योगिक उद्यमों की गैस आपूर्ति के लिए, विभिन्न दहनशील गैसों का उपयोग किया जाता है, जो मूल, रासायनिक संरचना और भौतिक गुणों में भिन्न होते हैं।
मूल रूप से, दहनशील गैसों को ठोस और तरल ईंधन से उत्पादित प्राकृतिक, या प्राकृतिक और कृत्रिम में विभाजित किया जाता है।
प्राकृतिक गैसों को तेल के साथ-साथ विशुद्ध रूप से गैस क्षेत्रों या तेल क्षेत्रों के कुओं से निकाला जाता है। तेल क्षेत्रों की गैसों को संबद्ध गैसें कहा जाता है।
शुद्ध गैस क्षेत्रों की गैसों में मुख्य रूप से भारी हाइड्रोकार्बन की एक छोटी सामग्री के साथ मीथेन होता है। उन्हें संरचना और कैलोरी मान की स्थिरता की विशेषता है।
मीथेन के साथ संबद्ध गैसों में भारी मात्रा में हाइड्रोकार्बन (प्रोपेन और ब्यूटेन) होते हैं। इन गैसों की संरचना और ऊष्मीय मान व्यापक रूप से भिन्न होते हैं।
विशेष गैस संयंत्रों में कृत्रिम गैसों का उत्पादन किया जाता है - या धातुकर्म संयंत्रों में कोयले के दहन के साथ-साथ तेल रिफाइनरियों में उप-उत्पाद के रूप में प्राप्त किया जाता है।
हमारे देश में कोयले से उत्पादित गैसों का उपयोग शहरी गैस आपूर्ति के लिए बहुत सीमित मात्रा में किया जाता है, और उनका विशिष्ट गुरुत्व लगातार कम होता जा रहा है। इसी समय, तेल शोधन के दौरान गैस-गैसोलीन संयंत्रों और तेल रिफाइनरियों में संबद्ध पेट्रोलियम गैसों से प्राप्त तरलीकृत हाइड्रोकार्बन गैसों का उत्पादन और खपत बढ़ रही है। शहरी गैस आपूर्ति के लिए उपयोग की जाने वाली तरल हाइड्रोकार्बन गैसों में मुख्य रूप से प्रोपेन और ब्यूटेन होते हैं।
गैसों की संरचना
गैस का प्रकार और इसकी संरचना काफी हद तक गैस के दायरे, गैस नेटवर्क की योजना और व्यास, गैस बर्नर और व्यक्तिगत गैस पाइपलाइन इकाइयों के लिए डिजाइन समाधान पूर्व निर्धारित करती है।
गैस की खपत कैलोरी मान पर निर्भर करती है, और इसलिए गैस पाइपलाइनों के व्यास और गैस दहन की स्थिति पर निर्भर करती है। औद्योगिक प्रतिष्ठानों में गैस का उपयोग करते समय, दहन तापमान और लौ प्रसार गति और गैस ईंधन संरचना की स्थिरता का बहुत महत्व है। गैसों की संरचना, साथ ही साथ उनके भौतिक-रासायनिक गुण, मुख्य रूप से प्राप्त करने के प्रकार और विधि पर निर्भर करते हैं। गैसें
दहनशील गैसें विभिन्न गैसों के यांत्रिक मिश्रण हैं<как горючих, так и негорючих.
गैसीय ईंधन के दहनशील भाग में शामिल हैं: हाइड्रोजन (एच 2) - बिना रंग, स्वाद और गंध के गैस, इसका कम कैलोरी मान 2579 है किलो कैलोरी / एनएम 3 \मीथेन (सीएच 4) - एक रंगहीन, स्वादहीन और गंधहीन गैस, प्राकृतिक गैसों का मुख्य ज्वलनशील हिस्सा है, इसका कम कैलोरी मान 8555 है किलो कैलोरी / एनएम 3;कार्बन मोनोऑक्साइड (CO) - एक रंगहीन, स्वादहीन और गंधहीन गैस, जो किसी भी ईंधन के अधूरे दहन से प्राप्त होती है, बहुत जहरीली, कम कैलोरी मान 3018 किलो कैलोरी / एनएम 3;भारी-हाइड्रोकार्बन (सी पी एन टी),इस शीर्षक से<и формулой обозначается целый ряд углеводородов (этан - С2Н 6 , пропан - С 3 Нв, бутан- С4Н 10 и др.), низшая теплотворная способность этих газов колеблется от 15226 до 34890 किलो कैलोरी/एनएम*.
गैसीय ईंधन के गैर-दहनशील भाग में शामिल हैं: कार्बन डाइऑक्साइड (सीओ 2), ऑक्सीजन (ओ 2) और नाइट्रोजन (एन 2)।
गैसों के गैर-दहनशील भाग को गिट्टी कहा जाता है। प्राकृतिक गैसों को उच्च कैलोरी मान और कार्बन मोनोऑक्साइड की पूर्ण अनुपस्थिति की विशेषता है। इसी समय, कई क्षेत्रों, मुख्य रूप से गैस और तेल में, एक बहुत ही जहरीली (और संक्षारक गैस) होती है - हाइड्रोजन सल्फाइड (एच 2 एस)। अधिकांश कृत्रिम कोयला गैसों में अत्यधिक जहरीली गैस - कार्बन मोनोऑक्साइड (सीओ) की एक महत्वपूर्ण मात्रा होती है। ) गैस कार्बन और अन्य विषाक्त पदार्थों में ऑक्साइड की उपस्थिति अत्यधिक अवांछनीय है, क्योंकि वे परिचालन कार्य के उत्पादन को जटिल करते हैं और गैस का उपयोग करते समय खतरे को बढ़ाते हैं। मुख्य घटकों के अलावा, गैसों की संरचना में विभिन्न अशुद्धियां शामिल हैं, जिसका विशिष्ट मूल्य प्रतिशत के संदर्भ में नगण्य है। हालाँकि, हजारों और लाखों क्यूबिक मीटर गैस को देखते हुए, अशुद्धियों की कुल मात्रा एक महत्वपूर्ण मूल्य तक पहुँच जाती है। गैस पाइपलाइनों में कई अशुद्धियाँ निकलती हैं, जो अंततः उनकी कमी की ओर ले जाती हैं थ्रूपुट, और कभी-कभी गैस प्रवाह की पूर्ण समाप्ति के लिए। इसलिए, गैस पाइपलाइनों के डिजाइन में गैस में अशुद्धियों की उपस्थिति को ध्यान में रखा जाना चाहिए, साथ ही ऑपरेशन के दौरान।
अशुद्धियों की मात्रा और संरचना गैस के उत्पादन या निष्कर्षण की विधि और उसके शुद्धिकरण की मात्रा पर निर्भर करती है। सबसे हानिकारक अशुद्धियाँ धूल, टार, नेफ़थलीन, नमी और सल्फर यौगिक हैं।
उत्पादन (निष्कर्षण) के दौरान या पाइपलाइनों के माध्यम से गैस परिवहन के दौरान गैस में धूल दिखाई देती है। राल ईंधन के थर्मल अपघटन का एक उत्पाद है और कई कृत्रिम गैसों के साथ होता है। गैस में धूल की उपस्थिति में, राल टार-कीचड़ प्लग और गैस पाइपलाइनों में रुकावटों के निर्माण में योगदान देता है।
नेफ़थलीन आमतौर पर कृत्रिम कोयला गैसों में पाया जाता है। कम तापमान पर, नेफ़थलीन पाइपों में अवक्षेपित हो जाता है और अन्य ठोस और तरल अशुद्धियों के साथ, गैस पाइपलाइनों के प्रवाह क्षेत्र को कम कर देता है।
वाष्प के रूप में नमी लगभग सभी प्राकृतिक और कृत्रिम गैसों में निहित है। यह पानी की सतह के साथ गैसों के संपर्क के कारण गैस क्षेत्र में ही प्राकृतिक गैसों में प्रवेश करता है, और उत्पादन प्रक्रिया के दौरान कृत्रिम गैसों को पानी से संतृप्त किया जाता है। गैस में नमी की महत्वपूर्ण मात्रा में उपस्थिति अवांछनीय है, क्योंकि यह कैलोरी को कम करती है गैस का मूल्य। इसके अलावा, इसमें वाष्पीकरण की उच्च ताप क्षमता होती है, गैस दहन के दौरान नमी वातावरण में दहन उत्पादों के साथ एक महत्वपूर्ण मात्रा में गर्मी को दूर करती है। गैस में एक बड़ी नमी सामग्री भी अवांछनीय है, क्योंकि जब संघनन होता है गैस को "पाइप के माध्यम से अपने आंदोलन के बोझ" में ठंडा किया जाता है, यह हटाए जाने के लिए गैस पाइपलाइन (निचले बिंदुओं में) में पानी के प्लग बना सकता है। इसके लिए विशेष घनीभूत कलेक्टरों की स्थापना और उन्हें पंप करने की आवश्यकता होती है।
सल्फर यौगिकों, जैसा कि पहले ही उल्लेख किया गया है, में हाइड्रोजन सल्फाइड, साथ ही कार्बन डाइसल्फ़ाइड, मर्कैप्टन आदि शामिल हैं। ये यौगिक न केवल मानव स्वास्थ्य पर प्रतिकूल प्रभाव डालते हैं, बल्कि पाइपों के महत्वपूर्ण क्षरण का कारण बनते हैं।
अन्य हानिकारक अशुद्धियों में अमोनिया और साइनाइड यौगिक शामिल हैं, जो मुख्य रूप से कोयला गैसों में पाए जाते हैं। अमोनिया और साइनाइड यौगिकों की उपस्थिति से पाइप धातु का क्षरण बढ़ जाता है।
दहनशील गैसों में कार्बन डाइऑक्साइड और नाइट्रोजन की उपस्थिति भी अवांछनीय है। ये गैसें दहन प्रक्रिया में भाग नहीं लेती हैं, एक गिट्टी होने के कारण जो कैलोरी मान को कम करती है, जिससे गैस पाइपलाइनों के व्यास में वृद्धि होती है और गैसीय ईंधन का उपयोग करने की आर्थिक दक्षता में कमी आती है।
शहरी गैस आपूर्ति के लिए उपयोग की जाने वाली गैसों की संरचना को GOST 6542-50 (तालिका 1) की आवश्यकताओं को पूरा करना चाहिए।
तालिका नंबर एक
देश में सबसे प्रसिद्ध क्षेत्रों की प्राकृतिक गैसों की संरचना का औसत मूल्य तालिका में प्रस्तुत किया गया है। 2.
गैस क्षेत्रों से (सूखा)
| पश्चिमी यूक्रेन। . . | 81,2 | 7,5 | 4,5 | 3,7 | 2,5 | - . | 0,1 | 0,5 | 0,735 | |
| शेबेलिंस्कोए …………………………… | 92,9 | 4,5 | 0,8 | 0,6 | 0,6 | ____ . | 0,1 | 0,5 | 0,603 | |
| स्टावरोपोल क्षेत्र। . | 98,6 | 0,4 | 0,14 | 0,06 | - | 0,1 | 0,7 | 0,561 | ||
| क्रास्नोडार क्षेत्र। . | 92,9 | 0,5 | - | 0,5 | _ | 0,01 | 0,09 | 0,595 | ||
| सेराटोव …………………………… | 93,4 | 2,1 | 0,8 | 0,4 | 0,3 | निशान | 0,3 | 2,7 | 0,576 | |
| गज़ली, बुखारा क्षेत्र | 96,7 | 0,35 | 0,4" | 0,1 | 0,45 | 0,575 | ||||
| तेल और गैस क्षेत्रों से (संबद्ध) | ||||||||||
| रोमाश्किनो …………………………… | 18,5 | 6,2 | 4,7 | 0,1 | 11,5 | 1,07 | ||||
| 7,4 | 4,6 | ____ | निशान | 1,112 | __ . | |||||
| तुयमाज़ी …………………………… | 18,4 | 6,8 | 4,6 | ____ | 0,1 | 7,1 | 1,062 | - | ||
| आशी....... | 23,5 | 9,3 | 3,5 | ____ | 0,2 | 4,5 | 1,132 | - | ||
| निडर.......... ............................. । | 2,5 | . ___ . | 1,5 | 0,721 | - | |||||
| सीज़रान-तेल ………………… | 31,9 | 23,9 - | 5,9 | 2,7 | 0,8 | 1,7 | 1,6 | 31,5 | 0,932 | - |
| ईशिम्बे …………………………… | 42,4 | 20,5 | 7,2 | 3,1 | 2,8 | 1,040 | _ | |||
| अंदिजान। ............................... | 66,5 | 16,6 | 9,4 | 3,1 | 3,1 | 0,03 | 0,2 | 4,17 | 0,801 ; | |
गैसों का ऊष्मीय मान
ईंधन की एक इकाई मात्रा के पूर्ण दहन के दौरान निकलने वाली ऊष्मा की मात्रा को कैलोरी मान (Q) या, जैसा कि कभी-कभी कहा जाता है, ऊष्मीय मान या कैलोरी मान कहा जाता है, जो ईंधन की मुख्य विशेषताओं में से एक है।
गैसों के ऊष्मीय मान को सामान्यतः 1 . कहा जाता है एम 3,सामान्य परिस्थितियों में लिया गया।
तकनीकी गणनाओं में, सामान्य परिस्थितियों को 0 डिग्री सेल्सियस के बराबर तापमान पर और 760 के दबाव पर गैस की स्थिति के रूप में समझा जाता है। एमएमएचजी कला।इन शर्तों के तहत गैस का आयतन निरूपित किया जाता है एनएम 3(सामान्य घन मीटर)।
GOST 2923-45 के अनुसार औद्योगिक गैस माप के लिए, 20 ° C का तापमान और 760 का दबाव सामान्य परिस्थितियों के रूप में लिया जाता है एमएमएचजी कला।गैस की मात्रा इन स्थितियों को संदर्भित करती है, इसके विपरीत एनएम 3हम फोन करेंगे एम 3 (घन मीटर)।
गैसों का ऊष्मीय मान (क्यू))में व्यक्त किया किलो कैलोरी/एनएम ईया में किलो कैलोरी / एम 3।
तरलीकृत गैसों के लिए, ऊष्मीय मान को 1 . कहा जाता है किलोग्राम।
उच्च (क्यू इंच) और निम्न (क्यू एन) कैलोरी मान हैं। सकल ऊष्मीय मान ईंधन के दहन के दौरान बनने वाले जलवाष्प के संघनन की ऊष्मा को ध्यान में रखता है। शुद्ध कैलोरी मान दहन उत्पादों के जल वाष्प में निहित गर्मी को ध्यान में नहीं रखता है, क्योंकि जल वाष्प संघनित नहीं होता है, लेकिन दहन उत्पादों के साथ दूर ले जाया जाता है।
अवधारणाएं क्यू इन और क्यू एन केवल उन गैसों पर लागू होती हैं, जिनके दहन के दौरान जल वाष्प निकलता है (ये अवधारणाएं कार्बन मोनोऑक्साइड पर लागू नहीं होती हैं, जो दहन के दौरान जल वाष्प नहीं देती हैं)।
जब जल वाष्प संघनित होता है, तो ऊष्मा 539 . के बराबर निकलती है किलो कैलोरी / किग्रा।इसके अलावा, जब कंडेनसेट को 0 डिग्री सेल्सियस (या 20 डिग्री सेल्सियस) तक ठंडा किया जाता है, तो क्रमशः 100 या 80 की मात्रा में गर्मी निकलती है। किलो कैलोरी / किग्रा।
कुल मिलाकर, जल वाष्प के संघनन के कारण, गर्मी 600 . से अधिक निकलती है किलो कैलोरी / किग्रा,जो गैस के सकल और शुद्ध ऊष्मीय मान के बीच का अंतर है। शहरी गैस आपूर्ति में उपयोग होने वाली अधिकांश गैसों के लिए यह अंतर 8-10% है।
कुछ गैसों के ऊष्मीय मान का मान तालिका में दिया गया है। 3.
शहरी गैस आपूर्ति के लिए, वर्तमान में गैसों का उपयोग किया जाता है, जो एक नियम के रूप में, कम से कम 3500 का कैलोरी मान होता है। किलो कैलोरी / एनएम 3.यह इस तथ्य से समझाया गया है कि शहरों में गैस की आपूर्ति पाइप के माध्यम से काफी दूरी पर की जाती है। कम ऊष्मीय मान के साथ, बड़ी मात्रा में आपूर्ति करना आवश्यक है। यह अनिवार्य रूप से गैस पाइपलाइनों के व्यास में वृद्धि की ओर जाता है और, परिणामस्वरूप, धातु निवेश में वृद्धि और गैस नेटवर्क के निर्माण के लिए धन, और बाद में, परिचालन लागत में वृद्धि के लिए। कम-कैलोरी गैसों का एक महत्वपूर्ण नुकसान यह है कि ज्यादातर मामलों में उनमें कार्बन मोनोऑक्साइड की एक महत्वपूर्ण मात्रा होती है, जो गैस का उपयोग करते समय और साथ ही नेटवर्क और प्रतिष्ठानों की सर्विसिंग के दौरान खतरे को बढ़ाती है।
3500 . से कम कैलोरी मान वाली गैस किलो कैलोरी/एनएम 3सबसे अधिक बार उद्योग में उपयोग किया जाता है, जहां इसे लंबी दूरी तक ले जाने की आवश्यकता नहीं होती है और भस्म को व्यवस्थित करना आसान होता है। शहरी गैस आपूर्ति के लिए, गैस का एक स्थिर ऊष्मीय मान होना वांछनीय है। उतार-चढ़ाव, जैसा कि हम पहले ही स्थापित कर चुके हैं, 10% से अधिक की अनुमति नहीं है। गैस के ऊष्मीय मान में अधिक परिवर्तन के लिए एक नए समायोजन की आवश्यकता होती है, और कभी-कभी घरेलू उपकरणों के लिए बड़ी संख्या में एकीकृत बर्नर में बदलाव की आवश्यकता होती है, जो महत्वपूर्ण कठिनाइयों से जुड़ा होता है।
दहन की गर्मी दहनशील पदार्थ की रासायनिक संरचना से निर्धारित होती है। दहनशील पदार्थ में निहित रासायनिक तत्वों को स्वीकृत प्रतीकों द्वारा निर्दिष्ट किया जाता है साथ में , एच , हे , एन , एस, और राख और पानी प्रतीक हैं लेकिनऔर वूक्रमश।
विश्वकोश YouTube
-
1 / 5
दहन की गर्मी दहनशील के कार्य द्रव्यमान से संबंधित हो सकती है क्यू पी (\displaystyle क्यू^(पी)), अर्थात्, एक दहनशील पदार्थ के रूप में जिस रूप में यह उपभोक्ता में प्रवेश करता है; पदार्थ को सुखाने के लिए क्यू सी (\displaystyle क्यू^(सी)); पदार्थ के दहनशील द्रव्यमान के लिए क्यू Γ (\displaystyle क्यू^(\गामा )), यानी एक ज्वलनशील पदार्थ जिसमें नमी और राख नहीं होती है।
उच्च अंतर करें ( Q B (\displaystyle Q_(B))) और निचला ( क्यू एच (\displaystyle Q_(H))) ज्वलन की ऊष्मा।
नीचे उच्च कैलोरी मानकिसी पदार्थ के पूर्ण दहन के दौरान निकलने वाली गर्मी की मात्रा को समझें, जिसमें दहन उत्पादों के ठंडा होने के दौरान जल वाष्प के संघनन की गर्मी भी शामिल है।
शुद्ध कैलोरी मानजल वाष्प के संघनन की गर्मी को ध्यान में रखे बिना, पूर्ण दहन के दौरान निकलने वाली गर्मी की मात्रा से मेल खाती है। जलवाष्प के संघनन की ऊष्मा को भी कहा जाता है वाष्पीकरण की गुप्त ऊष्मा (संघनन).
निम्न और उच्च ऊष्मीय मान अनुपात से संबंधित हैं: क्यू बी = क्यू एच + के (डब्ल्यू + 9 एच) (\displaystyle Q_(B)=Q_(H)+k(W+9H)),
जहां k 25 kJ/kg (6 kcal/kg) के बराबर गुणांक है; डब्ल्यू - दहनशील पदार्थ में पानी की मात्रा,% (वजन से); एच दहनशील पदार्थ में हाइड्रोजन की मात्रा है,% (द्रव्यमान से)।
दहन की गर्मी की गणना
इस प्रकार, उच्च ऊष्मीय मान एक दहनशील पदार्थ के एक इकाई द्रव्यमान या आयतन (गैस के लिए) के पूर्ण दहन के दौरान जारी ऊष्मा की मात्रा है और दहन उत्पादों को ओस बिंदु तापमान तक ठंडा करता है। गर्मी इंजीनियरिंग गणना में, सकल कैलोरी मान 100% के रूप में लिया जाता है। गैस के दहन की गुप्त ऊष्मा वह ऊष्मा है जो दहन उत्पादों में निहित जल वाष्प के संघनन के दौरान निकलती है। सैद्धांतिक रूप से, यह 11% तक पहुंच सकता है।
व्यवहार में, संक्षेपण को पूरा करने के लिए दहन उत्पादों को ठंडा करना संभव नहीं है, और इसलिए शुद्ध कैलोरी मान (क्यूएचपी) की अवधारणा पेश की जाती है, जो उच्च कैलोरी मान से जल वाष्प के वाष्पीकरण की गर्मी को घटाकर प्राप्त किया जाता है। पदार्थ और उसके दहन के दौरान गठित। 2514 kJ/kg (600 kcal/kg) 1 किलो जल वाष्प के वाष्पीकरण पर खर्च किया जाता है। शुद्ध कैलोरी मान सूत्रों (kJ / kg या kcal / kg) द्वारा निर्धारित किया जाता है:
क्यू एच पी = क्यू बी पी - 2514 ⋅ ((9 एच पी + डब्ल्यू पी) / 100) (\displaystyle Q_(H)^(P)=Q_(B)^(P)-2514\cdot ((9H^(P)+W^ (पी))/100))(ठोस के लिए)
क्यू एच पी = क्यू बी पी - 600 ⋅ ((9 एच पी + डब्ल्यू पी) / 100) (\displaystyle Q_(H)^(P)=Q_(B)^(P)-600\cdot ((9H^(P)+W^ (पी))/100))(एक तरल पदार्थ के लिए), जहां:
2514 - 0 डिग्री सेल्सियस पर वाष्पीकरण की गर्मी और वायुमंडलीय दबाव, kJ/kg;
एच पी (\displaystyle एच^(पी))और डब्ल्यू पी (\displaystyle डब्ल्यू^(पी))- काम कर रहे ईंधन में हाइड्रोजन और जल वाष्प की सामग्री,%;
9 एक गुणांक है जो दर्शाता है कि जब ऑक्सीजन के संयोजन में 1 किलो हाइड्रोजन जलाया जाता है, तो 9 किलो पानी बनता है।
ऊष्मीय मान ईंधन की सबसे महत्वपूर्ण विशेषता है, क्योंकि यह 1 किलो ठोस या तरल ईंधन या 1 वर्ग मीटर गैसीय ईंधन को kJ/kg (kcal/kg) में जलाने से प्राप्त ऊष्मा की मात्रा निर्धारित करता है। 1 किलो कैलोरी = 4.1868 या 4.19 केजे।
शुद्ध ऊष्मीय मान प्रत्येक पदार्थ के लिए प्रयोगात्मक रूप से निर्धारित किया जाता है और यह एक संदर्भ मान है। यह ठोस और तरल पदार्थों के लिए भी निर्धारित किया जा सकता है, एक ज्ञात मौलिक संरचना के साथ, डी। आई। मेंडेलीव, केजे / किग्रा या केकेसी / किग्रा के सूत्र के अनुसार गणना करके:
क्यू एच पी = 339 ⋅ सी पी + 1256 ⋅ एच पी - 109 ⋅ (ओ पी - एस एल पी) - 25.14 ⋅ (9 ⋅ एच पी + डब्ल्यू पी) (\displaystyle Q_(H)^(P)=339\cdot C^(P)+1256\ cdot H^(P)-109\cdot (O^(P)-S_(L)^(P))-25.14\cdot (9\cdot H^(P)+W^(P)))
क्यू एच पी = 81 ⋅ सी पी + 246 ⋅ एच पी - 26 ⋅ (ओ पी + एस एल पी) − 6 ⋅ डब्ल्यू पी (\displaystyle Q_(H)^(P)=81\cdot C^(P)+246\cdot H^(P) -26\cdot (O^(P)+S_(L)^(P))-6\cdot W^(P)), कहाँ पे:
सी पी (\डिस्प्लेस्टाइल सी_(पी)), एच पी (\displaystyle एच_(पी)), ओ पी (\displaystyle O_(P)), एस एल पी (\displaystyle S_(L)^(P)), डब्ल्यू पी (\displaystyle W_(P))-% (द्रव्यमान द्वारा) में ईंधन के कार्यशील द्रव्यमान में कार्बन, हाइड्रोजन, ऑक्सीजन, वाष्पशील सल्फर और नमी की सामग्री।
तुलनात्मक गणना के लिए, तथाकथित पारंपरिक ईंधन का उपयोग किया जाता है, जिसमें 29308 kJ / kg (7000 kcal / kg) के बराबर दहन की विशिष्ट ऊष्मा होती है।
रूस में, थर्मल गणना (उदाहरण के लिए, विस्फोट और आग के खतरे के लिए एक कमरे की श्रेणी निर्धारित करने के लिए गर्मी भार की गणना) आमतौर पर संयुक्त राज्य अमेरिका, ग्रेट ब्रिटेन, फ्रांस में सबसे कम कैलोरी मान के अनुसार की जाती है - उच्चतम के अनुसार . यूनाइटेड किंगडम और संयुक्त राज्य अमेरिका में, मीट्रिक प्रणाली की शुरुआत से पहले, विशिष्ट ताप मूल्यों को ब्रिटिश थर्मल यूनिट (BTU) प्रति पाउंड (lb) (1Btu/lb = 2.326 kJ/kg) में मापा जाता था।
पदार्थ और सामग्री शुद्ध कैलोरी मान क्यू एच पी (\displaystyle Q_(H)^(P)), एमजे / किग्रा पेट्रोल 41,87 मिटटी तेल 43,54 कागज: किताबें, पत्रिकाएं 13,4 लकड़ी (बार डब्ल्यू = 14%) 13,8 प्राकृतिक रबड़ 44,73 पॉलीविनाइल क्लोराइड लिनोलियम 14,31 रबड़ 33,52 स्टेपल फ़ाइबर 13,8 polyethylene 47,14 स्टायरोफोम 41,6 कपास ढीला 15,7 प्लास्टिक 41,87 टेबल ईंधन (तरल, ठोस और गैसीय) और कुछ अन्य दहनशील पदार्थों के दहन की द्रव्यमान विशिष्ट गर्मी प्रस्तुत करते हैं। ईंधन जैसे: कोयला, जलाऊ लकड़ी, कोक, पीट, मिट्टी का तेल, तेल, शराब, गैसोलीन, प्राकृतिक गैस, आदि माना जाता है।
तालिकाओं की सूची:
एक एक्ज़ोथिर्मिक ईंधन ऑक्सीकरण प्रतिक्रिया में, इसकी रासायनिक ऊर्जा एक निश्चित मात्रा में गर्मी की रिहाई के साथ तापीय ऊर्जा में परिवर्तित हो जाती है। परिणामी तापीय ऊर्जा को ईंधन के दहन की ऊष्मा कहा जाता है। यह इसकी रासायनिक संरचना, आर्द्रता पर निर्भर करता है और मुख्य है। ईंधन का ऊष्मीय मान, जिसे 1 किलो द्रव्यमान या 1 मीटर 3 आयतन के रूप में संदर्भित किया जाता है, द्रव्यमान या आयतन विशिष्ट कैलोरीफ मान बनाता है।
ईंधन के दहन की विशिष्ट ऊष्मा एक इकाई द्रव्यमान के पूर्ण दहन या ठोस, तरल या गैसीय ईंधन के आयतन के दौरान निकलने वाली ऊष्मा की मात्रा है। इंटरनेशनल सिस्टम ऑफ यूनिट्स में, यह मान J / kg या J / m 3 में मापा जाता है।
किसी ईंधन के दहन की विशिष्ट ऊष्मा प्रयोगात्मक रूप से निर्धारित की जा सकती है या विश्लेषणात्मक रूप से गणना की जा सकती है।ऊष्मीय मान निर्धारित करने के लिए प्रायोगिक तरीके ईंधन के दहन के दौरान निकलने वाली ऊष्मा की मात्रा के व्यावहारिक माप पर आधारित होते हैं, उदाहरण के लिए, थर्मोस्टैट और दहन बम के साथ कैलोरीमीटर में। एक ज्ञात रासायनिक संरचना वाले ईंधन के लिए, दहन की विशिष्ट गर्मी मेंडेलीव के सूत्र से निर्धारित की जा सकती है।
दहन के उच्च और निम्न विशिष्ट ताप होते हैं।ईंधन में निहित नमी के वाष्पीकरण पर खर्च की गई गर्मी को ध्यान में रखते हुए, सकल कैलोरी मान ईंधन के पूर्ण दहन के दौरान जारी गर्मी की अधिकतम मात्रा के बराबर है। कम ऊष्मीय मान संघनन की ऊष्मा के मान से उच्च मान से कम होता है, जो ईंधन की नमी और कार्बनिक द्रव्यमान के हाइड्रोजन से बनता है, जो दहन के दौरान पानी में बदल जाता है।
ईंधन गुणवत्ता संकेतक, साथ ही गर्मी इंजीनियरिंग गणना में निर्धारित करने के लिए आमतौर पर दहन की सबसे कम विशिष्ट गर्मी का उपयोग करते हैं, जो ईंधन की सबसे महत्वपूर्ण तापीय और परिचालन विशेषता है और नीचे दी गई तालिकाओं में दी गई है।
ठोस ईंधन (कोयला, जलाऊ लकड़ी, पीट, कोक) के दहन की विशिष्ट ऊष्मा
तालिका एमजे/किलोग्राम की इकाई में शुष्क ठोस ईंधन के दहन की विशिष्ट गर्मी के मूल्यों को दर्शाती है। तालिका में ईंधन को वर्णानुक्रम में नाम से व्यवस्थित किया गया है।
माना जाता है कि ठोस ईंधन में, कोकिंग कोल का सबसे अधिक कैलोरी मान होता है - इसकी विशिष्ट दहन गर्मी 36.3 MJ/kg (या SI इकाइयों में 36.3·10 6 J/kg) होती है। इसके अलावा, उच्च कैलोरी मान कोयले, एन्थ्रेसाइट, चारकोल और ब्राउन कोयले की विशेषता है।
कम ऊर्जा दक्षता वाले ईंधन में लकड़ी, जलाऊ लकड़ी, बारूद, फ़्रीज़टॉर्फ़, तेल शेल शामिल हैं। उदाहरण के लिए, जलाऊ लकड़ी के दहन की विशिष्ट ऊष्मा 8.4 ... 12.5 है, और बारूद - केवल 3.8 MJ / किग्रा।
ठोस ईंधन (कोयला, जलाऊ लकड़ी, पीट, कोक) के दहन की विशिष्ट ऊष्मा
ईंधन एन्थ्रेसाइट 26,8…34,8 लकड़ी छर्रों (गोलियों) 18,5 जलाऊ लकड़ी सूखी 8,4…11 सूखी सन्टी जलाऊ लकड़ी 12,5 गैस कोक 26,9 ब्लास्ट फर्नेस कोक 30,4 अर्द्ध कोक 27,3 पाउडर 3,8 स्लेट 4,6…9 तेल परत 5,9…15 ठोस प्रणोदक 4,2…10,5 पीट 16,3 रेशेदार पीट 21,8 मिलिंग पीट 8,1…10,5 पीट का टुकड़ा 10,8 लिग्नाइट कोयला 13…25 भूरा कोयला (ब्रिकेट्स) 20,2 भूरा कोयला (धूल) 25 डोनेट्स्क कोयला 19,7…24 लकड़ी का कोयला 31,5…34,4 कोयला 27 कोकिंग कोल 36,3 कुज़्नेत्स्क कोयला 22,8…25,1 चेल्याबिंस्क कोयला 12,8 एकिबस्तुज़ कोयला 16,7 फ़्रेज़टॉर्फ़ 8,1 लावा 27,5 तरल ईंधन (शराब, गैसोलीन, मिट्टी के तेल, तेल) के दहन की विशिष्ट गर्मी
तरल ईंधन और कुछ अन्य कार्बनिक तरल पदार्थों के दहन की विशिष्ट गर्मी की तालिका दी गई है। यह ध्यान दिया जाना चाहिए कि गैसोलीन, डीजल ईंधन और तेल जैसे ईंधन को दहन के दौरान उच्च गर्मी रिलीज की विशेषता है।
अल्कोहल और एसीटोन के दहन की विशिष्ट ऊष्मा पारंपरिक मोटर ईंधन की तुलना में काफी कम होती है। इसके अलावा, तरल प्रणोदक का अपेक्षाकृत कम कैलोरी मान होता है और इन हाइड्रोकार्बन के 1 किलो के पूर्ण दहन के साथ, क्रमशः 9.2 और 13.3 एमजे के बराबर गर्मी की मात्रा जारी की जाएगी।
तरल ईंधन (शराब, गैसोलीन, मिट्टी के तेल, तेल) के दहन की विशिष्ट गर्मी
ईंधन दहन की विशिष्ट गर्मी, एमजे / किग्रा एसीटोन 31,4 गैसोलीन A-72 (GOST 2084-67) 44,2 विमानन गैसोलीन B-70 (GOST 1012-72) 44,1 गैसोलीन AI-93 (GOST 2084-67) 43,6 बेंजीन 40,6 शीतकालीन डीजल ईंधन (GOST 305-73) 43,6 ग्रीष्मकालीन डीजल ईंधन (GOST 305-73) 43,4 तरल प्रणोदक (केरोसिन + तरल ऑक्सीजन) 9,2 उड्डयन मिट्टी का तेल 42,9 प्रकाश केरोसिन (GOST 4753-68) 43,7 ज़ाइलीन 43,2 उच्च सल्फर ईंधन तेल 39 कम सल्फर ईंधन तेल 40,5 कम सल्फर ईंधन तेल 41,7 सल्फर ईंधन तेल 39,6 मिथाइल अल्कोहल (मेथनॉल) 21,1 एन-ब्यूटाइल अल्कोहल 36,8 तेल 43,5…46 तेल मीथेन 21,5 टोल्यूनि 40,9 सफेद आत्मा (गोस्ट 313452) 44 इथाइलीन ग्लाइकॉल 13,3 एथिल अल्कोहल (इथेनॉल) 30,6 गैसीय ईंधन और दहनशील गैसों के दहन की विशिष्ट ऊष्मा
एमजे/किलोग्राम के आयाम में गैसीय ईंधन और कुछ अन्य दहनशील गैसों के दहन की विशिष्ट गर्मी की एक तालिका प्रस्तुत की गई है। माना गैसों में से, दहन की सबसे बड़ी द्रव्यमान विशिष्ट गर्मी भिन्न होती है। इस गैस के एक किलोग्राम के पूर्ण दहन से 119.83 MJ ऊष्मा निकल जाएगी। इसके अलावा, प्राकृतिक गैस जैसे ईंधन का उच्च कैलोरी मान होता है - प्राकृतिक गैस के दहन की विशिष्ट गर्मी 41 ... 49 एमजे / किग्रा (शुद्ध 50 एमजे / किग्रा के लिए) होती है।
गैसीय ईंधन और दहनशील गैसों (हाइड्रोजन, प्राकृतिक गैस, मीथेन) के दहन की विशिष्ट ऊष्मा
ईंधन दहन की विशिष्ट गर्मी, एमजे / किग्रा 1-ब्यूटेन 45,3 अमोनिया 18,6 एसिटिलीन 48,3 हाइड्रोजन 119,83 हाइड्रोजन, मीथेन के साथ मिश्रण (द्रव्यमान द्वारा 50% एच 2 और 50% सीएच 4) 85 हाइड्रोजन, मीथेन और कार्बन मोनोऑक्साइड के साथ मिश्रण (वजन के हिसाब से 33-33-33%) 60 हाइड्रोजन, कार्बन मोनोऑक्साइड के साथ मिश्रण (द्रव्यमान द्वारा 50% एच 2 50% सीओ 2) 65 ब्लास्ट फर्नेस गैस 3 कोक ओवन गैस 38,5 एलपीजी तरलीकृत हाइड्रोकार्बन गैस (प्रोपेन-ब्यूटेन) 43,8 आइसोब्यूटेन 45,6 मीथेन 50 एन-ब्यूटेन 45,7 एन-हेक्सेन 45,1 एन-पैंटेन 45,4 एसोसिएटेड गैस 40,6…43 प्राकृतिक गैस 41…49 प्रोपेडियन 46,3 प्रोपेन 46,3 प्रोपलीन 45,8 प्रोपलीन, हाइड्रोजन और कार्बन मोनोऑक्साइड के साथ मिश्रण (वजन के हिसाब से 90%-9%-1%) 52 एटैन 47,5 ईथीलीन 47,2 कुछ ज्वलनशील पदार्थों के दहन की विशिष्ट ऊष्मा
कुछ ज्वलनशील पदार्थों (लकड़ी, कागज, प्लास्टिक, पुआल, रबर, आदि) के दहन की विशिष्ट ऊष्मा की एक तालिका दी गई है। यह दहन के दौरान उच्च गर्मी रिलीज के साथ सामग्री पर ध्यान दिया जाना चाहिए। ऐसी सामग्रियों में शामिल हैं: विभिन्न प्रकार के रबर, विस्तारित पॉलीस्टाइनिन (पॉलीस्टाइनिन), पॉलीप्रोपाइलीन और पॉलीइथाइलीन।
कुछ ज्वलनशील पदार्थों के दहन की विशिष्ट ऊष्मा
ईंधन दहन की विशिष्ट गर्मी, एमजे / किग्रा कागज़ 17,6 कृत्रिम चमड़ा 21,5 लकड़ी (14% की नमी सामग्री वाले बार) 13,8 ढेर में लकड़ी 16,6 बलूत का लकड़ा 19,9 लकड़ी सजाना 20,3 लकड़ी हरा 6,3 देवदार की लकड़ी 20,9 कप्रोनो 31,1 कार्बोलाइट उत्पाद 26,9 गत्ता 16,5 स्टाइरीन-ब्यूटाडीन रबर SKS-30AR 43,9 प्राकृतिक रबड़ 44,8 सिंथेटिक रबर 40,2 रबड़ एससीएस 43,9 क्लोरोप्रीन रबर 28 पॉलीविनाइल क्लोराइड लिनोलियम 14,3 दो-परत पॉलीविनाइल क्लोराइड लिनोलियम 17,9 लिनोलियम पॉलीविनाइलक्लोराइड एक महसूस के आधार पर 16,6 गर्म आधार पर लिनोलियम पॉलीविनाइल क्लोराइड 17,6 कपड़े के आधार पर लिनोलियम पॉलीविनाइलक्लोराइड 20,3 लिनोलियम रबर (रिलिन) 27,2 पैराफिन ठोस 11,2 पॉलीफ़ोम पीवीसी -1 19,5 पॉलीफोम एफएस -7 24,4 पॉलीफोम एफएफ 31,4 विस्तारित पॉलीस्टाइनिन PSB-S 41,6 पॉलीयूरीथेन फ़ोम 24,3 fibreboard 20,9 पॉलीविनाइल क्लोराइड (पीवीसी) 20,7 पॉलीकार्बोनेट 31 polypropylene 45,7 polystyrene 39 हाइ डेन्सिटी पोलिथीन 47 कम दबाव वाली पॉलीथीन 46,7 रबड़ 33,5 रूबेरॉयड 29,5 कालिख चैनल 28,3 सूखी घास 16,7 घास 17 कार्बनिक ग्लास (प्लेक्सीग्लस) 27,7 टेक्स्टोलाइट 20,9 सहने 16 टीएनटी 15 सूती 17,5 सेल्यूलोज 16,4 ऊन और ऊन के रेशे 23,1 स्रोत:
- GOST 147-2013 ठोस खनिज ईंधन। उच्च ऊष्मीय मान का निर्धारण और निम्न ऊष्मीय मान की गणना।
- GOST 21261-91 पेट्रोलियम उत्पाद। सकल ऊष्मीय मान ज्ञात करने और शुद्ध उष्मीय मान की गणना करने की विधि।
- GOST 22667-82 दहनशील प्राकृतिक गैसें। ऊष्मीय मान, सापेक्ष घनत्व और वोबे संख्या निर्धारित करने के लिए गणना विधि।
- GOST 31369-2008 प्राकृतिक गैस। घटक संरचना के आधार पर कैलोरी मान, घनत्व, सापेक्ष घनत्व और वोबे संख्या की गणना।
- ज़ेम्स्की जी.टी. अकार्बनिक और कार्बनिक पदार्थों के ज्वलनशील गुण: संदर्भ पुस्तक एम .: वीएनआईआईपीओ, 2016 - 970 पी।
गैस ईंधन को प्राकृतिक और कृत्रिम में विभाजित किया गया है और यह एक निश्चित मात्रा में जल वाष्प, और कभी-कभी धूल और टार युक्त दहनशील और गैर-दहनशील गैसों का मिश्रण है। गैस ईंधन की मात्रा सामान्य परिस्थितियों (760 मिमी एचजी और 0 डिग्री सेल्सियस) के तहत घन मीटर में व्यक्त की जाती है, और संरचना मात्रा के प्रतिशत के रूप में व्यक्त की जाती है। ईंधन की संरचना के तहत इसके शुष्क गैसीय भाग की संरचना को समझें।
प्राकृतिक गैस ईंधन
सबसे आम गैस ईंधन प्राकृतिक गैस है, जिसका उच्च कैलोरी मान होता है। प्राकृतिक गैस का आधार मीथेन है, जिसकी सामग्री 76.7-98% है। अन्य गैसीय हाइड्रोकार्बन यौगिक 0.1 से 4.5% तक प्राकृतिक गैस का हिस्सा हैं।
तरलीकृत गैस तेल शोधन का एक उत्पाद है - इसमें मुख्य रूप से प्रोपेन और ब्यूटेन का मिश्रण होता है।
प्राकृतिक गैस (सीएनजी, एनजी): मीथेन CH4 90% से अधिक, एथेन C2 H5 4% से कम, प्रोपेन C3 H8 1% से कम
तरलीकृत गैस (एलपीजी): प्रोपेन C3 H8 65% से अधिक, ब्यूटेन C4 H10 35% से कम
दहनशील गैसों में शामिल हैं: हाइड्रोजन एच 2, मीथेन सीएच 4, अन्य हाइड्रोकार्बन यौगिक सी एम एच एन, हाइड्रोजन सल्फाइड एच 2 एस और गैर-दहनशील गैसें, कार्बन डाइऑक्साइड सीओ 2, ऑक्सीजन ओ 2, नाइट्रोजन एन 2 और जल वाष्प एच की एक छोटी मात्रा 2 ओ सूचकांक एमऔर पीसी और एच में विभिन्न हाइड्रोकार्बन के यौगिकों की विशेषता है, उदाहरण के लिए, मीथेन सीएच 4 . के लिए टी = 1 और एन= 4, एथेन 2 Н b . के लिए टी = 2और एन= बी आदि
शुष्क गैसीय ईंधन की संरचना (मात्रा के अनुसार प्रतिशत में):
सीओ + एच 2 + 2 सी एम एच एन + एच 2 एस + सीओ 2 + ओ 2 + एन 2 = 100%।शुष्क गैसीय ईंधन का गैर-दहनशील हिस्सा - गिट्टी - नाइट्रोजन एन और कार्बन डाइऑक्साइड सीओ 2 है।
गीले गैसीय ईंधन की संरचना निम्नानुसार व्यक्त की जाती है:
सीओ + एच 2 + Σ सी एम एच एन + एच 2 एस + सीओ 2 + ओ 2 + एन 2 + एच 2 ओ \u003d 100%।
दहन की गर्मी, kJ / m (kcal / m 3), सामान्य परिस्थितियों में शुद्ध शुष्क गैस का 1 m 3 निम्नानुसार निर्धारित किया जाता है:
क्यू एन एस \u003d 0.01,
जहां क्यूको, क्यू एन 2, क्यू एम एन एन क्यू एन 2 . के साथ एस। - मिश्रण बनाने वाली व्यक्तिगत गैसों के दहन की गर्मी, kJ / m 3 (kcal / m 3); सीओ, एच 2,सेमी एच एन, एच 2 एस - घटक जो गैस मिश्रण बनाते हैं, मात्रा से%।
अधिकांश घरेलू क्षेत्रों के लिए सामान्य परिस्थितियों में शुष्क प्राकृतिक गैस के 1 एम3 का कैलोरी मान 33.29 - 35.87 एमजे/एम3 (7946 - 8560 किलो कैलोरी/एम3) है। गैसीय ईंधन के अभिलक्षण तालिका 1 में दिए गए हैं।
उदाहरण।निम्नलिखित संरचना के प्राकृतिक गैस (सामान्य परिस्थितियों में) का शुद्ध कैलोरी मान निर्धारित करें:
एच 2 एस = 1%; सीएच 4 = 76.7%; सी 2 एच 6 = 4.5%; सी 3 एच 8 = 1.7%; सी 4 एच 10 = 0.8%; सी 5 एच 12 = 0.6%।
तालिका 1 से गैसों की विशेषताओं को सूत्र (26) में प्रतिस्थापित करने पर, हम प्राप्त करते हैं:
क्यू एनएस \u003d 0.01 \u003d 33981 केजे / एम 3 या
क्यू एनएस \u003d 0.01 (5585.1 + 8555 76.7 + 15 226 4.5 + 21 795 1.7 + 28 338 0.8 + 34 890 0.6) \u003d 8109 किलो कैलोरी / मी 3.
तालिका नंबर एक। गैसीय ईंधन के लक्षण
गैस
पद
ज्वलन की ऊष्माक्यू एन एस
केजे/एम3
किलो कैलोरी/एम3
हाइड्रोजन एच, 10820 2579 कार्बन मोनोआक्साइड इसलिए 12640 3018 हाइड्रोजन सल्फाइड एच 2 एस 23450 5585 मीथेन सीएच 4 35850 8555 एटैन सी 2 एच 6 63 850 15226 प्रोपेन सी 3 एच 8 91300 21795 बुटान सी 4 एच 10 118700 22338 पेंटेन सी 5 एच 12 146200 34890 ईथीलीन सी 2 एच 4 59200 14107 प्रोपलीन सी 3 एच 6 85980 20541 ब्यूटिलीन सी 4 एच 8 113 400 27111 बेंजीन सी 6 एच 6 140400 33528 DE प्रकार के बॉयलर एक टन भाप का उत्पादन करने के लिए 71 से 75 m3 प्राकृतिक गैस की खपत करते हैं। सितंबर 2008 में रूस में गैस की लागत 2.44 रूबल प्रति घन मीटर है। नतीजतन, एक टन भाप की कीमत 71 × 2.44 = 173 रूबल 24 कोप्पेक होगी। कारखानों में एक टन भाप की वास्तविक लागत डीई बॉयलरों के लिए कम से कम 189 रूबल प्रति टन भाप है।
DKVR प्रकार के बॉयलर एक टन भाप का उत्पादन करने के लिए 103 से 118 m3 प्राकृतिक गैस की खपत करते हैं। इन बॉयलरों के लिए एक टन भाप की न्यूनतम अनुमानित लागत 103 × 2.44 = 251 रूबल 32 कोप्पेक है। पौधों के लिए भाप की वास्तविक लागत कम से कम 290 रूबल प्रति टन है।
स्टीम बॉयलर DE-25 के लिए प्राकृतिक गैस की अधिकतम खपत की गणना कैसे करें? यह बॉयलर की विशिष्टता है। प्रति घंटे 1840 क्यूब्स। लेकिन आप गणना भी कर सकते हैं। 25 टन (25 हजार किग्रा) को भाप और पानी की थैलीपी (666.9-105) के बीच के अंतर से गुणा किया जाना चाहिए और यह सब बॉयलर की दक्षता 92.8% और गैस के दहन की गर्मी से विभाजित होता है। 8300. और सभी
कृत्रिम गैस ईंधन
कृत्रिम ज्वलनशील गैसें स्थानीय ईंधन हैं, क्योंकि इनका ऊष्मीय मान बहुत कम होता है। उनके मुख्य दहनशील तत्व कार्बन मोनोऑक्साइड CO और हाइड्रोजन H2 हैं। इन गैसों का उपयोग उत्पादन की सीमा के भीतर किया जाता है जहां उन्हें तकनीकी और बिजली संयंत्रों के लिए ईंधन के रूप में प्राप्त किया जाता है।
सभी प्राकृतिक और कृत्रिम दहनशील गैसें विस्फोटक होती हैं, जो खुली लौ या चिंगारी पर प्रज्वलित करने में सक्षम होती हैं। गैस की निचली और ऊपरी विस्फोटक सीमाएँ होती हैं, अर्थात्। हवा में उच्चतम और निम्नतम प्रतिशत सांद्रता। प्राकृतिक गैसों की निचली विस्फोटक सीमा 3% से 6% तक होती है, जबकि ऊपरी सीमा 12% से 16% तक होती है। सभी ज्वलनशील गैसें मानव शरीर में जहर पैदा कर सकती हैं। दहनशील गैसों के मुख्य विषैले पदार्थ हैं: कार्बन मोनोऑक्साइड CO, हाइड्रोजन सल्फाइड H2S, अमोनिया NH3।
प्राकृतिक दहनशील गैसें, साथ ही कृत्रिम, रंगहीन (अदृश्य), गंधहीन होती हैं, जो गैस पाइपलाइन फिटिंग में लीक के माध्यम से बॉयलर रूम के इंटीरियर में घुसने पर उन्हें खतरनाक बनाती हैं। विषाक्तता से बचने के लिए, दहनशील गैसों को एक गंधक के साथ इलाज किया जाना चाहिए - एक अप्रिय गंध वाला पदार्थ।
ठोस ईंधन के गैसीकरण द्वारा उद्योग में कार्बन मोनोऑक्साइड सीओ प्राप्त करना
औद्योगिक उद्देश्यों के लिए, कार्बन मोनोऑक्साइड ठोस ईंधन के गैसीकरण द्वारा प्राप्त किया जाता है, अर्थात इसका गैसीय ईंधन में परिवर्तन। तो आप किसी भी ठोस ईंधन से कार्बन मोनोऑक्साइड प्राप्त कर सकते हैं - जीवाश्म कोयला, पीट, जलाऊ लकड़ी, आदि।
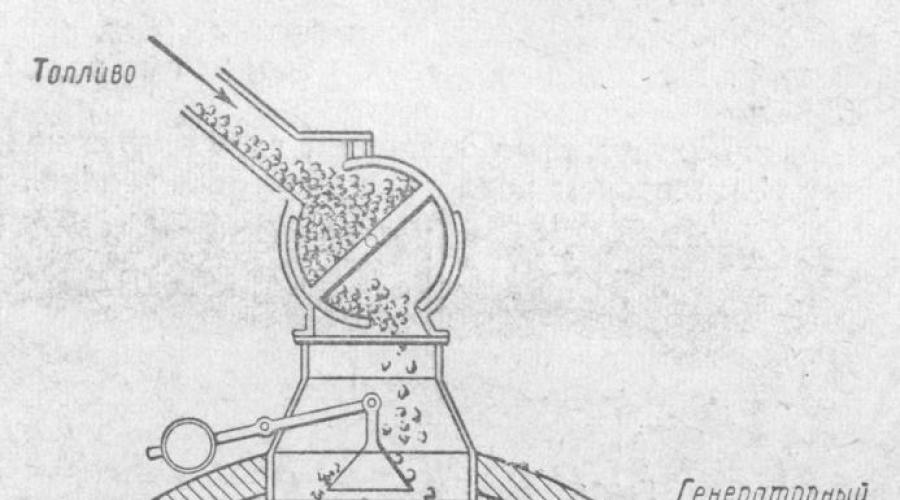
ठोस ईंधन के गैसीकरण की प्रक्रिया को प्रयोगशाला प्रयोग (चित्र 1) में दिखाया गया है। आग रोक ट्यूब को चारकोल के टुकड़ों से भरकर, हम इसे जोर से गर्म करते हैं और ऑक्सीजन को गैसोमीटर से गुजरने देते हैं। ट्यूब से निकलने वाली गैसों को एक चूने के पानी के वॉशर से गुजरने दें और फिर उसमें आग लगा दें। चूने का पानी बादल बन जाता है, गैस एक नीली लौ के साथ जलती है। यह प्रतिक्रिया उत्पादों में CO2 डाइऑक्साइड और कार्बन मोनोऑक्साइड CO की उपस्थिति को इंगित करता है।
इन पदार्थों के निर्माण को इस तथ्य से समझाया जा सकता है कि जब ऑक्सीजन गर्म कोयले के संपर्क में आती है, तो बाद वाले को पहले कार्बन डाइऑक्साइड में ऑक्सीकृत किया जाता है: सी + ओ 2 \u003d सीओ 2
फिर, गर्म कोयले से गुजरते हुए, कार्बन डाइऑक्साइड आंशिक रूप से इसके द्वारा कार्बन मोनोऑक्साइड में कम हो जाता है: सीओ 2 + सी \u003d 2CO
चावल। 1. कार्बन मोनोऑक्साइड (प्रयोगशाला अनुभव) प्राप्त करना।
औद्योगिक परिस्थितियों में, ठोस ईंधन का गैसीकरण भट्टियों में किया जाता है जिन्हें गैस जनरेटर कहा जाता है।
गैसों के परिणामी मिश्रण को उत्पादक गैस कहते हैं।
गैस जनरेटर डिवाइस को चित्र में दिखाया गया है। यह एक स्टील सिलेंडर है जिसकी ऊंचाई लगभग 5 . है एमऔर लगभग 3.5 . का व्यास एम,आग रोक ईंटों के साथ अंदर पंक्तिबद्ध। ऊपर से, गैस जनरेटर ईंधन से भरा हुआ है; नीचे से हवा या जलवाष्प की आपूर्ति पंखे द्वारा जाली के माध्यम से की जाती है।
हवा में ऑक्सीजन ईंधन के कार्बन के साथ प्रतिक्रिया करता है, कार्बन डाइऑक्साइड बनाता है, जो गर्म ईंधन की एक परत के माध्यम से ऊपर उठता है, कार्बन द्वारा कार्बन मोनोऑक्साइड में कम हो जाता है।
यदि जनरेटर में केवल हवा को उड़ाया जाता है, तो एक गैस प्राप्त होती है, जिसमें इसकी संरचना में कार्बन मोनोऑक्साइड और हवा की नाइट्रोजन (साथ ही सीओ 2 और अन्य अशुद्धियों की एक निश्चित मात्रा) होती है। इस जनरेटर गैस को वायु गैस कहा जाता है।
यदि, हालांकि, जल वाष्प को गर्म कोयले के साथ जनरेटर में उड़ाया जाता है, तो प्रतिक्रिया के परिणामस्वरूप कार्बन मोनोऑक्साइड और हाइड्रोजन बनते हैं: सी + एच 2 ओ \u003d सीओ + एच 2
गैसों के इस मिश्रण को जल गैस कहते हैं। वायु गैस की तुलना में जल गैस का ऊष्मीय मान अधिक होता है, क्योंकि इसकी संरचना में कार्बन मोनोऑक्साइड के साथ-साथ एक दूसरी दहनशील गैस - हाइड्रोजन भी शामिल है। जल गैस (संश्लेषण गैस), ईंधन के गैसीकरण के उत्पादों में से एक। जल गैस में मुख्य रूप से CO (40%) और H2 (50%) होते हैं। जल गैस एक ईंधन है (ऊष्मीय मान 10,500 kJ/m3, या 2730 kcal/mg) और साथ ही मेथनॉल के संश्लेषण के लिए कच्चा माल है। जल गैस, हालांकि, लंबे समय तक प्राप्त नहीं की जा सकती है, क्योंकि इसके गठन की प्रतिक्रिया एंडोथर्मिक (गर्मी के अवशोषण के साथ) होती है, और इसलिए जनरेटर में ईंधन ठंडा हो जाता है। कोयले को गर्म रखने के लिए, जनरेटर में जल वाष्प के इंजेक्शन को हवा के इंजेक्शन के साथ वैकल्पिक किया जाता है, जिसकी ऑक्सीजन, जैसा कि ज्ञात है, गर्मी छोड़ने के लिए ईंधन के साथ प्रतिक्रिया करता है।
हाल ही में, ईंधन गैसीकरण के लिए भाप-ऑक्सीजन विस्फोट का व्यापक रूप से उपयोग किया गया है। ईंधन परत के माध्यम से जल वाष्प और ऑक्सीजन को एक साथ उड़ाने से प्रक्रिया को लगातार करना संभव हो जाता है, जनरेटर की उत्पादकता में काफी वृद्धि होती है और हाइड्रोजन और कार्बन मोनोऑक्साइड की उच्च सामग्री के साथ गैस प्राप्त होती है।
आधुनिक गैस जनरेटर निरंतर क्रिया के शक्तिशाली उपकरण हैं।
ताकि जब गैस जनरेटर को ईंधन की आपूर्ति की जाती है, दहनशील और जहरीली गैसें वातावरण में प्रवेश नहीं करती हैं, तो लोडिंग ड्रम को दोगुना कर दिया जाता है। जबकि ईंधन ड्रम के एक डिब्बे में प्रवेश करता है, ईंधन दूसरे डिब्बे से जनरेटर में डाला जाता है; जब ड्रम घूमता है, तो इन प्रक्रियाओं को दोहराया जाता है, जबकि जनरेटर हर समय वातावरण से अलग रहता है। जनरेटर में ईंधन का समान वितरण एक शंकु का उपयोग करके किया जाता है, जिसे विभिन्न ऊंचाइयों पर स्थापित किया जा सकता है। जब इसे नीचे किया जाता है, तो कोयला जनरेटर के केंद्र के करीब होता है, जब शंकु को ऊपर उठाया जाता है, तो कोयले को जनरेटर की दीवारों के करीब फेंक दिया जाता है।
गैस जनरेटर से राख को हटाना यंत्रीकृत है। शंकु के आकार की जाली को एक विद्युत मोटर द्वारा धीरे-धीरे घुमाया जाता है। उसी समय, राख को जनरेटर की दीवारों पर विस्थापित कर दिया जाता है और विशेष उपकरणों के साथ राख बॉक्स में डाल दिया जाता है, जहां से इसे समय-समय पर हटा दिया जाता है।
पहला गैस लैंप 1819 में सेंट पीटर्सबर्ग में आप्टेकार्स्की द्वीप पर जलाया गया था। जिस गैस का उपयोग किया गया था वह कोयले के गैसीकरण द्वारा प्राप्त की गई थी। इसे हल्की गैस कहा जाता था।
महान रूसी वैज्ञानिक डी। आई। मेंडेलीव (1834-1907) ने इस विचार को व्यक्त करने वाले पहले व्यक्ति थे कि कोयले का गैसीकरण सीधे भूमिगत किया जा सकता है, इसे उठाए बिना। ज़ारिस्ट सरकार ने मेंडेलीव के प्रस्ताव की सराहना नहीं की।
भूमिगत गैसीकरण के विचार को वी. आई. लेनिन ने गर्मजोशी से समर्थन दिया। उन्होंने इसे "प्रौद्योगिकी की महान विजयों में से एक" कहा। सोवियत राज्य द्वारा पहली बार भूमिगत गैसीकरण किया गया था। महान देशभक्तिपूर्ण युद्ध से पहले ही, सोवियत संघ में डोनेट्स्क और मॉस्को क्षेत्र के कोयला घाटियों में भूमिगत जनरेटर काम कर रहे थे।
चित्रा 3 भूमिगत गैसीकरण के तरीकों में से एक का एक विचार देता है कोयला सीम में दो कुएं रखे गए हैं, जो एक चैनल के साथ नीचे से जुड़े हुए हैं। इस तरह के चैनल में एक कुएं के पास कोयले में आग लगाई जाती है और वहां विस्फोट की आपूर्ति की जाती है। दहन उत्पाद, चैनल के साथ चलते हुए, गर्म कोयले के साथ बातचीत करते हैं, जिसके परिणामस्वरूप पारंपरिक जनरेटर की तरह दहनशील गैस का निर्माण होता है। गैस दूसरे कुएं से सतह पर आती है।
जनरेटर गैस का व्यापक रूप से औद्योगिक भट्टियों को गर्म करने के लिए उपयोग किया जाता है - धातुकर्म, कोक और कारों में ईंधन के रूप में (चित्र 4)।
चावल। 3. कोयले के भूमिगत गैसीकरण की योजना।
कई कार्बनिक उत्पाद, जैसे तरल ईंधन, जल गैस के हाइड्रोजन और कार्बन मोनोऑक्साइड से संश्लेषित होते हैं। सिंथेटिक तरल ईंधन - ईंधन (मुख्य रूप से गैसोलीन), कार्बन मोनोऑक्साइड और हाइड्रोजन से 150-170 डिग्री सेल्सियस पर संश्लेषण द्वारा प्राप्त किया जाता है और उत्प्रेरक (निकल) की उपस्थिति में 0.7 - 20 एमएन / एम 2 (200 किग्रा / सेमी 2) का दबाव होता है। लोहा, कोबाल्ट)। तेल की कमी के कारण द्वितीय विश्व युद्ध के दौरान जर्मनी में सिंथेटिक तरल ईंधन का पहला उत्पादन आयोजित किया गया था। सिंथेटिक तरल ईंधन को उनकी उच्च लागत के कारण व्यापक वितरण नहीं मिला है। हाइड्रोजन का उत्पादन करने के लिए जल गैस का उपयोग किया जाता है। ऐसा करने के लिए, जल वाष्प के साथ मिश्रण में जल गैस को उत्प्रेरक की उपस्थिति में गर्म किया जाता है और परिणामस्वरूप, जल गैस में पहले से मौजूद हाइड्रोजन के अतिरिक्त हाइड्रोजन प्राप्त होता है: सीओ + एच 2 ओ \u003d सीओ 2 + एच 2