Теплота сгорания попутного газа. Природный газ и его теплотворность в условиях домашнего использования
Читайте также
Количество тепла, выделяемое при полном сгорании единицы количества топлива, называется теплотворной способностью (Q) или, как иногда говорят, теплотворностью, или калорийностью, которая является одной из основных характеристик топлива.
Теплотворную способность газов обычно относят к 1 м 3 , взятому при нормальных условиях.
При технических расчетах под нормальными условиями понимается состояние газа при температуре, равной 0°С, и, при давлении 760 мм рт. ст. Объем газа при этих условиях обозначается нм 3 (нормальный метр кубический).
Для промышленных измерений газа по ГОСТ 2923-45 за нормальные условия приняты температура 20°С и Давление 760 мм рт. ст. Объем газа, отнесенный к этим условиям, в отличие от нм 3 будем называть м 3 (метр кубический).
Теплотворная способность газов (Q}) выражается в ккал/нм э или в ккал/м 3 .
Для сжиженных газов теплотворную способность относят к 1 кг.
Различают высшую (Q в) и низшую (Q н) теплотворность. Высшая теплотворная способность учитывает теплоту конденсации водяных паров, образующихся при сжигании топлива. Низшая теплотворная способность не учитывает тепло, содержащееся в водяных парах продуктов сгорания, так как водяные лары не конденсируются, а уносятся с продуктами сгорания.
Понятия Q в и Q н относятся только к тем газам, при сгорании которых выделяются водяные пары (к окиси углерода, не дающей при сгорании паров воды, эти понятия не относятся).
При конденсации водяных паров выделяется тепло, равное 539 ккал/кг. Кроме того, при охлаждении конденсата до 0°С (.или 20°С) соответственно выделяется тепло в количестве 100 или 80 ккал/кг.
Всего за счет конденсации водяных паров выделяется тепла более 600 ккал/кг, что составляет разность между высшей и низшей теплотворной способностью газа. Для большинства газов, применяемых в городском газоснабжении, эта разность равна 8-10%.
Значения теплотворных способностей некоторых газов приведены в табл. 3.
Для городского газоснабжения в настоящее время используют газы, имеющие, как правило, теплотворность не менее 3500 ккал/нм 3 . Объясняется это тем, что в условиях городов газ подается по трубам на значительные расстояния. При низкой теплотворности его требуется подавать большое количество. Это неизбежно ведет к увеличению диаметров газоцроводов и как следствие к увеличению металловложений и средств на строительство газовых сетей, а.в.последующем: и к увеличению затрат на эксплуатацию. Существенным недостатком низкокалорийных газов является еще то, что в большинстве случаев они содержат значительное количество окиси углерода, из-за чего повышается опасность при использовании газа, а также при обслуживании сетей и установок.
Газ теплотворной способностью менее 3500 ккал/нм 3 наиболее часто используют в промышленности, где не требуется транспортировать его на большие расстояния и проще организовать сжигание. Для городского газоснабжения теплотворность газа желательно иметь постоянной. Колебания, как мы уже установили, допускаются не более 10%. Большее изменение теплотворной способности газа требует новой регулировки, а иногда и смены большого количества унифицированных горелок бытовых приборов, что связано со значительными трудностями.
Классификация горючих газов
Для газоснабжения городов и промышленных предприятий применяют различные горючие газы, отличающиеся по происхождению, химическому составу и физическим свойствам.
По происхождению горючие газы разделяются на естественные, или природные, и на искусственные, вырабатываемые из твердого и жидкого топлива.
Природные газы добывают из скважин чисто газовых месторождений или нефтяных месторождений попутно с нефтью. Газы нефтяных месторождений называются попутными.
Газы чисто газовых месторождений в основном состоят из метана с небольшим содержанием тяжелых углеводородов. Они характеризуются постоянством состава и теплотворности.
Попутные газы наряду с метаном содержат значительное количество тяжелых углеводородов (пропан и бутан). Состав и теплотворность этих газов колеблются в широких пределах.
Искусственные газы вырабатывают на специальных газовых заводах -или получают как побочный продукт при сжигании угля на металлургических заводах, а также на заводах по переработке нефти.
Газы, вырабатываемые из каменного угля, у нас в стране для городского газоснабжения применяются в весьма ограниченных количествах, и удельный вес их все время уменьшается. В то же время растет производство и потребление сжиженных углеводородных газов, полученных из попутных нефтяных газов на газобензиновых заводах и на нефтеперерабатывающих заводах при переработке нефти. Жидкие углеводородные газы, используемые для городского газоснабжения, состоят в основном из пропана и бутана.
Состав газов
Вид газа и его состав в значительной степени предопределяют область применения газа, схему и диаметры газовой сети, конструктивные решения газогорелочных устройств и отдельных узлов газопроводов.
От теплотворной способности зависит расход газа, а отсюда-диаметры газопроводов и условия сжигания газа. При применении газа в промышленных установках весьма существенное значение имеют температура горения и скорость распространения пламени и постоянство состава газового топлива Состав газов, а также физико-химические свойства их прежде всего зависят от вида и способа получения газов.
Горючие газы представляют механические смеси различных газов <как горючих, так и негорючих.
В горючую часть газообразного топлива входят: водород (Н 2)-газ без цвета, вкуса и запаха, низшая теплотворная способность его составляет 2579 ккал/нм 3 \ метан (СН 4) - газ без цвета, вкуса и запаха, является основной горючей частью природных газов, низшая теплотворная способность его 8555 ккал/нм 3 ; окись углерода (СО) - газ без цвета, вкуса и запаха, получается пр.и неполном сгорании любого топлива, очень ядовит, низшая теплотворная способность 3018 ккал/нм 3 ; тяжелые-углеводороды (С п Н т), Этим названием <и формулой обозначается целый ряд углеводородов (этан - С2Н 6 , пропан - С 3 Нв, бутан- С4Н 10 и др.), низшая теплотворная способность этих газов колеблется от 15226 до 34890 ккал/нм*.
В негорючую часть газообразного топлива входят: углекислый газ (СО 2), кислород (О 2) и азот (N 2).
Негорючую часть газов принято называть балластом. Природные газы характеризуются высокой теплотворностью и полным отсутствием окиси углерода. В то же время (ряд месторождений, главным образом газонёфтяных, содержит очень ядовитый (и агрессивный в коррозионном отношении газ - сероводород (H 2 S). Большинство искусственных каменноугольных газов содержит значительное количество высокотоксичного газа - окиси углерода (СО). Наличие в газе окиси углерода и других ядовитых веществ весьма нежелательно, так как они усложняют производство эксплуатационных работ и повышают опасность при использовании газа. Кроме основных компонентов е состав газов входят различные примеси, удельное значение которых в процентном отношении ничтожно. Однако если учесть, что по газопроводам подаются тысячи и даже миллионы кубических метров газа, то суммарное количество примесей достигает значительной величины. Многие примеси выпадают в газопроводах, что в итоге приводит к снижению их пропускной способности, а иногда и к полному прекращению прохода газа. Поэтому наличие примесей в газе необходимо учитывать как при проектировании газопроводов, так и в процессе эксплуатации.
Количество и состав примесей зависят от способа производства или добычи газа и степени его очистки. Наиболее вредными примесями являются пыль, смола, нафталин, влага и сернистые соединения.
Пыль появляется в газе в процессе производства (добычи) или при транспортировке газа по трубопроводам. Смола является продуктом термического разложения топлива и сопутствует многим искусственным газам. При наличии в газе пыли смола способствует образованию смоло-грязевых пробок и закупорок газопроводов.
Нафталин обычно содержится в искусственных каменноугольных газах. При низких температурах нафталин выпадает в трубах и вместе с другими твердыми и жидкими примесями уменьшает проходное сечение газопроводов.
Влага в виде паров содержится почти во всех естественных и искусственных газах. В естественные газы она попадает в самом газовом месторождении вследствие контактов газов с поверхностью воды, а искусственные газы насыщаются водой в процессе "производства. Наличие влаги в газе в значительных количествах нежелательно, так как она понижает теплотворную способность газа. Кроме того, отличаясь большой теплоемкостью парообразования, влага при сжигании газа уносит значительное количество тепла вместе с продуктами сгорания в атмосферу. Большое содержание влаги о газе нежелательно еще и потому, что, конденсируясь при охлаждении газа во "Бремя движения его по трубам, она может создавать водяные пробки в газопроводе (в низших точках),которые необходимо удалять. Для этого требуется установка специальных конденсатосборников и откачка их.
К сернистым соединениям, как уже отмечалось, относятся сероводород, а также сероуглерод, меркаптан и др. Эти соединения не только вредно действуют на здоровье людей, но и вызывают значительную коррозию труб.
Из других вредных примесей следует отметить аммиак и цианистые соединения, которые содержатся главным образом в каменноугольных газах. Наличие аммиака и цианистых соединений приводит к увеличенной коррозии металла труб.
Присутствие в горючих газах углекислого газа и азота также нежелательно. Эти газы в процессе горения не участвуют, являясь балластом, уменьшающим теплотворную способность, что приводит к увеличению диаметра газопроводов и к снижению экономической эффективности использования газообразного топлива.
Состав газов, используемых для городского газоснабжения, должен удовлетворять требованиям ГОСТ 6542-50 (табл. 1).
Таблица 1
Средние значения состава естественных газов наиболее известных месторождений страны представлены в табл. 2.
Из газовых месторождений (сухие)
| Западная Украина. . . | 81,2 | 7,5 | 4,5 | 3,7 | 2,5 | - . | 0,1 | 0,5 | 0,735 | |
| Шебелинское............................... | 92,9 | 4,5 | 0,8 | 0,6 | 0,6 | ____ . | 0,1 | 0,5 | 0,603 | |
| Ставропольский край. . | 98,6 | 0,4 | 0,14 | 0,06 | - | 0,1 | 0,7 | 0,561 | ||
| Краснодарский край. . | 92,9 | 0,5 | - | 0,5 | _ | 0,01 | 0,09 | 0,595 | ||
| Саратовское............................... | 93,4 | 2,1 | 0,8 | 0,4 | 0,3 | Следы | 0,3 | 2,7 | 0,576 | |
| Газли, Бухарской области | 96,7 | 0,35 | 0,4" | 0,1 | 0,45 | 0,575 | ||||
| Из газонефтяных месторождений (попутные) | ||||||||||
| Ромашкино............................... | 18,5 | 6,2 | 4,7 | 0,1 | 11,5 | 1,07 | ||||
| 7,4 | 4,6 | ____ | Следы | 1,112 | __ . | |||||
| Туймазы............................... | 18,4 | 6,8 | 4,6 | ____ | 0,1 | 7,1 | 1,062 | - | ||
| Зольный....... | 23,5 | 9,3 | 3,5 | ____ | 0,2 | 4,5 | 1,132 | - | ||
| Жирное.......... ............................ . | 2,5 | . ___ . | 1,5 | 0,721 | - | |||||
| Сызрань-нефть............................... | 31,9 | 23,9 - | 5,9 | 2,7 | 0,8 | 1,7 | 1,6 | 31,5 | 0,932 | - |
| Ишимбай............................... | 42,4 | 20,5 | 7,2 | 3,1 | 2,8 | 1,040 | _ | |||
| Андижан. ............................... | 66,5 | 16,6 | 9,4 | 3,1 | 3,1 | 0,03 | 0,2 | 4,17 | 0,801 ; | |
Теплотворная способность газов
Количество тепла, выделяемое при полном сгорании единицы количества топлива, называется теплотворной способностью (Q) или, как иногда говорят, теплотворностью, или калорийностью, которая является одной из основных характеристик топлива.
Теплотворную способность газов обычно относят к 1 м 3 , взятому при нормальных условиях.
При технических расчетах под нормальными условиями понимается состояние газа при температуре, равной 0°С, и, при давлении 760 мм рт. ст. Объем газа при этих условиях обозначается нм 3 (нормальный метр кубический).
Для промышленных измерений газа по ГОСТ 2923-45 за нормальные условия приняты температура 20°С и Давление 760 мм рт. ст. Объем газа, отнесенный к этим условиям, в отличие от нм 3 будем называть м 3 (метр кубический).
Теплотворная способность газов (Q}) выражается в ккал/нм э или в ккал/м 3 .
Для сжиженных газов теплотворную способность относят к 1 кг.
Различают высшую (Q в) и низшую (Q н) теплотворность. Высшая теплотворная способность учитывает теплоту конденсации водяных паров, образующихся при сжигании топлива. Низшая теплотворная способность не учитывает тепло, содержащееся в водяных парах продуктов сгорания, так как водяные лары не конденсируются, а уносятся с продуктами сгорания.
Понятия Q в и Q н относятся только к тем газам, при сгорании которых выделяются водяные пары (к окиси углерода, не дающей при сгорании паров воды, эти понятия не относятся).
При конденсации водяных паров выделяется тепло, равное 539 ккал/кг. Кроме того, при охлаждении конденсата до 0°С (.или 20°С) соответственно выделяется тепло в количестве 100 или 80 ккал/кг.
Всего за счет конденсации водяных паров выделяется тепла более 600 ккал/кг, что составляет разность между высшей и низшей теплотворной способностью газа. Для большинства газов, применяемых в городском газоснабжении, эта разность равна 8-10%.
Значения теплотворных способностей некоторых газов приведены в табл. 3.
Для городского газоснабжения в настоящее время используют газы, имеющие, как правило, теплотворность не менее 3500 ккал/нм 3 . Объясняется это тем, что в условиях городов газ подается по трубам на значительные расстояния. При низкой теплотворности его требуется подавать большое количество. Это неизбежно ведет к увеличению диаметров газоцроводов и как следствие к увеличению металловложений и средств на строительство газовых сетей, а.в.последующем: и к увеличению затрат на эксплуатацию. Существенным недостатком низкокалорийных газов является еще то, что в большинстве случаев они содержат значительное количество окиси углерода, из-за чего повышается опасность при использовании газа, а также при обслуживании сетей и установок.
Газ теплотворной способностью менее 3500 ккал/нм 3 наиболее часто используют в промышленности, где не требуется транспортировать его на большие расстояния и проще организовать сжигание. Для городского газоснабжения теплотворность газа желательно иметь постоянной. Колебания, как мы уже установили, допускаются не более 10%. Большее изменение теплотворной способности газа требует новой регулировки, а иногда и смены большого количества унифицированных горелок бытовых приборов, что связано со значительными трудностями.
Теплота сгорания определяется химическим составом горючего вещества. Содержащиеся в горючем веществе химические элементы обозначаются принятыми символами С , Н , О , N , S , а зола и вода - символами А и W соответственно.
Энциклопедичный YouTube
-
1 / 5
Теплота сгорания может быть отнесена к рабочей массе горючего вещества Q P {\displaystyle Q^{P}} , то есть к горючему веществу в том виде, в каком оно поступает к потребителю; к сухой массе вещества Q C {\displaystyle Q^{C}} ; к горючей массе вещества Q Γ {\displaystyle Q^{\Gamma }} , то есть к горючему веществу, не содержащему влаги и золы.
Различают высшую ( Q B {\displaystyle Q_{B}} ) и низшую ( Q H {\displaystyle Q_{H}} ) теплоту сгорания.
Под высшей теплотой сгорания понимают то количество теплоты, которое выделяется при полном сгорании вещества, включая теплоту конденсации водяных паров при охлаждении продуктов сгорания.
Низшая теплота сгорания соответствует тому количеству теплоты, которое выделяется при полном сгорании, без учёта теплоты конденсации водяного пара. Теплоту конденсации водяных паров также называют скрытой теплотой парообразования (конденсации) .
Низшая и высшая теплота сгорания связаны соотношением: Q B = Q H + k (W + 9 H) {\displaystyle Q_{B}=Q_{H}+k(W+9H)} ,
где k - коэффициент, равный 25 кДж/кг (6 ккал/кг); W - количество воды в горючем веществе, % (по массе); Н - количество водорода в горючем веществе, % (по массе).
Расчёт теплоты сгорания
Таким образом, высшая теплота сгорания - это количество теплоты, выделившейся при полном сгорании единицы массы или объема (для газа) горючего вещества и охлаждении продуктов сгорания до температуры точки росы. В теплотехнических расчетах высшая теплота сгорания принимается как 100 %. Скрытая теплота сгорания газа - это теплота, которая выделяется при конденсации водяных паров, содержащихся в продуктах сгорания. Теоретически она может достигать 11 %.
На практике не удается охладить продукты сгорания до полной конденсации, и потому введено понятие низшей теплоты сгорания (QHp), которую получают, вычитая из высшей теплоты сгорания теплоту парообразования водяных паров как содержащихся в веществе, так и образовавшихся при его сжигании. На парообразование 1 кг водяных паров расходуется 2514 кДж/кг (600 ккал/кг). Низшая теплота сгорания определяется по формулам (кДж/кг или ккал/кг):
Q H P = Q B P − 2514 ⋅ ((9 H P + W P) / 100) {\displaystyle Q_{H}^{P}=Q_{B}^{P}-2514\cdot ((9H^{P}+W^{P})/100)} (для твердого вещества)
Q H P = Q B P − 600 ⋅ ((9 H P + W P) / 100) {\displaystyle Q_{H}^{P}=Q_{B}^{P}-600\cdot ((9H^{P}+W^{P})/100)} (для жидкого вещества), где:
2514 - теплота парообразования при температуре 0 °C и атмосферном давлении, кДж/кг;
H P {\displaystyle H^{P}} и W P {\displaystyle W^{P}} - содержание водорода и водяных паров в рабочем топливе, %;
9 - коэффициент, показывающий, что при сгорании 1 кг водорода в соединении с кислородом образуется 9 кг воды.
Теплота сгорания является наиболее важной характеристикой топлива, так как определяет количество тепла, получаемого при сжигании 1 кг твердого или жидкого топлива или 1 м³ газообразного топлива в кДж/кг (ккал/кг). 1 ккал = 4,1868 или 4,19 кДж.
Низшая теплота сгорания определяется экспериментально для каждого вещества и является справочной величиной. Также её можно определить для твердых и жидких материалов, при известном элементарном составе, расчётным способом в соответствии с формулой Д. И. Менделеева, кДж/кг или ккал/кг:
Q H P = 339 ⋅ C P + 1256 ⋅ H P − 109 ⋅ (O P − S L P) − 25.14 ⋅ (9 ⋅ H P + W P) {\displaystyle Q_{H}^{P}=339\cdot C^{P}+1256\cdot H^{P}-109\cdot (O^{P}-S_{L}^{P})-25.14\cdot (9\cdot H^{P}+W^{P})}
Q H P = 81 ⋅ C P + 246 ⋅ H P − 26 ⋅ (O P + S L P) − 6 ⋅ W P {\displaystyle Q_{H}^{P}=81\cdot C^{P}+246\cdot H^{P}-26\cdot (O^{P}+S_{L}^{P})-6\cdot W^{P}} , где:
C P {\displaystyle C_{P}} , H P {\displaystyle H_{P}} , O P {\displaystyle O_{P}} , S L P {\displaystyle S_{L}^{P}} , W P {\displaystyle W_{P}} - содержание в рабочей массе топлива углерода, водорода, кислорода, летучей серы и влаги в % (по массе).
Для сравнительных расчётов используется так называемое Топливо условное , имеющее удельную теплоту сгорания, равную 29308 кДж/кг (7000 ккал/кг).
В России тепловые расчёты (например, расчёт тепловой нагрузки для определения категории помещения по взрывопожарной и пожарной опасности ) обычно ведут по низшей теплоте сгорания, в США, Великобритании, Франции - по высшей. В Великобритании и США до внедрения метрической системы мер удельная теплота сгорания измерялась в британских тепловых единицах (BTU) на фунт (lb) (1Btu/lb = 2,326 кДж/кг).
Вещества и материалы Низшая теплота сгорания Q H P {\displaystyle Q_{H}^{P}} , МДж/кг Бензин 41,87 Керосин 43,54 Бумага: книги, журналы 13,4 Древесина (бруски W = 14%) 13,8 Каучук натуральный 44,73 Линолеум поливинилхлоридный 14,31 Резина 33,52 Волокно штапельное 13,8 Полиэтилен 47,14 Пенополистирол 41,6 Хлопок разрыхленный 15,7 Пластмасса 41,87 В таблицах представлена массовая удельная теплота сгорания топлива (жидкого, твердого и газообразного) и некоторых других горючих материалов. Рассмотрено такое топливо, как: уголь, дрова, кокс, торф, керосин, нефть, спирт, бензин, природный газ и т. д.
Перечень таблиц:
При экзотермической реакции окисления топлива его химическая энергия переходит в тепловую с выделением определенного количества теплоты. Образующуюся тепловую энергию принято называть теплотой сгорания топлива. Она зависит от его химического состава, влажности и является основным . Теплота сгорания топлива, отнесенная на 1 кг массы или 1 м 3 объема образует массовую или объемную удельную теплоты сгорания.
Удельной теплотой сгорания топлива называется количество теплоты, выделяемое при полном сгорании единицы массы или объема твердого, жидкого или газообразного топлива. В Международной системе единиц эта величина измеряется в Дж/кг или Дж/м 3 .
Удельную теплоту сгорания топлива можно определить экспериментально или вычислить аналитически. Экспериментальные методы определения теплотворной способности основаны на практическом измерении количества теплоты, выделившейся при горении топлива, например в калориметре с термостатом и бомбой для сжигания. Для топлива с известным химическим составом удельную теплоту сгорания можно определить по формуле Менделеева .
Различают высшую и низшую удельные теплоты сгорания. Высшая теплота сгорания равна максимальному количеству теплоты, выделяемому при полном сгорании топлива, с учетом тепла затраченного на испарение влаги, содержащейся в топливе. Низшая теплота сгорания меньше значения высшей на величину теплоты конденсации , который образуется из влаги топлива и водорода органической массы, превращающегося при горении в воду.
Для определения показателей качества топлива, а также в теплотехнических расчетах обычно используют низшую удельную теплоту сгорания , которая является важнейшей тепловой и эксплуатационной характеристикой топлива и приведена в таблицах ниже.
Удельная теплота сгорания твердого топлива (угля, дров, торфа, кокса)
В таблице представлены значения удельной теплоты сгорания сухого твердого топлива в размерности МДж/кг. Топливо в таблице расположено по названию в алфавитном порядке.
Наибольшей теплотворной способностью из рассмотренных твердых видов топлива обладает коксующийся уголь — его удельная теплота сгорания равна 36,3 МДж/кг (или в единицах СИ 36,3·10 6 Дж/кг). Кроме того высокая теплота сгорания свойственна каменному углю, антрациту, древесному углю и углю бурому.
К топливам с низкой энергоэффективностью можно отнести древесину, дрова, порох, фрезторф, горючие сланцы. Например, удельная теплота сгорания дров составляет 8,4…12,5, а пороха — всего 3,8 МДж/кг.
Удельная теплота сгорания твердого топлива (угля, дров, торфа, кокса)
Топливо Антрацит 26,8…34,8 Древесные гранулы (пиллеты) 18,5 Дрова сухие 8,4…11 Дрова березовые сухие 12,5 Кокс газовый 26,9 Кокс доменный 30,4 Полукокс 27,3 Порох 3,8 Сланец 4,6…9 Сланцы горючие 5,9…15 Твердое ракетное топливо 4,2…10,5 Торф 16,3 Торф волокнистый 21,8 Торф фрезерный 8,1…10,5 Торфяная крошка 10,8 Уголь бурый 13…25 Уголь бурый (брикеты) 20,2 Уголь бурый (пыль) 25 Уголь донецкий 19,7…24 Уголь древесный 31,5…34,4 Уголь каменный 27 Уголь коксующийся 36,3 Уголь кузнецкий 22,8…25,1 Уголь челябинский 12,8 Уголь экибастузский 16,7 Фрезторф 8,1 Шлак 27,5 Удельная теплота сгорания жидкого топлива (спирта, бензина, керосина, нефти)
Приведена таблица удельной теплоты сгорания жидкого топлива и некоторых других органических жидкостей. Следует отметить, что высоким тепловыделением при сгорании отличаются такие топлива, как: бензин, дизельное топливо и нефть.
Удельная теплота сгорания спирта и ацетона существенно ниже традиционных моторных топлив. Кроме того, относительно низким значением теплоты сгорания обладает жидкое ракетное топливо и — при полном сгорании 1 кг этих углеводородов выделится количество теплоты, равное 9,2 и 13,3 МДж, соответственно.
Удельная теплота сгорания жидкого топлива (спирта, бензина, керосина, нефти)
Топливо Удельная теплота сгорания, МДж/кг Ацетон 31,4 Бензин А-72 (ГОСТ 2084-67) 44,2 Бензин авиационный Б-70 (ГОСТ 1012-72) 44,1 Бензин АИ-93 (ГОСТ 2084-67) 43,6 Бензол 40,6 Дизельное топливо зимнее (ГОСТ 305-73) 43,6 Дизельное топливо летнее (ГОСТ 305-73) 43,4 Жидкое ракетное топливо (керосин + жидкий кислород) 9,2 Керосин авиационный 42,9 Керосин осветительный (ГОСТ 4753-68) 43,7 Ксилол 43,2 Мазут высокосернистый 39 Мазут малосернистый 40,5 Мазут низкосернистый 41,7 Мазут сернистый 39,6 Метиловый спирт (метанол) 21,1 н-Бутиловый спирт 36,8 Нефть 43,5…46 Нефть метановая 21,5 Толуол 40,9 Уайт-спирит (ГОСТ 313452) 44 Этиленгликоль 13,3 Этиловый спирт (этанол) 30,6 Удельная теплота сгорания газообразного топлива и горючих газов
Представлена таблица удельной теплоты сгорания газообразного топлива и некоторых других горючих газов в размерности МДж/кг. Из рассмотренных газов наибольшей массовой удельной теплотой сгорания отличается . При полном сгорании одного килограмма этого газа выделится 119,83 МДж тепла. Также высокой теплотворной способностью обладает такое топливо, как природный газ — удельная теплота сгорания природного газа равна 41…49 МДж/кг (у чистого 50 МДж/кг).
Удельная теплота сгорания газообразного топлива и горючих газов (водород, природный газ, метан)
Топливо Удельная теплота сгорания, МДж/кг 1-Бутен 45,3 Аммиак 18,6 Ацетилен 48,3 Водород 119,83 Водород, смесь с метаном (50% H 2 и 50% CH 4 по массе) 85 Водород, смесь с метаном и оксидом углерода (33-33-33% по массе) 60 Водород, смесь с оксидом углерода (50% H 2 50% CO 2 по массе) 65 Газ доменных печей 3 Газ коксовых печей 38,5 Газ сжиженный углеводородный СУГ (пропан-бутан) 43,8 Изобутан 45,6 Метан 50 н-Бутан 45,7 н-Гексан 45,1 н-Пентан 45,4 Попутный газ 40,6…43 Природный газ 41…49 Пропадиен 46,3 Пропан 46,3 Пропилен 45,8 Пропилен, смесь с водородом и окисью углерода (90%-9%-1% по массе) 52 Этан 47,5 Этилен 47,2 Удельная теплота сгорания некоторых горючих материалов
Приведена таблица удельной теплоты сгорания некоторых горючих материалов ( , древесина, бумага, пластик, солома, резина и т. д.). Следует отметить материалы с высоким тепловыделением при сгорании. К таким материалам можно отнести: каучук различных типов, пенополистирол (пенопласт), полипропилен и полиэтилен.
Удельная теплота сгорания некоторых горючих материалов
Топливо Удельная теплота сгорания, МДж/кг Бумага 17,6 Дерматин 21,5 Древесина (бруски влажностью 14 %) 13,8 Древесина в штабелях 16,6 Древесина дубовая 19,9 Древесина еловая 20,3 Древесина зеленая 6,3 Древесина сосновая 20,9 Капрон 31,1 Карболитовые изделия 26,9 Картон 16,5 Каучук бутадиенстирольный СКС-30АР 43,9 Каучук натуральный 44,8 Каучук синтетический 40,2 Каучук СКС 43,9 Каучук хлоропреновый 28 Линолеум поливинилхлоридный 14,3 Линолеум поливинилхлоридный двухслойный 17,9 Линолеум поливинилхлоридный на войлочной основе 16,6 Линолеум поливинилхлоридный на теплой основе 17,6 Линолеум поливинилхлоридный на тканевой основе 20,3 Линолеум резиновый (релин) 27,2 Парафин твердый 11,2 Пенопласт ПХВ-1 19,5 Пенопласт ФС-7 24,4 Пенопласт ФФ 31,4 Пенополистирол ПСБ-С 41,6 Пенополиуретан 24,3 Плита древесноволокнистая 20,9 Поливинилхлорид (ПВХ) 20,7 Поликарбонат 31 Полипропилен 45,7 Полистирол 39 Полиэтилен высокого давления 47 Полиэтилен низкого давления 46,7 Резина 33,5 Рубероид 29,5 Сажа канальная 28,3 Сено 16,7 Солома 17 Стекло органическое (оргстекло) 27,7 Текстолит 20,9 Толь 16 Тротил 15 Хлопок 17,5 Целлюлоза 16,4 Шерсть и шерстяные волокна 23,1 Источники:
- ГОСТ 147-2013 Топливо твердое минеральное. Определение высшей теплоты сгорания и расчет низшей теплоты сгорания.
- ГОСТ 21261-91 Нефтепродукты. Метод определения высшей теплоты сгорания и вычисление низшей теплоты сгорания.
- ГОСТ 22667-82 Газы горючие природные. Расчетный метод определения теплоты сгорания, относительной плотности и числа Воббе.
- ГОСТ 31369-2008 Газ природный. Вычисление теплоты сгорания, плотности, относительной плотности и числа Воббе на основе компонентного состава.
- Земский Г. Т. Огнеопасные свойства неорганических и органических материалов: справочник М.: ВНИИПО, 2016 — 970 с.
Газовое топливо делится на природное и искусственное и представляет собой смесь горючих и негорючих газов, содержащую некоторое количество водяных паров, а иногда пыли и смолы. Количество газового топлива выражают в кубических метрах при нормальных условиях (760 мм рт. ст. и 0°С), а состав - в процентах по объему. Под составом топлива понимают состав его сухой газообразной части.
Природное газовое топливо
Наиболее распространенное газовое топливо - это природный газ, обладающий высокой теплотой сгорания. Основой природного газа является метан, содержание которого 76,7-98%. Другие газообразные соединения углеводородов входят в состав природного газа от 0,1 до 4,5%.
Сжиженный газ продукт переработки нефти - состоит в основном из смеси пропана и бутана.
Природный газ (CNG, NG): метан CH4 более 90%, этан C2 H5 менее 4%, пропан C3 H8 менее 1%
Сжиженный газ (LPG): пропан C3 H8 более 65%, бутан C4 H10 менее 35%
В состав горючих газов входят: водород Н 2 , метан СН 4 , Другие углеводородные соединения С m Н n , сероводород Н 2 S и негорючие газы, двуокись углерода СО2, кислород О 2 , азот N 2 и незначительное количество водяных паров Н 2 О. Индексы m и п при С и Н характеризуют соединения различных углеводородов, например для метана СН 4 т = 1 и n = 4, для этана С 2 Н б т = 2 и n = б и т. д.
Состав сухого газообразного топлива (в процентах по объему):
СО + Н 2 + 2 С m Н n + Н 2 S + СO 2 + O 2 + N 2 = 100%.Негорючую часть сухого газового топлива - балласт - составляют азот N и двуокись углерода СО 2 .
Состав влажного газообразного топлива выражают следующим образом:
СО + Н 2 + Σ С m Н n + Н 2 S + СО 2 + O 2 + N 2 + Н 2 О = 100%.
Теплоту сгорания, кДж/м (ккал/м 3), 1 м 3 чистого сухого газа при нормальных условиях определяют следующим образом:
Q н с = 0,01 ,
где Qсо, Q н 2 , Q с m н n Q н 2 s. - теплота сгорания отдельных газов, входящих в состав смеси, кДж/м 3 (ккал/м 3); СО, Н 2 , Cm Н n , Н 2 S - компоненты, составляющие газовую смесь, % по объему.
Теплота сгорания 1 м3 сухого природного газа при нормальных условиях для большинства отечественных месторождений составляет 33,29 - 35,87 МДж/м3 (7946 - 8560 ккал/м3). Характеристика газообразного топлива приведена в таблице 1.
Пример. Определить низшую теплоту сгорания природного газа (при нормальных условиях) следующего состава:
Н 2 S = 1%; СН 4 = 76,7%; С 2 Н 6 = 4,5%; С 3 Н 8 = 1,7%; С 4 Н 10 = 0,8%; С 5 Н 12 = 0,6%.
Подставляя в формулу (26) характеристики газов из таблицы 1, получим:
Q нс = 0,01 = 33981 кДж/м 3 или
Q нс = 0,01 (5585,1 + 8555 76,7 + 15 226 4,5 + 21 795 1,7 + 28 338 0,8 + 34 890 0,6) = 8109 ккал/м 3 .
Таблица 1. Характеристика газообразного топлива
Газ
Обозначение
Теплота сгорания Q н с
КДж/м3
Ккал/м3
Водород Н, 10820 2579 Окисьуглерода СО 12640 3018 Сероводород Н 2 S 23450 5585 Метан СН 4 35850 8555 Этан С 2 Н 6 63 850 15226 Пропан С 3 Н 8 91300 21795 Бутан С 4 Н 10 118700 22338 Пентан С 5 Н 12 146200 34890 Этилен С 2 Н 4 59200 14107 Пропилен С 3 Н 6 85980 20541 Бутилен С 4 Н 8 113 400 27111 Бензол С 6 Н 6 140400 33528 Котлы типа ДЕ потребляют от 71 до 75 м3 природного газа на получение одной тонны пара. Стоимость газа в России на сентябрь 2008г. составляет 2,44 рубля за кубометр. Следовательно, тонна пара будет стоить 71 × 2,44 = 173 руб 24 коп. Реальная стоимость тонны пара на заводах составляет для котлов ДЕ составляет не менее 189 рублей за тонну пара.
Котлы типа ДКВР потребляют от 103 до 118 м3 природного газа на получение одной тонны пара. Минимальная расчетная стоимость тонны пара для этих котлов составляет 103 × 2,44 = 251 руб 32 коп. Реальная же стоимость пара по заводам составляет не менее 290 рублей за тонну.
Как рассчитать максимальный расход природного газа на паровой котел ДЕ-25? Это техническая характеристика котла. 1840 кубиков в час. Но можно и расчитать. 25 тонн (25 тыс кг) надо умножить на разность энтальпий пара и воды (666,9-105) и всё это разделить на к.п.д котла 92,8% и теплоту сгорания газа. 8300. и все
Искусственное газовое топливо
Искуственные горючие газы являются топливом местного значения, поскольку имеют значительно меньшую теплоту сгорания. Основными горючими элементами их являются окись углерода СО и водород Н2. Эти газы используют в пределах того производства, где они получаются в качестве топлива технологических и энергетических установок.
Все природные и искусственные горючие газы являются взрывоопасными, способны воспламеняться на открытом огне или искре. Различают нижний и верхний предел взрываемости газа, т.е. наибольшую и наименьшую процентную его концентрацию в воздухе. Нижний предел взрываемости природных газов колеблется от 3% до 6%, а верхний - от 12% до 16%. Все горючие газы способны вызывать отравление организма человека. Основными отравляющими веществами горючих газов являются: окись углерода СО, сероводород H2S, аммиак NH3.
Природные горючие газы, так и искусственные бесцветны (невидимы), не имеют запаха, что делает их опасными при проникновении во внутреннее помещение котельной через неплотности газопроводной арматуры. Во избежание отравления горючие газы следует обрабатывать одорантом - веществом с неприятным запахом.
Получение окиси углерода СО в промышленности газификацией твердого топлива
Для промышленных целей окись углерода получают путём газификации твёрдого топлива, т. е. превращения его в газообразное топливо. Так можно получить окись углерода из любого твёрдого топлива - ископаемых углей, торфа, дров и т. д.
Процесс газификации твердого топлива показан на лабораторном опыте (рис.1). Заполнив тугоплавкую трубку кусочками древесного угля, сильно нагреем её и будем пропускать кислород из газометра. Выходящие из трубки газы пропустим через промывалку с известковой водой и затем подожжём. Известковая вода мутится, газ горит синеватым пламенем. Это указывает на наличие двуокиси СО2 и окиси углерода СО в продуктах реакции.
Образование этих веществ можно объяснить тем, что при соприкосновении кислорода с раскалённым углем последний сначала окисляется в двуокись углерода: С + О 2 = СО 2
Затем, проходя через раскалённый уголь, углекислый газ частично восстанавливается им до окиси углерода: СО 2 + С = 2СО
Рис. 1. Получение окиси углерода (лабораторный опыт).
В промышленных условиях газификацию твёрдого топлива осуществляют в печах, называемых газогенераторами.
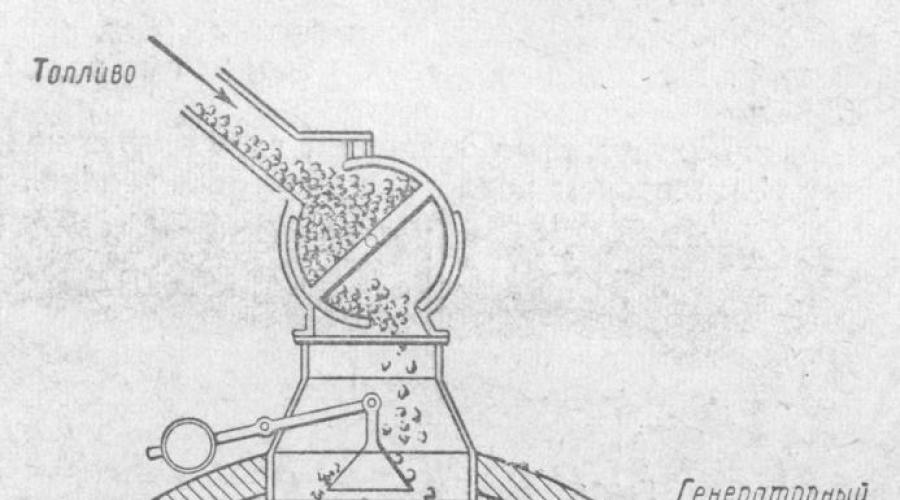
Образующаяся смесь газов называется генераторным газом.
Устройство генератора газа показано на рисунке. Он представляет собой стальной цилиндр высотой около 5 м и диаметром примерно 3,5 м, футерованный внутри огнеупорным кирпичом. Сверху газогенератор загружается топливом; снизу через колосниковую решётку вентилятором подаётся воздух или водяной пар.
Кислород воздуха реагирует с углеродом топлива, образуя углекислый газ, который, поднимаясь вверх через слой раскалённого топлива, восстанавливается углеродом до окиси углерода.
Если в генератор вдувать только воздух, то получается газ, который в своём составе содержит окись углерода и азот воздуха (а также некоторое количество СО 2 и других примесей) . Такой генераторный газ называется воздушным газом.
Если же в генератор с раскалённым углем вдувать водяной пар, то в результате реакции образуются окись углерода и водород: С + Н 2 О = СO + Н 2
Эта смесь газов называется водяным газом. Водяной газ обладает более высокой теплотворной способностью, чем воздушный, так как в его состав наряду с окисью углерода входит и второй горючий газ - водород. Водяной газ (синтез газ), один из продуктов газификациии топлив. Водяной газ состоит главным образом из СО (40%) и Н2 (50%). Водяной газ - это топливо (теплота сгорания 10 500 кДж/м3, или 2730 ккал/мг) и одновременно сырье для синтеза метилового спирта. Водяной газ, однако, нельзя получать продолжительное время, так как реакция образования его эндотермическая (с поглощением теплоты), и поэтому топливо в генераторе остывает. Чтобы поддерживать уголь в раскалённом состоянии, вдувание водяного пара в генератор чередуют с вдуванием воздуха, кислород которого, как известно, реагирует с топливом с выделением тепла.
В последнее время для газификации топлива стали широко применять парокислородное дутьё. Одновременное продувание через слой топлива водяного пара и кислорода позволяет вести процесс непрерывно, значительно повышать производительность генератора и получать газ с высоким содержанием водорода и окиси углерода.
Современные газогенераторы - это мощные аппараты непрерывного действия.
Чтобы при подаче топлива в газогенератор горючие и ядовитые газы не проникали в атмосферу, загрузочный барабан делают двойным. В то время как топливо поступает в одно отделение барабана, из другого отделения топливо высыпается в генератор; при вращении барабана эти процессы повторяются, генератор же всё время остаётся изолированным от атмосферы. Равномерное распределение топлива в генераторе осуществляется при помощи конуса, который может устанавливаться на различной высоте. Когда его опускают, уголь ложится ближе к центру генератора, когда конус поднимают, уголь отбрасывается ближе к стенкам генератора.
Удаление золы из газогенератора механизировано. Колосниковая решётка, имеющая конусовидную форму, медленно вращается электродвигателем. При этом зола смещается к стенкам генератора и особыми приспособлениями сбрасывается в зольный ящик, откуда периодически удаляется.
Первые газовые фонари зажглись в Санкт-Петербурге на Аптекарском острове в 1819 году. Газ, который применялся, получали путем газификации каменного угля. Он назывался светильным газом.
Великий русский учёный Д. И. Менделеев (1834-1907) впервые высказал идею о том, что газификацию каменного угля можно производить непосредственно под землёй, не поднимая его наружу. Царское правительство не оценило этого предложения Менделеева.
Идею подземной газификации горячо поддержал В. И. Ленин. Он назвал её «одной из великих побед техники». Подземную газификацию осуществило впервые Советское государство. Уже до Великой Отечественной войны в Советском Союзе работали подземные генераторы в Донецком и Подмосковном угольных бассейнах.
Представление об одном из способов подземной газификации даёт рисунок 3. В угольный пласт прокладывают две скважины, которые внизу соединяют каналом. Уголь поджигают в таком канале у одной из скважин и подают туда дутьё. Продукты горения, двигаясь по каналу, взаимодействуют с раскалённым углем, в результате чего образуется горючий газ как и в обычном генераторе. Газ выходит на поверхность через вторую скважину.
Генераторный газ широко применяется для обогрева промышленных печей - металлургических, коксовых и в качестве топлива в автомобилях (рис. 4).
Рис. 3. Схема подземной газификации каменного угля.
Из водорода и окиси углерода водяного газа синтезируют ряд органических продуктов, например жидкое топливо. Синтетическое жидкое топливо - горючее (в основном бензин), получаемое синтезом из окиси углерода и водорода при 150-170 гр Цельсия и давлении 0,7 - 20 МН/м2 (200 кгс/см2), в присутствии катализатора (никель, железо, кобальт). Первое производство синтетического жидкого топлива организовано в Германии во время 2й Мировой войны в связи с нехваткой нефти. Широкого распространения синтетическое жидкое топливо не получило из-за его высокой стоимости. Водяной газ используют для производства водорода. Для этого водяной газ в смеси с водяным паром нагревают в присутствии катализатора и в результате получают водород дополнительно к уже имеющемуся в водяном газе: СО+Н 2 О=СО 2 +Н 2