Описание элемента по положению в периодической системе. Характеристика элемента по его положению в псхэ презентация к уроку по химии (9 класс) на тему
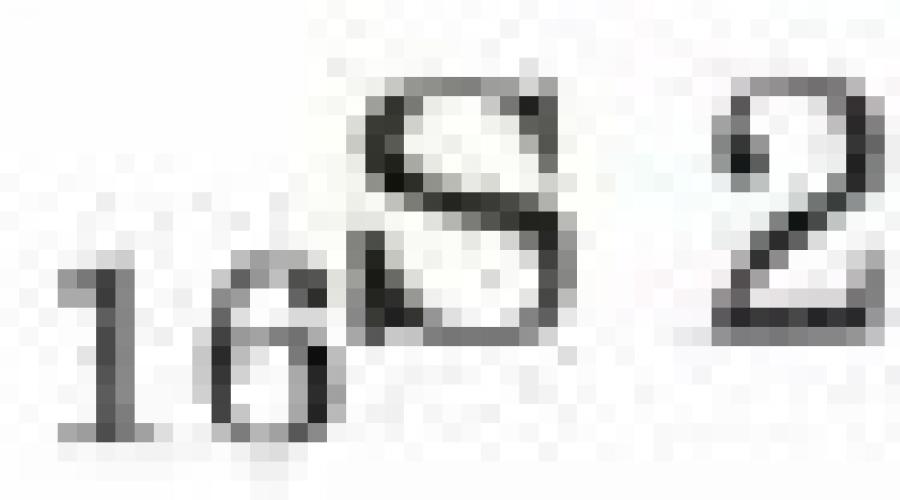
Как и литературным героям, химическим элементам - «героям» химических процессов дают характеристики. Только если для первых в качестве первоисточника используют литературное произведение, то для вторых - Периодическую систему химических элементов Д. И. Менделеева. Однако и в первом, и во втором случае необходим план.
Характеризуя химический элемент, будем придерживаться следующего плана.
- Положение элемента в Периодической системе Д. И. Менделеева и строение его атомов.
- Характер простого вещества (металл, неметалл).
- Сравнение свойств простого вещества со свойствами простых веществ, образованных соседними по подгруппе элементами.
- Сравнение свойств простого вещества со свойствами простых веществ, образованных соседними по периоду элементами.
- Состав высшего оксида, его характер (основный, кислотный, амфотерный).
- Состав высшего гидроксида, его характер (кислородсодержащая кислота, основание, амфотерный гидроксид).
- Состав летучего водородного соединения (для неметаллов).
В приведённом плане для вас незнакомыми являются следующие химические понятия: переходные металлы, амфотерные оксиды и гидроксиды. Их смысл будет раскрыт в следующем параграфе. Пока же рассмотрим характеристики металла и неметалла.
При этом будем руководствоваться уже известными вам из курса 8 класса основными закономерностями изменения свойств атомов, простых веществ и соединений, образованных химическими элементами главных подгрупп (А групп) и периодов Периодической системы Д. И. Менделеева (табл. 1).
Таблица 1
Закономерности изменения свойств атомов, простых веществ и соединений, образованных химическими элементами, в пределах главных подгрупп и периодов Периодической системы Д. И. Менделеева
|
Формы существования химического элемента и их свойства |
Изменения свойств |
||
|
в главных подгруппах ↓ |
в периодах → |
||
|
Заряд ядра |
Увеличивается |
Увеличивается |
|
|
Число заполняемых энергетических уровней |
Увеличивается |
Не изменяется и равно номеру периода |
|
|
Число электронов на внешнем уровне |
Не изменяется и равно номеру группы |
У величивается |
|
|
Радиус атома |
Увеличивается |
Уменьшается |
|
|
Восстанови-
|
Усиливаются |
Ослабевают |
|
|
Окислительные
|
Ослабевают |
Усиливаются |
|
|
Высшая степень окисления |
Постоянная и равна номеру группы (N) |
У величивается от +1 до +7 (+8) |
|
|
Низшая степень окисления |
Не изменяется и равна (8-N) |
Увеличивается от -4 до -1 |
|
|
Простые
|
Металлические
|
Усиливаются |
Ослабевают |
|
Неметаллические свойства |
Ослабевают |
Усиливаются |
|
|
Соеди-
|
Характер
|
Усиление
|
Основный ->
Усиление кислотных свойств и ослабление основных Щёлочь -> Нерастворимое основание ->
|
Характеристика металла на примере магния.
1. Магний имеет порядковый номер в Периодической системе Z - 12 и массовое число А - 24. Соответственно заряд ядра его атома +12 (число протонов). Следовательно, число нейтронов в ядре равно N = А - Z = 12. Так как атом электронейтрален, то число электронов, содержащихся в атоме магния, тоже равно 12.
Элемент магний находится в 3-м периоде Периодической системы, значит, все электроны атома располагаются на трёх энергетических уровнях. Строение электронной оболочки атома магния можно отразить с помощью следующей схемы:
Исходя из строения атома, можно предсказать и степень окисления магния в его соединениях. В химических реакциях атом магния отдаёт два внешних электрона, проявляя восстановительные свойства, следовательно, он получает степень окисления +2.
Восстановительные свойства у магния выражены сильнее, чем у бериллия, но слабее, чем у кальция (элементы IIA группы), что связано с увеличением радиусов атомов при переходе от Be к Mg и Са. Соответственно в ряду Be - Mg - Са два внешних электрона всё более удаляются от ядра, ослабевает их связь с ядром, и они всё легче покидают атом, который при этом переходит в ион М 2+ (М - металл).
2. Для магния - простого вещества - характерна металлическая кристаллическая решётка и металлическая химическая связь, а отсюда и все типичные для металлов свойства (вспомните какие).
3. Металлические свойства у магния выражены сильнее, чем у бериллия, но слабее, чем у кальция (объясните почему, учитывая, что металлические свойства определяются в первую очередь способностью атомов отдавать электроны).
4. Металлические свойства у магния выражены слабее, чем у натрия, но сильнее, чем у алюминия (соседние элементы 3-го периода) (объясните почему).
5. Оксид магния MgO является основным оксидом и проявляет все типичные свойства основных оксидов {вспомните какие).
6. В качестве гидроксида магнию соответствует основание Mg(OH) 2 , которое проявляет все характерные свойства оснований (вспомните какие).
7. Летучего водородного соединения магний не образует.
Характеристика неметалла на примере серы.
1. Сера - элемент VIA группы и 3-го периода, Z = 16, А = 32. Соответственно атом серы содержит в ядре 16 протонов и 16 нейтронов и на электронной оболочке - 16 электронов. Строение его электронной оболочки можно отразить с помощью следующей схемы:
![]()
Атомы серы проявляют как окислительные свойства (принимают недостающие для завершения внешнего уровня два электрона, получая при этом степень окисления -2, например в соединениях с металлами или менее электроотрицательными элементами-неметаллами - водородом, углеродом и т. п.), так и восстановительные свойства (отдают 2, 4 или все 6 внешних электронов более электроотрицательным элементам, например кислороду, галогенам, приобретая при этом степени окисления +2, +4, +6).
Сера - менее сильный окислитель, чем кислород, но более сильный, чем селен, что связано с увеличением радиусов атомов от кислорода к селену. По этой же причине восстановительные свойства элементов в главной подгруппе VI группы (VIA группы) при переходе от кислорода к селену усиливаются. {Дайте объяснения указанных изменений окислительных и восстановительных свойств.)
2. Сера - простое вещество, типичный неметалл. Сере свойственно явление аллотропии. Разные простые вещества, образованные химическим элементом серой, имеют различные свойства, так как кристаллическое строение их различно. Например, у ромбической серы молекулярная кристаллическая решётка состоит из циклических молекул состава S 8 , а у пластической серы молекулы представляют собой длинные открытые цепи атомов:

3. Неметаллические свойства у серы выражены слабее, чем у кислорода, но сильнее, чем у селена.
4. Неметаллические свойства у серы выражены сильнее, чем у фосфора, но слабее, чем у хлора (соседние элементы в 3-м периоде).
5. Высший оксид серы имеет формулу SO 2 . Это кислотный оксид. Он проявляет все типичные свойства кислотных оксидов {какие?).
6. Высший гидроксид серы - хорошо известная вам серная кислота H 2 SO 4 , раствор которой проявляет все типичные свойства кислот {какие?).
7. Сера образует летучее водородное соединение - сероводород H 2 S.
Подобные характеристики можно привести для большинства элементов-металлов и элементов-неметаллов главных подгрупп. На их основе можно составить генетические ряды металла и неметалла.
Генетический ряд металла:
Генетический ряд неметалла:
Новые слова и понятия
- План характеристики химического элемента.
- Характеристика элемента-металла.
- Характеристика элемента-неметалла.
- Генетические ряды металла и неметалла.
Задания для самостоятельной работы
- Дайте характеристику элементов: а) фосфора; б) калия.
- Запишите уравнения химических реакций, характеризующие свойства: a) MgO и SO 3 ; б) Mg(OH) 2 и H 2 SO 4 . Уравнения реакций с участием электролитов запишите также в ионной форме.
- Дайте характеристику магния - простого вещества. Какой тип связи наблюдается в нём? Какие физические свойства имеет металл магний? Запишите уравнения реакций магния со следующими веществами: а) кислородом; б) хлором Сl 2 ; в) серой; г) азотом N 2 ; д) соляной кислотой. Рассмотрите их с позиций процессов окисления-восстановления.
- Что такое аллотропия? Какой тип химической связи реализуется в молекулах состава: a) S 8 ; б) H 2 S? Какие физические свойства имеет наиболее устойчивая модификация серы - ромбическая сера? Запишите уравнения реакций серы со следующими веществами: а) натрием; б) кальцием; в) алюминием; г) кислородом; д) водородом; е) фтором F 2 . Рассмотрите их с позиций процессов окисления-восстановления.
- Сравните свойства простого вещества кремния со свойствами простых веществ, образованных химическими элементами - соседями кремния по периоду.
- У высшего оксида какого химического элемента наиболее выражены кислотные свойства: а) азота или фосфора; б) фосфора или серы?
- Вычислите объём воздуха (примите объёмную долю кислорода в нём равной 0,2), который потребуется для сжигания 120 мг образца магния, содержащего 2% негорючих примесей.
- Вычислите объём оксида серы (IV) (н. у.), который может быть получен при сжигании 1,6 кг серы, если выход продукта составляет 80% от теоретически возможного.
Указание . Сначала по уравнению реакции рассчитайте объём оксида серы (IV) - это теоретический объём V теор, затем найдите практический объём V практ, исходя из известного выхода продукта W:
W = V практ: V теор, отсюда V практ = W V теор.
Аналогично можно найти массу продукта реакции, используя формулу:
W = m практ: m теор, отсюда m практ = W m теор.
- Можно ли утверждать, что высшему оксиду серы SO 3 соответствует сернистая кислота H 2 SO 3 ? Почему?
- Используя метод электронного баланса, определите коэффициенты в схемах химических реакций:
а) Mg + СO 2 -> MgO + С;
б) S + КСlO 3 -> КСl + SO 2 .
Закономерности изменения некоторых свойств химических элементов в ПС. ХарактеристикаВ пределах периодаВ пределах одной группы (для элементов главных подгрупп) Заряд ядра атома Увеличивается Число энергетических уровней Не изменяется Увеличивается Число электронов на внешнем энергетическом уровне Увеличивается Не изменяется Радиус атома Уменьшается Увеличивается Электроотрицательность УвеличиваетсяУменьшается Восстановительные свойства Уменьшаются Увеличиваются Металлические свойства Уменьшаются Увеличиваются

Натрий Хлор Заряд ядра Число нуклоновp=11, n=12p=17,n=18 Число электроновe=11E=17 Число энергетических уровней 33 Электронная формула 1s 2 2s 2 2p 6 3s 1 1s 2 2s 2 2p 6 3s 2 3p 5 Высшая степень окисления+1+7 Окислительно-восстановительные свойства Восстановитель Окислитель 1. Положение элемента в ПС и строение его атома




Натрий Хлор Оксид натрия Na2O проявляет основные свойства. Ему соответствует основание NaOH. Na 2 O + H 2 O = 2NaOH Na 2 O + 2HCl = 2NaCl + H 2 O Na 2 O + SO 3 = Na 2 SO 4 Высший оксид хлора Cl2O7 является кислотным оксидом. Ему соответствует кислота HClO4. Cl 2 O 7 + H 2 O = 2HClO 4 Cl 2 O 7 + Na 2 O = 2NaClO 4 Cl 2 O 7 + 2NaOH = 2NaClO 4 + H 2 O
Натрий Хлор Гидроксид натрия NaOH, является сильным основанием и проявляет свойства, характерные для основания. NaOH + HCl = NaCl + H2O 2NaOH + CO2 = Na2CO3 + H2O 2NaOH + CuCl2 = Cu(OH)2 + 2NaCl Хлорная кислота HClO4 проявляет свойства сильной кислоты. HClO2 + KOH = KClO4 + H2O


(от др.-греч. αλλος «другой», τροπος «поворот, свойство») существование одного и того же химического элемента в виде двух и более простых веществ, различных по строению и свойствам так называемых аллотропических модификаций или аллотропических форм.др.-греч.химического элемента простых веществ

Вопрос 1.
А) Характеристика фосфора.
1. Фосфор - элемент пятой группы и третьего периода, Z = 15,
Соответственно, атом фосфора содержит в ядре 15 протонов, 16
Нейтронов и 15 электронов. Строение его электронной оболочки
Можно отразить с помощью следующей схемы:
15Р 2ё; 8ё; 5ё.
Атомы фосфора проявляют как окислительные свойства (принимают недостающие для завершения внешнего уровня три электрона, получая при этом степень окисления -3, например, в соединениях с менее электроотрицательными элементами - металлами, водородом и т. п.) так и восстановительные свойства (отдают 3 или 5 электронов более электроотрицательным элементам - кислороду, галогенам и т. п., приобретая при этом степени окисления +3 и+5.)
Фосфор менее сильный окислитель, чем азот, но более сильный, чем мышьяк, что связано с ростом радиусов атомов от азота к мышьяку. По этой же причине восстановительные свойства, наоборот, усиливаются.
2. Фосфор- простое вещество, типичный неметалл. Фосфору свойственно явление аллотропии. Например, существуют аллотропные модификации фосфора такие, как белый, красный и черный фосфор, которые обладают разными химическими и физическими свойствами. 3. Неметаллические свойства фосфора выражены слабее, чем у азота, но сильнее, чем у мышьяка (соседние элементы в группе).
4. Неметаллические свойства фосфора выражены сильнее, чем у кремния, но слабее, чем у серы (соседние элементы в периоде). 5. Высший оксид фосфора имеет формулу Р205. Это кислотный оксид. Он проявляет все типичные свойства кислотных оксидов. Так, например, при взаимодействии его с водой получается фосфорная кислота.
Р205 + ЗН20 =*2Н3Р04.
При взаимодействии его с основными оксидами и основаниями он дает соли.
Р205 + 3MgO = Mg3(P04)2; Р205 + 6КОН = 2К3Р04+ ЗН20.
6. Высший гидроксид фосфора - фосфорная кислота Н3Р04,
Раствор которой проявляет все типичные свойства кислот:
Взаимодействие с основаниями и основными оксидами:
Н3Р04 + 3NaOH = Na3P04 + ЗН20. 2Н3Р04 + ЗСаО = Ca3(P04)2i + ЗН20.
7. Фосфор образует летучее соединение Н3Р - фосфин.
Б) Характеристика калия.
1. Калий имеет порядковый номер 19, Z = 19 и относительную
Атомную массу А,(К) = 39. Соответственно заряд ядра его атома +19
(равен числу протонов). Следовательно, число нейтронов в ядре
Равно 20. Так как атом электронейтрален, то число электронов,
Элемент калий находится в четвертом периоде периодической системы, значит, все электроны располагаются на четырех энергетических уровнях. Таким образом, строение атома калия записывается так:
19К: 2ё; 8ё; 8ё; 1ё.
Исходя из строения атома, можно предсказать степень окисления калия в его соединениях. Так как в химических реакциях атом калия отдает один внешний электрон, проявляя восстановительные свойства, следовательно, он приобретает степень окисления +1.
Восстановительные свойства у калия выражены сильнее, чем у натрия, но слабее, чем у рубидия, что связано с ростом радиусов от Na к Rb.
2. Калий - простое вещество, для него характерна металлическая
Кристаллическая решетка и металлическая химическая связь, а
Отсюда - и все типичные для металлов свойства.
3. Металлические свойства у калия выражены сильнее, чем у натрия, но слабее, чем у рубидия, т. к. атом калия легче отдает электрон, чем атом натрия, но труднее, чем атом рубидия.
4. Металлические свойства у калия выражены сильнее, чем у кальция, т. к. один электрон атома калия легче оторвать, чем два электрона атома кальция.
5. Оксид калия КгО является основным оксидом и проявляет все типичные свойства основных оксидов. Взаимодействие с кислотами и кислотными оксидами.
К20 + 2НС1 = 2КС1+Н20; К20 + S03 = K2S04.
6. В качестве гидроксида калию соответствует основание (щелочь) КОН, которое проявляет все характерные свойства оснований: взаимодействие с кислотами и кислотными оксидами.
KOH+HNO3 = KN03+H20; 2KOH+N205 = 2KN03+H20.
7. Летучего водородного соединения калий не образует, а образует гидрид калия КН.
Вопрос 2.
А) MgO - основной оксид, S03 - кислотный оксид.
1) MgO + S03 = MgS04;
2) MgO + 2HNO3 = Mg(N03)2 + H20;
3) MgO + 2H+ = Mg + + H20; 2RbOH + S03 = Rb2S04 + H20; S03 + 20РГ = S04 ~ + H20.
Б) Mg(OH)2 - основной гидроксид, H2S04 - кислотный гидроксид.
1) Mg(OH)2 + H2S04 = MgS04 + 2H20; OH~ + H+ = H20;
2) Mg(OH)2 + S03 = MgS04 + H20; S03 + 20РГ = H20 + S04"; I) H2b04 + Na20 = Na2b04 + H20; Na20 + 2H = 2Na + H20.
Вопрос 3.
Магний - простое вещество, для него характерна металлическая кристаллическая решетка; он обладает металлическим блеском, электропроводностью.
A) 2Mg + 02 = 2MgO
6) Mg + Cl2 = MgCl2 Mg°-2e = Mg2+ 1
Вопрос 4.
Аллотропия - явление существования химического элемента в
Виде нескольких простых веществ, различных по строению и
Свойствам (так называемых аллотропных форм).
А) В молекулах состава S8 реализуется ковалентно-неполярный тип
Связи (т. е. не происходит смещения электронной пары, образующей
Б) В молекулах состава H2S реализуется ковалентно-полярный тип связи, т. к. происходит смещение электронной пары к более электроотрицательному атому - сере (S).
Н->S <- Н
Физические свойства ромбической серы (S8):
Вещество лимонно-желтого цвета, устойчивое до t = 95,6°С, растворяется в сероуглероде (CS2), анилине, бензоле, феноле. Уравнения реакций:
A) 2Na + S = Na2S
Восстановитель
Са°-2" =еСа2+
B)S2Al + 3l=Al2S3 А1°-Зё=А12
Е) S + 3F2 = SF6 6
1 - восстановитель 1 - окислитель
Восстановитель 1 - окислитель
1 - восстановитель 3 - окислитель
Вопрос 5.
Неметаллические свойства кремния выражены слабее, чем у фосфора, но сильнее, чем у алюминия.
Вопрос 6.
А) У азота кислотные свойства выражены сильнее, чем у фосфора,
Т. к. в группах сверху вниз происходит усиление основных и
Ослабление кислотных свойств.
Б) У серы кислотные свойства выражены сильнее, чем у фосфора,
Т. к. в периодах слева направо происходит усиление кислотных и
Ослабление основных свойств.
Вопрос 7. Дано : Ti(0 2) = 0,2; m(Mg) = 0,12г; Юм8(примеси) = 2 %. Найти : V (воздуха)
Р^ние : 1. Найдем массу магния без примеси: тчистый(Ме) = т(Ме) - т(Ме)-Юм0 (примеси); тчистый (Mg) =0,121-0,12г-0,02 = 0,1176г.
2. Запишем уравнение реакции сжигания магния. ОД 176 г.
2Mg + 02 = 2MgO,
У=2моль; у=1моль;
М = 24 г/моль; Vv = 22,4 л/моль;
Шуравнению реакции составим пропорцию: 48 г -22,4 л 0,1176 г -хл
Х = °"1176"22"4 = 0,05488 л. 48
Следовательно, 0,05488 л чистого кислорода требуется на сжигание
0,1176 г магния.
3. Найдем объем воздуха, который потребуется на сжигание магния:
У(воздуха) = X(°ll = 0,05488 = 0,2744 л.
Ответ : У(воздуха) = 0,2744 л.
Вопрос 8.
Дано : m(S) = 1.6 кг -1600 г.
Найти : V(S02)
Решение : 1. Запишем уравнение реакции сжигания серы в кислороде.
1 £(\(\ Г VTT
1. Дайте характеристику элементов: а) фосфора; б) калия.

2. Запишите уравнения химических реакций, и характеризующие свойства: Уравнения реакций с участием электролитов запишите также в ионной форме.

3. Дайте характеристику магния - простого вещества. Какой тип связи наблюдается в нем? Какие физические свойства имеет металл магний? Запишите уравнения реакция магния со следующими веществами: а) кислородом; б) хлором Cl2; в) серой; г) азотом N2; д) соляной кислотой. Рассмотрите их с позиций процессов окисления-восстановления.
Магний— простое вещество, дня него характерна металлическая кристаллическая решетка; он обладает металлическим блеском, электропроводностью.

4. Что такое аллотропия? Какой тип химической связи реализуется в молекулах состава: a) S8; б) H2S? Какие физические свойства имеет наиболее устойчивая модификация серы — ромбическая сера? Запишите уравнения реакций серы со следующими веществами: а) натрием; б) кальцием; в) алюминием; г) кислородом; д) водородом; е) фтором F2. Рассмотрите их с позиций процессов окисления-восстановления.
Аллотропия — явление существования химического элемента в виде нескольких простых веществ, различных по строению и свойствам (так называемых аллотропных форм).

5. Сравните свойства простого вещества кремния со свойства-ми простых веществ, образованных химическими элементами — соседями кремния по периоду.
Неметаллические свойства кремния выражены слабее, чем у фосфора, но сильнее, чем у алюминия.
6. У высшего оксида какого химического элемента наиболее выражены кислотные свойства: а) азота или фосфора, б) фосфора или серы?
а) У азота кислотные свойства выражены сильнее, чем у фосфора, т. к. в группах сверху вниз происходит усиление основных и ослабление кислотных свойств.
б) У серы кислотные свойства выражены сильнее, чем у фосфора, т. к. в периодах слева направо происходит усиление кислотных и ослабление основных свойств.
7. Вычислите объем воздуха (примите объемную долю кислорода в нем равной 0,2), который потребуется для сжигания 120 мг образца магния, содержащего 2% негорючих примесей.

8. Вычислите объем оксида серы (IV) (н. у.), который может быть получен при сжигании 1,6 кг серы, если выход продукта составляет 80% от теоретически возможного.


9. Можно ли утверждать, что высшему оксиду серы SO3 соответствует сернистая кислота H2SO3? Почему?
