Ионный обмен. Иониты и их классификация
Читайте также
Обменная емкость
Для количественной характеристики ионообменных и сорбционных свойств ионитов применяют следующие величины: полная, динамическая и рабочая обменная емкость.
Полная обменная емкость (ПОЕ ) определяется числом функциональных групп, способных к ионному обмену, в единице массы воздушно-сухого или набухшего ионита и выражается в мг-экв/г или мг-экв/л. Она является постоянной величиной, которую указывают в паспорте ионита, и не зависит от концентрации или природы обменивающегося иона. ПОЕ может изменяться (уменьшаться) из-за термического, химического или радиационного воздействия. В реальных условиях эксплуатации ПОЕ уменьшается со временем вследствие старения матрицы ионита, необратимого поглощения ионов-отравителей (органики, железа и т. п.), которые блокируют функциональные группы.
Равновесная (статическая) обменная емкость зависит от концентрации ионов в воде, рН и отношения объемов ионита и раствора при измерениях. Необходима для проведения расчетов технологических процессов.
Динамическая обменная емкость (ДОЕ ) - важнейший показатель в процессах водоподготовки. В реальных условиях многократного применения ионита в цикле сорбции-регенерации обменная емкость используется не полностью, а лишь частично.
Степень использования определяется методом регенерации и расходом регенерирующего агента, временем контакта ионита с водой и с регенерирующим агентом, концентрацией солей, рН, конструкцией и гидродинамикой используемого аппарата. На рисунке показано, что процесс очистки воды прекращают при определенной концентрации лимитирующего иона, как правило, задолго до полного насыщения ионита. Количество поглощенных при этом ионов, соответствующее площади прямоугольника А, отнесенное к объему ионита, и будет ДОЕ.
Количество поглощенных ионов, соответствующее полному насыщению, когда проскок равен 1, соответствующее сумме ДОЕ и площади заштрихованной фигуры над S -образной кривой, называют полной динамической обменной емкостью (ПДОЕ). В типовых процессах водоподготовки ДОЕ обычно не превышает 0,4-0,7 ПОЕ.
Рис. 1
Экспериментальная часть
Реагенты и растворы: соли MgCl2*6H2O в дистиллированной воде в мерной колбе ёмкостью 250 см З
Раствор 1 нитрата кальция (0.02М) готовили растворением навески (1.18 г.) соли Са(NО3)2·4Н20. После растворения навески раствор разбавили в дистиллированной воде в мерной колбе ёмкостью 250 см З.
Раствор 2 нитрата кальция (О.1М) готовили растворением навески (5.09г.) соли Са(NО3)2·4Н20. После растворения навески раствор разбавили в дистиллированной воде в мерной колбе ёмкостью 250 см З.
Исходный раствор комплексона III готовили из фиксанала. Стандартизацию проводили по сульфату магния.
Буферные растворы готовили из NH4Cl “ч.д.а.” и NH4OH.
Остаточную концентрацию ионов Mg 2+ определяли комплексонометрически с индикатором эриохромом черным Т.
Остаточную концентрацию ионов Ca 2+ определяли комплексонометрически с индикатором мурексидом.
Сорбированную концентрацию находили по разности между исходной и остаточной.
В качестве сорбента использовали цеолитсодержащую породу Атяшевского проявления.
Приготовление сорбента.
ЦСП Атяшевского проявления дробили, просеивали, собирали фракции гранул размером 1 - 2 - 3 мм и просушивали в сушильном шкафу.
Ионообменная емкость в статическом режиме. К 20 см З раствора, содержащего ионы Ca 2+ ,в другом случае Mg 2+ ,с известной концентрацией и
определённым значением рН прибавляли 5.0 г сорбента, встряхивали в течение заданного времени и отделяли твёрдую фазу фильтрованием. В
Селективность хелатометрического титрования в отношении кальция можно повысить, проводя определение в сильнощелочной среде (магний фильтрате определили остаточную концентрацию ионов Ca 2+ ,в другом случае Mg 2+ .Сорбированную концентрацию находили по разности между исходной и остаточной.
Металлохромного индикатора - мурексид.
ЭДТА, 0.05М раствор; аммиачная буферная смесь рН=9; NaOH, 2М раствор; индикаторы - эриохром чёрный Т И мурексид - твёрдые (смесь с NaCl в отношении 1: 100).
Методика определения
1. Пробу анализируемого раствора переносили в колбу для титрования, добавляли 10см 3 аммиачной буферной смеси (рН 9), 25 см 3 дистиллированной воды, на кончике шпателя 30 - 40 мг эриохром чёрного Т И перевешивали систему до полного растворения индикатора. Раствор приобрёл вино-красный цвет. Титрование раствором ЭДТА проводили по каплям из бюретки при непрерывном перемешивании до изменения окраски в четко синюю.
2. Пробу анализируемого раствора переносили в колбу для титрования, добавляли 5 см 3 2М раствора NaOH, 30 см 3 дистиллированной воды и на кончике шпателя 30 мг мурексида. Раствор приобрёл красный цвет. Титрование проводили раствором ЭДТА до перехода окраски в фиолетовую.
Вычисление статистических условиях по отношению к ионам кальция и магния.
Определение обменной ёмкости по магнию
К 20 см 3 раствора хлорида магния с молярной концентрацией эквивалента 0.02 моль/л прибавил и 5,0г сорбента, предварительно просушенного при 105 0 С в течение 1 часа и встряхивали в течение заданного времени (0.5 часа). В другом случае 1 час и так далее. По истечении времени раствор отфильтровали. Брали на анализ 5 см 3 фильтрата и определяли остаточную концентрацию ионов Mg 2+ комплексонометрическим методом.
2. К 20 см3 раствора хлорида кальция с молярной концентрацией эквивалента 0,l моль/л прибавили 5.0 г сорбента, предварительно просушенного при 1050C в течение 1 часа и встряхивали в течение заданного времени (0.5 часа). В другом случае 1 час и так далее. По истечении времени раствор отфильтровали. Брали на анализ 5 см3 фильтрата и определяли остаточную концентрацию ионов Ca2+ комплексонометрическим методом.
Влияние времени контакта ЦСП и раствора CaCl2 * 4Н2О на обменную ёмкость ЦСП в статических условиях.
(С(Са2+)исх = 0.1 моль/л;mцсп = 5.0 г.)
При увеличении времени контакта фаз наблюдается увеличение равновесной концентрации. А по истечении 3 часов устанавливается динамическое подвижное равновесие.
6. Ограничение срока действия снято по протоколу N 5-94 Межгосударственного Совета по стандартизации, метрологии и сертификации (ИУС 11-12-94)
7. ИЗДАНИЕ (январь 2002 г.) с Поправкой (ИУС 3-91)
Настоящий стандарт распространяется на иониты и устанавливает методы определения динамической обменной емкости с полной регенерацией ионита и с заданным расходом регенерирующего вещества.
Методы заключаются в определении количества ионов, поглощаемых из рабочего раствора единицей объема набухшего ионита при непрерывном протекании раствора через слой ионита.
1. МЕТОД ОТБОРА ПРОБ
1. МЕТОД ОТБОРА ПРОБ
1.1. Метод отбора проб указывают в нормативно-технической документации на конкретную продукцию.
1.2. Для ионитов, у которых массовая доля влаги менее 30%, отбирают пробу (100±10) г. Для набухания пробу помещают в стакан вместимостью 600 см и заливают насыщенным раствором хлористого натрия, который должен с избытком покрывать слой ионита с учетом его набухаемости. Через 5 ч ионит промывают дистиллированной водой.
1.3. Для ионитов с массовой долей влаги более 30% отбирают пробу (150±10) г в стакан вместимостью 600 см и приливают 200 см дистиллированной воды.
2. РЕАКТИВЫ, РАСТВОРЫ, ПОСУДА, ПРИБОРЫ
Вода дистиллированная по ГОСТ 6709 или деминерализованная, отвечающая требованиям ГОСТ 6709 .
Барий хлористый по ГОСТ 742 , х.ч., раствор с массовой долей 10%.
Кальций хлористый 2-водный, х.ч., растворы концентраций (СаСl=0,01 моль/дм (0,01 н.) и (СаСl)=0,0035 моль/дм (0,0035 н.).
Кислота соляная по ГОСТ 3118 , х.ч., растворы с массовой долей 5% и концентраций (НСl)=0,5 моль/дм (0,5 н.), (НСl)=0,1 моль/дм (0,1 н.) и (НСl)=0,0035 моль/дм (0,0035 н.).
Кислота серная по ГОСТ 4204 , х.ч., растворы с массовой долей 1%, концентрации (HSO)=0,5 моль/дм (0,5 н.).
Натрия гидроокись по ГОСТ 4328 , х.ч., растворы с массовой долей 2, 4, 5%, концентраций (NaOH)=0,5 моль/дм (0,5 н.), (NaOH)=0,1 моль/дм (0,1 н.), (NaOH)=0,0035 моль/дм (0,0035 н.).
Натрий хлористый по ГОСТ 4233 , х.ч., насыщенный раствор и раствор концентрации (NaCI)=0,01 моль/дм (0,01 н.).
Индикатор смешанный, состоящий из метилового красного и метиленового голубого или из метилового красного и бромкрезолового зеленого, готовят по ГОСТ 4919.1 .
Индикатор метиловый оранжевый или метиловый красный, раствор с массовой долей 0,1%, готовят по ГОСТ 4919.1 .
Индикатор фенолфталеин, спиртовой раствор с массовой долей 1%, готовят по ГОСТ 4919.1 .
Поглотитель химический известковый ХПИ-1 по ГОСТ 6755 или известь натронная.
Трубка (хлоркальциевая) по ГОСТ 25336 .
Мензурка 1000 по ГОСТ 1770 .
Цилиндры по ГОСТ 1770 исполнений 1-4 вместимостью 100 и 250 см и исполнений 1, 2 вместимостью 500 и 1000 см.
Стаканы В или Н по ГОСТ 25336 в любом исполнении вместимостью 600 и 1000 см.
Колбы Кн-1-250 по ГОСТ 25336 .
Пипетки 2-2-100, 2-2-25, 2-2-20 и 2-2-10 по НТД.
Бюретки по НТД типов 1, 2, исполнений 1-5, классов точности 1, 2, вместимостью 25 или 50 см, с ценой деления не более 0,1 см и бюретки типов 1, 2, исполнения 6, классов точности 1, 2, вместимостью 2 или 5 см, с ценой деления не более 0,02 см.
Колбы мерные исполнений 1, 2 по ГОСТ 1770 , классов точности 1, 2, вместимостью 10, 25 и 100 см.
Сито с контрольной сеткой 0315К по ГОСТ 6613 с обечайкой диаметром 200 мм.
Чашка ЧКЦ-5000 по ГОСТ 25336 или из полимеризационного материала, достаточная для помещения в нее сита.
Установка лабораторная (см. чертеж) состоит из бутыли 1 и стеклянной колонки 6 внутренним диаметром (25,0±1,0) мм и высотой не менее 600 мм для определения динамической обменной емкости в условиях полной регенерации ионита и внутренним диаметром (16,0±0,5) мм и высотой не менее 850 мм для определения в условиях заданного расхода регенерирующего вещества. В нижнюю часть колонки впаян фильтр 7 типа ФКП ПОР 250 ХС по ГОСТ 25336 или другое фильтрующее устройство, устойчивое к действию кислот и щелочей, не пропускающее зерен ионита размером более 0,25 мм и обладающее малым сопротивлением фильтрации. Колонку соединяют с бутылью с помощью стеклянной трубки 3 и резинового шланга 4 с винтовым зажимом 5. Для предотвращения попадания углекислого газа из воздуха в раствор гидроокиси натрия в пробку бутыли устанавливают хлоркальциевую трубку 2 с поглотителем ХПИ-1.
Лабораторная установка
Допускается применение других средств измерения с метрологическими характеристиками не хуже указанных, а также реактивов по качеству не ниже указанных.
3. МЕТОД ОПРЕДЕЛЕНИЯ ДИНАМИЧЕСКОЙ ОБМЕННОЙ ЕМКОСТИ С ПОЛНОЙ РЕГЕНЕРАЦИЕЙ ИОНИТА
3.1. Подготовка к испытанию
3.1.1. Подготовку к испытанию проводят по ГОСТ 10896 и после подготовки ионит хранят в закрытой колбе под слоем дистиллированной воды.
Катионит марки КУ-2-8чС и анионит марки АВ-17-8чС к испытанию по ГОСТ 10896 не готовят.
3.1.2. Пробу ионита из колбы в виде водной суспензии переносят в цилиндр вместимостью 100 см и уплотняют слой ионита постукиванием о твердую поверхность дна цилиндра до прекращения усадки. Объем ионита доводят до 100 см и с помощью дистиллированной воды переносят ионит в колонку, следя за тем, чтобы между гранулами ионита не попали пузырьки воздуха. Избыток воды из колонки сливают, оставляя над уровнем ионита слой высотой 1-2 см.
3.1.3. Ионит в колонке промывают дистиллированной водой, пропуская ее сверху вниз со скоростью 1,0 дм/ч. При этом анионит отмывают от щелочи (по фенолфталеину), а катионит от кислоты (по метиловому оранжевому).
3.1.4. Сильноосновные аниониты в гидроксильной форме быстро загружают и промывают водой, не содержащей углекислый газ.
3.2. Проведение испытания
3.2.1. Определение динамической обменной емкости ионитов состоит из нескольких циклов, каждый из которых включает три последовательные операции - насыщение, регенерацию, отмывку, условия проведения которых приведены в табл.1.
Таблица 1
Условия определения динамической обменной емкости с полной регенерацией ионита
Показатель | Класс ионитов | Рабочий раствор для насыщения ионитов | Контроль насыщения | Регенери- | |||
насыще- | отмыв- | регене- |
|||||
Динамическая обменная емкость до проскока () | Сильно- | Кальций хлористый (CaCl)=0,01 моль/дм (0,01 н.) | До концентрации ионов кальция в фильтрате (Са)=0,05 ммоль/дм (0,05 мг·экв/дм) определяют по ГОСТ 4151 | Соляная кислота, раствор с массовой долей 5% | |||
Сильно- | Натрий хлористый (NaCl)=0,01 моль/дм (0,01 н.) | До снижения концентрации щелочи на 0,5 ммоль/дм (0,5 мг·экв/дм) в сравнении с максимально устойчивым ее значением в фильтрате [индикатор смешанный, титрующий раствор, соляная кислота концентрации (НСl)=0,01 моль/дм (0,01 н.)] и до повышения содержания ионов хлора в сравнении с его устойчивым содержанием в фильтрате (определяют по ГОСТ 15615) | Гидроокись натрия, раствор с массовой долей 5% | ||||
Слабо- | До появления в фильтрате кислоты (по метиловому оранжевому) | ||||||
Полная динамическая обменная емкость () | Слабо- | Соляная кислота (НСl)=0,1 моль/дм (0,1 н.) | До уравнивания концентрации фильтрата с концентрацией рабочего раствора | Гидроокись натрия, раствор с массовой долей 2% | |||
Примечания:
1. При определении концентрации ионов Ca по ГОСТ 4151
2. Удельная нагрузка - это объем раствора, пропускаемый через объем ионита за 1 ч. Например, 5 дм/дм·ч соответствует скорости фильтрации, при которой через 100 см ионита за 1 ч проходит 500 см раствора (8,3 см/мин).
3. Скорость фильтрации устанавливают измерением в мерном цилиндре объема фильтрата, полученного за определенный интервал времени.
Растворы и воду подают сверху вниз. При насыщении анионита марок АН-1 и АН-2ФН растворы подают снизу вверх.
3.2.2 Перед проведением операций насыщения, регенерации и отмывки колонку заполняют соответствующим раствором. Слой раствора над ионитом должен быть (15±3) см.
3.2.3. После насыщения, регенерации и отмывки в колонке над ионитом оставляют слой жидкости высотой 1-2 см.
3.2.4. Колонку с ионитом заполняют рабочим раствором для конкретного класса ионита (см. табл.1) так, чтобы слой раствора над ионитом составлял (15±3) см, и выбирают соответствующую скорость фильтрации.
При пропускании через колонку с ионитом рабочих растворов концентрации 0,1 моль/дм (0,1 н.), фильтрат собирают в цилиндры вместимостью 250 см, при концентрации 0,01 моль/дм (0,01 н.) - в цилиндры вместимостью 1000 см. Во втором и последующих циклах насыщения перед появлением ионов рабочего раствора в фильтрате (определяют после первого цикла) фильтрат собирают порциями по 100 и 250 см соответственно концентрациям рабочего раствора.
3.2.5. От каждой порции фильтрата отбирают пробу и контролируют насыщение в соответствии с табл.1.
3.2.6. После появления в порции фильтрата ионов рабочего раствора вычисляют общий объем фильтрата.
3.2.7. Для определения полной динамической обменной емкости продолжают пропускать раствор до выравнивания концентрации фильтрата с концентрацией рабочего раствора. Контроль насыщения в этом случае проводят титрованием пробы раствором кислоты (гидроокиси натрия) со смешанным индикатором до изменения окраски.
3.2.8. Перед проведением регенерации ионит в колонке взрыхляют током дистиллированной воды снизу вверх так, чтобы все зерна ионита были в движении. Взрыхление катионита марки КУ-1 и анионитов марок АН-1 и АН-2ФН проводят перед операцией насыщения.
3.2.9. Регенерацию ионита проводят раствором кислоты (гидроокиси натрия) со скоростью, указанной в табл.1. Фильтрат непрерывно собирают порциями цилиндром объемом 250-1000 см, добавляя 3-4 капли индикатора. При появлении кислоты (гидроокиси натрия) в фильтрате в последующих порциях определяют ее концентрацию. Для контроля фильтрата отбирают пипеткой или мерной колбой пробу и титруют раствором кислоты (гидроокиси натрия) концентрации (НСl, HSO)=0,5 моль/дм (0,5 н.), (NaOH)=0,5 моль/дм (0,5 н.) в присутствии индикатор
3.2.10. Раствор кислоты (гидроокиси натрия) пропускают до уравнивания концентрации фильтрата с концентрацией регенерирующего раствора.
3.2.11. Ионит после регенерации промывают дистиллированной водой до нейтральной реакции по метиловому оранжевому (фенолфталеину) со скоростью, указанной в табл.1. Затем ионит выдерживают в дистиллированной воде в течение 1 ч и снова проверяют фильтрат. Если фильтрат не имеет нейтральной реакции, ионит промывают повторно.
3.2.12. Определение динамической обменной емкости заканчивают, если в двух последних циклах получены результаты, расхождение между которыми не превышает 5% среднего результата.
3.2.13. Динамическую обменную емкость анионита АВ-17-8чС определяют на двух параллельных пробах по первому циклу насыщения, перед появлением ионов рабочего раствора в фильтрате. Фильтрат собирают порциями по 250 см. За результат принимают среднее арифметическое результатов двух определений, допускаемое расхождение между которыми не превышает 5% среднего результата.
(Поправка, ИУС 3-91).
4. МЕТОД ОПРЕДЕЛЕНИЯ ДИНАМИЧЕСКОЙ ОБМЕННОЙ ЕМКОСТИ С ЗАДАННЫМ РАСХОДОМ РЕГЕНЕРИРУЮЩЕГО ВЕЩЕСТВА
4.1. Подготовка к испытанию
4.1.1. Ионит, отобранный в соответствии с пп.1.2 и 1.3, отделяют от мелких фракций методом мокрого рассева по ГОСТ 10900 , используя сито с сеткой N 0315К.
4.1.2. Отсеянный анионит помещают в стакан, приливают 500 см раствора гидроокиси натрия с массовой долей 4% и перемешивают. Через 4 ч раствор гидроокиси сливают, а анионит промывают водой до слабощелочной реакции по фенолфталеину и переносят в колонку, как указано в п.3.1.2.
4.1.3. Отсеянный катионит промывают от взвеси и мути дистиллированной водой декантацией до появления светлой промывной воды и переносят в колонку в соответствии с п.3.1.2.
4.2. Проведение испытания
4.2.1. Определение динамической обменной емкости ионитов до появления ионов рабочего раствора в фильтрате () состоит из нескольких циклов, каждый из которых включает три последовательные операции - насыщение, регенерацию, отмывку, условия проведения которых приведены в табл.2. Растворы и воду подают сверху вниз. Высоту слоя жидкости над уровнем ионита устанавливают, как указано в пп.3.2.2 и 3.2.3.
Таблица 2
Условия определения динамической обменной емкости ионитов при заданном расходе регенерирующего вещества
Класс ионитов | Регенери- | Норма удельного расхода регене- | Контроль отмывки | Рабочий раствор для насыщения ионита | Контроль насыщения | Скорость фильтрации |
||
насы- | отмывка | реге- |
||||||
Сильно | До остаточной концентрации кислоты в фильтрате не более | Кальций хлористый (СаСl=0,0035 моль/дм (0,0035 н.) | До концентрации ионов кальция в фильтрате более (Ca)=0,05 ммоль/дм | |||||
Слабо- | Серная кислота, раствор с массовой долей 1% | До отсутствия в фильтрате сульфатионов (проба с BaCl в присутствии НСl) | Гидроокись натрия (NaOH)=0,0035 моль/дм (0,0035 н.) | До концентрации в фильтрате гидроокиси натрия (NaOH)=0,1 ммоль/дм | ||||
Сильно- | Гидроокись натрия с массовой долей 4% | До остаточной концентрации гидроокиси натрия в фильтрате не более (NaOH)=0,2 ммоль/дм | Натрий хлористый (NaCI)=0,01 моль/дм (0,01 н.) | До снижения концентрации щелочи на (NaOH)=0,7 ммоль/дм | ||||
Слабо- | Гидроокись натрия, раствор с массовой долей 4% | До остаточной концентрации гидроокиси натрия в фильтрате не более (NaOH)=0,2 ммоль/дм (0,2 мг·экв/дм) по фенолфталеину | Соляная (серная) кислота (НСl,HSO)=0,0035 моль/дм (0,0035 н.) | До остаточной концентрации кислоты в фильтрате не более (Н)=0,1 ммоль/дм (0,1 мг·экв/дм), индикатор смешанный, титрующий раствор - гидроокись натрия концентрации (NaOH)=0,01 моль/дм (0,01 н.) | ||||
Примечания:
1. При выражении нормы удельного расхода регенерирующего вещества () в граммах на моль под словом "моль" имеется в виду молярная масса эквивалента иона (Na, K, Са, Mg, Сl, NO, НСО, HSO, СО, SO
И т.д.).
2. Фактический расход регенерирующего вещества не должен отличаться от заданной нормы более чем на 5%.
3. При определении концентрации ионов Са по ГОСТ 4151 допускается использование 2-3 капель индикатора хром-темно-синего и титрование раствором трилона Б концентрации (NaHCON·2HO)=0,01 моль/дм (0,01
4. Удельная нагрузка - это объем раствора, пропускаемый через объем ионита за 1 ч. Например, 5 дм/дм·ч соответствует скорости фильтрации, при которой через 100 см ионита за 1 ч проходит 500 см раствора (8,3 см/мин).
5. Скорость фильтрации устанавливают измерением в мерном цилиндре объема фильтрата, полученного за определенный интервал времени.
Во избежание загипсовывания катионита регенерацию кислотой и отмывку от продуктов регенерации проводят без остановок, не допуская разрыва между операциями.
Перед проведением каждого последующего цикла ионит взрыхляют током воды снизу вверх так, чтобы все зерна ионита были в движении.
4.2.2. Через ионит в колонке пропускают регенерирующий раствор, объем которого () в кубических сантиметрах вычисляют по формуле
где - заданная норма удельного расхода регенерирующего вещества, г/моль (г/г·экв);
- динамическая обменная емкость; выбирают по нормативно-технической документации на конкретный ионит, моль/м (г·экв/м); для ионитов марок АВ-17-8, АН-31 и ЭДЭ-10П допускается для первой регенерации увеличенное значение динамической обменной емкости до 3;
- объем пробы ионита, см;
- концентрация регенерирующего раствора, г/дм.
Количество регенерирующего раствора измеряют на выходе из колонки цилиндром или мензуркой. Затем колонку отсоединяют, уровень раствора над ионитом в колонке опускают до 1-2 см и закрывают нижний за
4.2.3. Иониты после регенерации промывают дистиллированной водой от избытка кислоты (гидроокиси натрия) со скоростью, указанной в табл.2.
Периодически отбирают пробу фильтрата и титруют растворами гидроокиси натрия (кислоты) концентрации (NaOH, HCl, HSO)=0,1 моль/дм (0,1 н.) в присутствии метилового оранжевого (фенолфталеина).
Отмывку контролируют по табл.2.
4.2.4. После отмывки колонку заполняют рабочим раствором и устанавливают по табл.2 скорость насыщения.
При пропускании через колонку рабочих растворов концентрации 0,01 моль/дм (0,01 н.) фильтрат собирают в цилиндр вместимостью 250 см, при концентрации 0,0035 моль/дм (0,0035 н.) используют цилиндр вместимостью 1000 см. Во втором и последующих циклах насыщения перед появлением ионов рабочего раствора в фильтрате (определяют после первого цикла) фильтрат собирают по 100 и 250 см соответственно концентрациям рабочего раствора.
4.2.5. Для контроля насыщения от порции фильтрата отбирают пробу и анализируют ее в соответствии с табл.2. Если результат анализа показывает, что уровень насыщения не достиг значений, указанных в табл.2, все предыдущие пробы фильтрата можно не анализировать.
4.2.6. После появления в порции фильтрата ионов рабочего раствора в количествах, указанных в табл.2, насыщение заканчивают и вычисляют общий объем фильтрата () и динамическую обменную емкость.
4.2.7. Ионит подвергают второй регенерации и отмывают в соответствии с пп.4.2.2 и 4.2.3.
При расчете регенерирующего вещества, необходимого для второго цикла, используют значение динамической обменной емкости, полученное в первом цикле в соответствии с п.4.2.6.
Перед проведением последующих циклов насыщения расход регенерирующего вещества вычисляют по величине динамической обменной емкости, полученной в предыдущем цикле.
4.2.8. Определение заканчивают, если в двух последних циклах получены результаты, допускаемые расхождения между которыми не превышают 5% среднего результата, при фактическом удельном расходе регенерирующего вещества, отличающемся от заданной нормы не более чем на 5%.
5. ОБРАБОТКА РЕЗУЛЬТАТОВ
5.1. Динамическую обменную емкость () в молях на кубический метр (г·экв/м) до появления ионов рабочего раствора в фильтрате вычисляют по формуле
где - общий объем фильтрата, пропущенный через ионит до появления ионов рабочего раствора, см;
- объем ионита, см.
5.2. Фактический расход регенерирующего вещества () в граммах на моль (г/г·экв) поглощенных ионов вычисляют по формуле
где - объем регенерирующего раствора, см;
- концентрация регенерирующего раствора, г/дм;
- общий объем фильтрата, пропущенного через ионит до появления ионов рабочего раствора, см;
- концентрация рабочего раствора, моль/дм (н.
5.3. Полную динамическую обменную емкость () в молях на кубический метр (г·экв/м) вычисляют по формуле
где - общий объем фильтрата, пропущенный через ионит до уравнивания концентраций фильтрата и рабочего раствора, см;
- концентрация рабочего раствора, моль/дм (н.);
- объем порции фильтрата после появления ионов рабочего раствора (проскока), см;
- концентрация раствора в порции фильтрата после появления ионов рабочего раствора (проскока), моль/дм (н.);
- объем ионита,
5.4. За результат определения принимают среднее арифметическое результатов двух последних циклов, допускаемые расхождения между которыми не превышают ±5%, при доверительной вероятности =0,95.
Примечание. При выражении динамической обменной емкости ионитов в молях на кубический метр под словом "моль" имеется в виду молярная масса эквивалента иона (Na, K, Ca, Mg, Сl, NO, НСО, HSO, CO, SO и т.д.).
Текст документа сверен по:
официальное издание
Иониты. Методы определения
обменной емкости: Сб. ГОСТов. -
М.: ИПК Издательство стандартов, 2002
Общие понятия
В общих словах, под емкостью ионообменной смолы понимается количество ионов, которое может быть поглощено определенным объемом смолы. Причем единицы измерения емкости смолы могут быть разными. Например, мг-экв/мл (meq/ml), г-экв/л (eq/l) или килогран на кубический фут (Kgr/ft3). Зная эквивалентную массу вещества, можно рассчитать емкость смолы. Эквивалентная масса вещества определяется как отношение молярной массы вещества к его валентности (строго говоря, к числу эквивалентности вещества). Например, молярный вес кальция равен 40 г./моль, а валентность 2, тогда эквивалентная масса равна 20 г./моль (40/2 = 20). Ионообменная смола с обменной емкостью 1,95 г.-экв/л способна извлечь из раствора 1,95 Ч 20 = 39 грамм на 1 литр смолы.
На практике обменная емкость смолы определяется в лабораториях титрованием. Через колонку, в которую помещена навеска катионита в водородной форме (H-форма), пропускают раствор гидроксида натрия (NaOH). Часть ионов Na+ обменивается на ионы водорода. Гидроксид натрия, не вступивший в реакцию с ионогенной группой смолы, оттитровывают кислотой. Вычитая из начальной концентрации гидроксида натрия концентрацию остаточную, можно определить емкость катионита. Другой способ определения обменной емкости ионита состоит в пропускании через слой смолы раствора хлористого кальция. Аналогичным образом определяется емкость анионообменной смолы (в OH-форме), через которую пропускают раствор кислоты.
Емкость смолы может быть измерена в мг-экв/мл (объемная) или мг-экв/г (весовая). Если определена емкость, выраженная в мг-экв/г (причем имеется в виду масса сухого ионита), то, зная влажность смолы, легко перейти к мг-экв/мл.
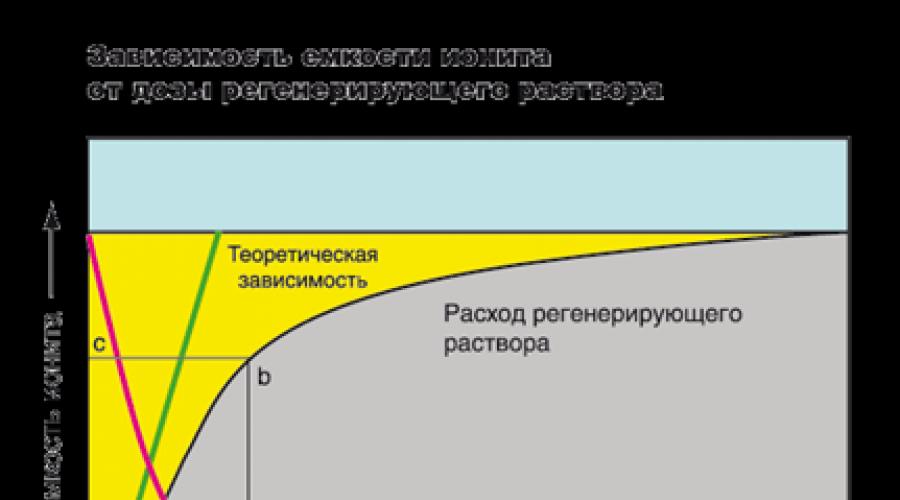
На рисунке обменная емкость смолы графически изображена областью желтого цвета, расположенную между вертикальными прямыми АN и СL. Область серого цвета, расположенная ниже кривой, - это концентрация ионов в очищенной воде. В начале цикла концентрация ионов в фильтрате очень мала, и остается постоянной на протяжении всего фильтроцикла, в момент, когда фронт фильтрования достигнет конца слоя ионита, наступает проскок ионов в фильтрат (на рисунке - точка Р). Это является сигналом к регенерации смолы. Обычно, регенерацию фильтра проводят до проскока. Например, в промышленности концентрация ионов жесткости, при которой фильтр выводят в регенерацию, может достигать величины менее 0,05 0Ж, а в бытовых системах умягчения - менее 0,5 0Ж. Длина отрезка x - y соответствует объему очищенной воды в литрах или галлонах. Площадь фигуры ANLB - полное поглощение ионов смолой, а площадь фигуры ANMB - количество поглощенных ионов до момента наступления проскока.
Говоря о емкости, мы чаще подразумеваем именно рабочую, а не полную обменную емкость. Рабочая емкость не является величиной постоянной, она зависит от множества факторов: марки ионита, концентрации и типа поглощаемых ионов, pH раствора, от требований, предъявляемых к очищенной воде, скорости потока, высоты слоя ионита и других требований.

Достижение высокой степени извлечения ионов из водного раствора требует увеличения дозы регенерирующего раствора (красная линия). Однако, увеличивать концентрацию регенерирующего раствора бесконечно невозможно (зеленая линия - теоретическая зависимость между степенью восстановления емкости смолы и расходом регенерирующего раствора). На практике, чтобы достигнуть высокую емкость, необходимо увеличивать количество смолы. При первом фильтроцикле степень восстановления ионообменных свойств может достигать 100%, но с течением времени эта величина будет уменьшаться. Например. большинство производителей систем умягчения воды рекомендуют использовать раствор NaCl концентрацией 100 - 125 г./л для восстановления емкости катионита до 50 - 55% от полной обменной емкости.
При определении емкости необходимо знать ионную форму смолы (солевая, кислотная, основная). При регенерации или в процессе работы объем засыпанной смолы меняется, происходит процесс, называемый «дыханием» смолы. В таблице показано, как ведут себя смолы в различных процессах.
Различают катиониты и аниониты. Реакции, в которых участвуют иониты приведены в таблице.
ионообменный смола реакция титрование

Причем, в англоязычной литературе символ SAC обозначает сильнокислотный катионит, SBA - сильноосновный анионит, WAC - слабокислотный катионит, а WBA - слабоосновный анионит. Способность к ионному обмену определяется наличием функциональной группы, сильнокислотные катиониты содержат сульфогруппу - SO3H, а слабокислотные катиониты карбоксильную группу - COOH. Сильнокислотные катиониты обмениваются катионами при любых значениях pH раствора, то есть ведут себя, как сильные кислоты в растворе. А слабокислотные катиониты подобны слабым кислотам и вступают в реакцию ионного обмена только при значениях pH выше 7. Аниониты содержат функциональные группы пяти типов: (-NH2, NH=, N?, - N(CH3) 3OH, - N(CH3) 2С2H4OH). Первые три группы придает аниониту слабоосновные свойства, а группы - N(CH3) 3OH, - N(CH3) 2С2H4OH - сильноосновные. Слабоосновыные аниониты вступают в реакции с анионами сильных кислот (SO, Cl-, NO), а сильноосновные с анионами сильных и слабых (HCO, HSiO) в диапазоне pH от 1 до 14. Говоря о емкости сильноосновного анионита, следует обратить внимание на то, что в смоле присутствуют функциональные группы, присущие и слабоосновным анионитам. При старении сильноосновного анионита или под действием высоких температур происходит снижение основности и частичное разрушение функциональных групп.
Рассмотрим подробнее реакции, протекающие с участием ионообменных смол. Реакция 1 - умягчение воды на сильнокислотном катионите в солевой (Na) форме, 2 - удаление нитрат-ионов на сильноосновном анионите в Cl-форме. Применение в качестве регенерирующего раствора хлорида натрия и хлорида калия способствует широкому применению этого типа смол в быту, промышленности и очистке сточных вод. Катиониты также могут восстанавливаться растворами кислот (например, соляная кислота), а аниониты - раствором едкого натра (NaOH). Иониты в H и OH-форме используют в схемах подготовки обессоленной воды (реакции 3 и 4). Слабокислотный катионит проявляет ионообменные свойства при высоких значениях pH (реакция 5), а слабоосновный анионит - при низких значениях pH (реакция 6). Реакция 5 - одновременное умягчение и снижение щелочности воды. Следует заметить, что WBA смола в результате регенерации щелочным раствором переходит не в OH-форму, а так называемую FB-форму (свободное основание).
Слабокислотные катиониты по сравнению с сильнокислотными обладают более высокой обменной емкостью, для них свойственно большое сродство к ионам водорода, поэтому регенерация протекает легче и быстрее. Важно, что для регенерации WAC, также как и WBA, не используют растворы хлористого натрия или калия. Выбор той или иной марки ионообменной смолы зависит от многих условий. Например, различают два типа сильноосновных анионитов: тип I (функциональная группа - N(CH3) 3OH) и тип II (-N(CH3) 2С2H4OH). Аниониты типа I лучше поглощают ионы HSiO в отличие от анионитов типа II, но при этом последние характеризуются более высокой обменной емкостью и лучше регенерируются.
В заключении заметим, что в литературе, а также в паспорте на продукцию указывается полная весовая и обменная емкость смолы, которые определяются в лаборатории. Рабочая емкость смолы ниже заявленной производителем и зависит от многих факторов, которые не могут быть учтены в лабораторных условиях (геометрические характеристики слоя смолы, конкретные условия процесса: скорости потоков, концентрации растворенных веществ, степень регенерации и т.д.).
Материалы ВИОН применяются для очистки вентиляционных отходящих газовых выбросов промышленности от растворимых компонентов, аэрозолей кислот и солей тяжелых металлов, где их используют главным образом в виде нетканых иглопробивных полотен.
Ход работы:
Взвесить 2 гр. катионита ВИОН КН-1 (сухого). Насыпать в бюретку. Пропускать через колонку заполненным катионитом исходный раствор CuCl 2 (3,6 ммоль/л). Далее отдираем пробы по 50 мл титрованием. На основе методики (пункт 3.1) определяем оптическую плотность пробы и находим концентрацию меди. Результаты представлены в таблице 3.5.
Таблица 3.5
|
С, ммоль/л |
||||
Построили график зависимости концентрации меди в фильтрате от объема прошедшего через ионит раствора.
Рис. 3.4
Процесс сорбции заключается в полном поглощении первых порций катионов катионитом, причем область поглощения постепенно перемещается по колонке к выходу. После этого наступает момент, когда, в силу исчерпания емкости катионита, катионы начинают выходить из колонны. Из графика видно, что концентрация меди на выходе из колонки увеличивается постепенно и имеет вид S-образной кривой, начиная от нулевых концентраций до максимальной. Эта кривая растягивается при маленьких концентрациях солей.
Рассчитали количество меди, поглотившегося колонкой до полного насыщения катионита, как площадь фигуры, ограниченной S-образной кривой и прямой максимальной концентрации:
н = ?Vi*(Cmax - Ci) (3)
где Vi = 50 мл,
Cmax = 3,6ммоль
н1 = 2,20 ммоль.
Рассчитали объемную емкость катионита:
з1 = н1/m к = 2,20/2 = 1,10 ммоль/гр. катионита.
Обсуждение результатов
В ходе экспериментальных работ определили полную обменную емкость трех различных катионитов (КУ-2-8, КУ-1, ВИОН КН-1). Результаты представлены на рисунке 3.5.

Полная обменная емкость катионита пропорциональна площади фигуры, ограниченной S-образной кривой и прямой максимальной концентрации. Как видно из рисунка 3.5. Емкости различных ионитов различны и меньше полной обменной емкости катионитов заявленных в паспорте. Так полная обменная емкость катионита КУ-2-8 найдена эксперементальным путем ниже паспортного значения на 28%, полная обменная емкость КУ-1 ниже паспортного значения на 57%, а ПОЕ катионита ВИОН КН-1 ниже на 39%. Эти данные необходимо учитывать при расчете и конструировании ионообменных аппаратов и фильтров.
Ионный обмен протекает на тех адсорбентах, которые являются полиэлектролитами (ионообменники, иониты, ионообменные смолы).
Ионный обменом называется процесс эквивалентного обмена ионов, находящихся в ионообменнике, на другие ионы того же знака, находящиеся в растворе. Процесс ионного обмена обратим.
Иониты подразделяются на катиониты, аниониты и амфотерные иониты.
Катиониты – вещества, содержащие в своей структуре фиксированные отрицательно заряженные группы (фиксированные ионы), около которых находятся подвижные катионы (противоионы), которые могут обмениваются с катионами, находящимися в растворе (рис. 81).
Рис. 81. Модель матрицы полиэлектролита (катионита) с фиксированными анионами и подвижными противоионами, где – – фиксированные ионы;
– коионы, – противоионы
Различают природные катиониты: цеолиты, пермутиты, силикагель, целлюлоза, а также искусственные: высокомолекулярные твердые нерастворимые ионогенные полимеры, содержащие чаще всего сульфогруппы, карбоксильные, фосфиновокислые, мышьяковокислые или селеновокислые группы. Реже применяются синтетические неорганические катиониты, являющиеся чаще всего алюмосиликатами.
По степени ионизации ионогенных групп катиониты делят на сильнокислотные и слабокислотные. Сильнокислотные катиониты способны обменивать свои подвижные катионы на внешние катионы в щелочной, нейтральной и кислой средах. Слабокислотные катиониты обменивают противоионы на другие катионы только в щелочной среде. К сильнокислотным относят катиониты с сильно диссоциированными кислотными группами – сульфокислотными. К слабокислотным относят катиониты, содержащие слабодиссоциированные кислотные группы – фосфорнокислотные, карбоксильные, оксифенильные.
Аниониты – ионообменники, которые содержат в своей структуре положительно заряженные ионогенные группы (фиксированные ионы), около которых находятся подвижные анионы (противоионы), которые могут обмениваться с анионами, находящимися в растворе (рис. 82). Различают природные и синтетические аниониты.

Рис. 82. Модель матрицы полиэлектролита (анионита) с фиксированными катионами и подвижными противоионами, где + – фиксированные ионы;
– коионы, – противоионы
Синтетические аниониты содержат в макромолекулах положительно заряженные ионогенные группы. Слабоосновные аниониты имеют в своем составе первичные, вторичные и третичные аминогруппы, сильноосновные аниониты содержат группы четвертичных ониевых солей и оснований (аммониевых, пиридиниевых, сульфониевых, фосфониевых). Сильноосновные аниониты обменивают подвижные анионы в кислой, нейтральной и щелочной средах, слабоосновные – только в кислой среде.
Амфотерные иониты содержат и катионные, и анионные ионогенные группы. Эти иониты могут сорбировать одновременно и катионы и анионы.
Количественной характеристикой ионита является полная обменная емкость (ПОЕ). Определение ПОЕ можно осуществить статическим или динамическим методом, основанном на реакциях, протекающих в системе «ионит – раствор»:
RSO 3 – H + + NaOH → RSO 3 – Na + + H 2 O
RNH 3 + OH – + HCl → RNH 3 + Cl – + H 2 O
Емкость определяется числом ионогенных групп в ионите и поэтому теоретически должна быть постоянной величиной. Однако практически она зависит от ряда условий. Различают статическую обменную емкость (СОЕ) и динамическую обменную емкость (ДОЕ). Статическая обменная емкость - полная емкость, характеризующая общее количество ионогенных групп (в миллиэквивалентах), приходящихся на единицу массы воздушно-сухого ионита или нa единицу объема набухшего ионита. Природные иониты имеют небольшую статическую обменную емкость, не превышающую 0,2-0,3 мэкв/г. Для синтетических ионообменных смол она находится в пределах 3-5 мэкв/г, а иногда достигает 10,0 мэкв/г.
Динамическая, или рабочая, обменная емкость относится только к той части ионогеппых групп, которые участвуют в ионном обмене, протекающем в технологических условиях, например, в ионообменной колонке при определенной относительной скорости движения ионита и раствора. Динамическая емкость зависит от скорости движения, размеров колонки и других факторов и всегда меньше статической обменной емкости.
Для определения статической обменной емкости ионитов применяют различные методы. Все эти методы сводятся к насыщению ионита каким-либо ионом, затем вытеснению его другим ионом и анализу первого в растворе. Например, катионит удобно полностью перевести в Н + -форму (противоионами являются ионы водорода), затем промыть его раствором хлорида натрия и полученный кислый раствор оттитровать раствором щелочи. Емкость равна отношению количества перешедшей в раствор кислоты к навеске ионита.
При статическом методе титруют кислоту или щелочь, которые в результате ионообменной адсорбции появляются в растворе.
При динамическом методе ПОЕ определяется с помощью хроматографических колонок. Через колонку, заполненную ионообменной смолой, пропускают раствор электролита и регистрируют зависимость концентрации поглощаемого иона в выходящем растворе (элюате) от объема прошедшего раствора (выходная кривая). ПОЕ рассчитывают по формуле
 , ,
| (337) |
где V общ – суммарный объем раствора, содержащий вытесненную из смолы кислоту; с – концентрация кислоты в этом растворе; m – масса ионообменной смолы в колонке.
Константу равновесия ионного обмена можно определить из данных о равновесном распределении ионов в статических условиях (равновесное состояние при ионном обмене описывается законом действия масс), а также динамическим методом по скорости перемещения зоны вещества по слою смолы (элюентная хроматография).
Для реакции ионного обмена
![]()
константа равновесия равна
 , ,
| (338) |
где , – концентрация ионов в ионите; , – концентрация ионов в растворе.
Применяя иониты, можно умягчить воду или опреснять засоленную воду и получать пригодную для фармацевтических целей. Другое применение ионообменной адсорбции в фармации состоит в использовании его для аналитических целей как метода извлечения из смесей того или другого анализируемого компонента.
Примеры решения задач
1. В 60 мл раствора с концентрацией некоторого вещества 0,440 моль/л поместили активированный уголь массой 3 г. Раствор с адсорбентом взбалтывали до установления адсорбционного равновесия, в результате чего концентрация вещества снизилась до 0,350 моль/л. Вычислите величину адсорбции и степень адсорбции.
Решение:
Адсорбция рассчитывается по формуле (325):

По формуле (326) определяем степень адсорбции
2. По приведенным данным для адсорбции димедрола на поверхности угля рассчитайте графически константы уравнения Ленгмюра:
Рассчитайте адсорбцию димедрола при концентрации 3,8 моль/л.
Решение:
Для графического определения констант уравнения Ленгмюра используем линейную форму этого уравнения (327):
Рассчитаем значения 1/а и 1/с :
Строим график в координатах 1/а – 1/с (рис. 83).
Рис. 83. Графическое определение констант уравнения Ленгмюра
В том случае, когда точка х = 0 расположена за пределами рисунка, используют второй способ y=ax+b . Вначале выбираем две любые точки, лежащие на прямой (рис. 83) и определяем их координаты:
(·)1(0,15; 1,11); (·)2 (0,30; 1,25).

b= y 1 – ax 1 = 0,11 – 0,93· 0,15 = 0,029.
Получаем, что b = 1/а ¥ = 0,029 мкмоль/м 2 , следовательно а ¥ = 34,48 мкмоль/ м 2 .
Константа адсорбционного равновесия K определяется следующим образом:
Рассчитаем адсорбцию димедрола при концентрации 3,8 моль/л по уравнению Ленгмюра (327):
3. При изучении адсорбции бензойной кислоты на твердом адсорбенте получены следующие данные:
Решение:
Для расчета констант уравнения Фрейндлиха необходимо использовать линейную форму уравнения (332), в координатах lg(х/т ) – lgс изотерма имеет вид прямой.
Найдем значения lg c и lg x/m , входящие в линеаризованное уравнение Фрейндлиха.

| lg c | –2,22 | –1,6 | –1,275 | –0,928 |
| lg x/m | –0,356 | –0,11 | 0,017 | 0,158 |
Строим график в координатах lg(х/т ) – lgс (рис. 84).
Рис. 84. Графическое определение констант уравнения Фрейндлиха
Так как точка х = 0 расположена за пределами рисунка (84), используем второй способ определения коэффициентов прямой y=ax+b (См. «Вводный блок. Основы математической обработки экспериментальных данных»). Вначале выбираем две любые точки, лежащие на прямой (например, точки 1 и 2) и определяем их координаты:
(·)1 (–2,0; –0,28); (·)2 (–1,0; 0,14).
Затем рассчитываем угловой коэффициент по формуле:

b= y 1 – ax 1 = –0,28 – 0,42 · (–2,0) = 0,56.
Константы уравнения Фрейндлиха равны:
lgK = b= 0,56; K = 10 0,56 = 3,63;
1/n = а = 0,42.
Рассчитаем адсорбцию бензойной кислоты при концентрации 0,028 моль/л, используя уравнение Фрейндлиха (330):
4. Используя уравнение БЭТ, рассчитайте удельную поверхность адсорбента по данным об адсорбции газообразного азота:
Площадь, занимаемая молекулой азота в плотном монослое, равна 0,08 нм 2 , плотность азота 1,25 кг/м 3 .
Решение:
Уравнение изотермы полимолекулярной адсорбции БЭТ в линейной форме имеет вид (333)
Для построения графика определим значения:
Строим график в координатах – p/p s (рис. 85).
Используем первый способ (См. «Вводный блок. Основы математической обработки экспериментальных данных») определения коэффициентов прямой y=ax+b. По графику определяем значение коэффициента b , как ординату точки, лежащей на прямой, у которой абсцисса равна 0 (х = 0): b = 5.Выбираем точку на прямой и определяем ее координаты:
(·)1 (0,2; 309).
Затем рассчитываем угловой коэффициент:


Рис. 85. Графическое определение констант уравнения изотермы полимолекулярной адсорбции БЭТ
Константы уравнения изотермы полимолекулярной адсорбции БЭТ равны:
 ; .
; .
Решая систему уравнений, получаем а ∞ = 6,6·10 –8 м 3 /кг.
Чтобы вычислить предельное значение адсорбции, отнесем а ∞ к 1 моль:
 .
.
Величину удельной поверхности адсорбента находим по формуле (329):
5. Полистирольный сульфокатионит в Н + -форме массой 1 г внесли в раствор KCl с исходной концентрацией с 0 = 100 экв/м 3 объемом V = 50 мл и смесь выдержали до равновесного состояния. Рассчитайте равновесную концентрацию калия в ионите, если константа ионообменного равновесия = 2,5, а полная обменная емкость катионита ПОЕ = 5 моль-экв/кг.
Решение:
Для определения константы ионного обмена используем уравнение (338). В смоле ионы Н + обмениваются на эквивалентное количество ионов K
Масса сульфокатионита в Н + -форме определяется по формуле (337):


Суммарное количество анионита в ОН – -форме равно:
Масса анионита в ОН – -форме также определяется по формуле (337):
